Des chercheurs révèlent que la cnicine, un composé extrait du chardon béni (une plante à fleurs), favorise la régénération nerveuse en accélérant considérablement la croissance des axones. En administrant quotidiennement le composé à des modèles murins atteints de lésions nerveuses graves, une récupération fonctionnelle significative a été observée. Ces résultats mettent en évidence le potentiel d’une plante médicinale couramment utilisée pour les atteintes nerveuses.
Suite à une lésion, les axones (les prolongements des cellules nerveuses) du système nerveux périphérique possèdent une excellente capacité de régénération. Cependant, malgré cette capacité, la récupération fonctionnelle complète est généralement difficile à obtenir. En effet, les cellules de Schwann (entourant certains axones) cessent de soutenir la croissance des axones au bout de 3 mois. Étant donné que les axones se régénèrent à une vitesse de 1 à 2 millimètres par jour, la régénération ne peut ainsi couvrir qu’une distance de 9 à 18 centimètres. Or, les lésions périphériques se produisent généralement sur des zones plus étendues, ce qui entrave la restauration complète des fonctions nerveuses.
Les stratégies thérapeutiques permettant d’accélérer la croissance des axones constituent un domaine de recherche très actif. Parmi celles explorées figurent par exemple les facteurs de croissance nerveuse et le tacrolimus (un immunosuppresseur), qui ont montré des effets de régénération axonale chez des modèles animaux. Cependant, leur application clinique est limitée en raison de graves effets secondaires.
D’un autre côté, un composé appelé parthénolide et abondant dans la grande camomille (Tanacetum parthenium) a montré des effets neurorégénératifs prometteurs chez des modèles murins. Toutefois, ces résultats n’ont été observés qu’avec une administration intraveineuse, tandis que l’administration par voie orale s’est avérée inefficace en raison de sa faible biodisponibilité (la proportion du composé qui atteint la circulation sanguine sous sa forme inchangée).
Dans le cadre de leur nouvelle étude récemment parue dans la revue Phytomedicine, des chercheurs de l’Université de Cologne (en Allemagne) ont tenté d’identifier un composé structurellement similaire (induisant ainsi les mêmes effets) au parthénolide, mais dont la biodisponibilité orale serait meilleure. Ce dernier serait ainsi plus bénéfique pour une utilisation à long terme. Ils ont alors identifié la cnicine, un composé extrait du chardon béni (Cnicus benedictus), une plante à fleurs, qui est largement utilisé pour traiter différentes affections, dont certains troubles digestifs.
Une efficacité remarquable par voie orale
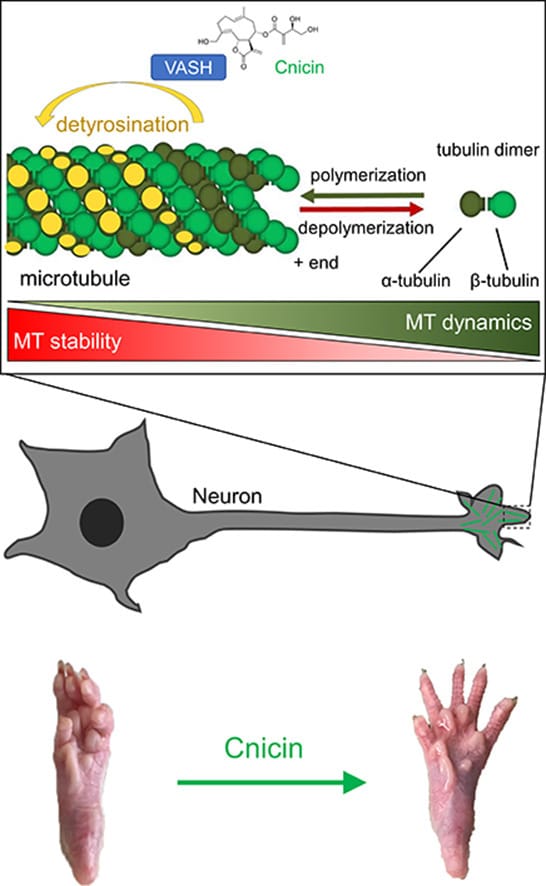
Afin d’évaluer les effets de la cnicine sur la régénération des axones, les chercheurs ont utilisé des cellules nerveuses prélevées sur des patients humains et des modèles animaux. Ils ont démontré que le composé est aussi efficace que le parthénolide pour inhiber la détyrosination des microtubules dans les extrémités des axones. Il s’agit d’un facteur critique influençant la croissance des axones. Plus précisément, les extrémités des axones en croissance possèdent une forte proportion en tyrosine (un acide aminé), qui diminue à mesure que cette croissance s’arrête.

Une autre partie de l’étude consistait à administrer le composé chez des rats et des souris ayant subi des lésions nerveuses graves induisant une neuropathie et une paralysie. L’administration intraveineuse du composé (dosé à 2 µg/kg) a considérablement accéléré la croissance des axones et la récupération des fonctions motrices. D’autre part, une efficacité similaire a été observée avec l’administration orale quotidienne de cnicine, avec une biodisponibilité orale de 84,7 %. « Ces résultats mettent en valeur le potentiel de la cnicine en tant que médicament prometteur pour traiter les atteintes axonales et améliorer la récupération fonctionnelle », indiquent les chercheurs dans leur document.
D’un autre côté, « trouver la dose correcte précise est crucial, car la cnicine n’agit que dans une fenêtre thérapeutique spécifique », précise Dietmar Fischer, coauteur principal de l’étude, dans un communiqué de l’Université de Cologne. « Les doses trop faibles ou trop élevées sont inefficaces. C’est pourquoi de nouvelles études cliniques sur l’homme sont cruciales », ajoute-t-il. En d’autres termes, il est essentiel de déterminer la dose exacte à administrer pour une application clinique.
En outre, il est important de noter que la régénération axonale doit être davantage accélérée chez l’Homme, car la distance à parcourir pour que les fibres nerveuses atteignent leur destination (pour restaurer les fonctions neuronales) y est plus importante que chez les modèles animaux. La prochaine étape de la recherche explorera les meilleures stratégies en vue des essais cliniques.


