Des chercheurs ont identifié une petite molécule qui réduit considérablement l’inflammation liée à l’âge et améliore les fonctions cérébrale et musculaire chez la souris. Le composé agit notamment en restaurant les niveaux de télomérase, une enzyme essentielle au maintien de l’intégrité des télomères et qui diminue avec l’âge. Ces résultats pourraient avoir d’importantes implications à la fois pour la lutte contre les maladies liées à l’âge et le cancer.
De nombreux changements épigénétiques surviennent avec le vieillissement et provoquent un déclin fonctionnel et physiologique progressif et irréversible. Parmi ces changements figure le raccourcissement des télomères, les structures surmontant les extrémités des chromosomes et contribuant à leur stabilité.
Les télomères sont des séquences complexes comportant jusqu’à 15 000 paires de bases. Ils perdent entre 25 et 200 paires de bases à chaque processus de division cellulaire. Ces pertes peuvent être exacerbées par le stress oxydatif. Lorsque les télomères deviennent trop courts ou trop altérés, cela déclenche une cascade de dommages à l’ADN, pouvant conduire à la sénescence cellulaire (un phénomène de vieillissement cellulaire au cours duquel des marqueurs inflammatoires sont libérés et endommagent les tissus).
Le raccourcissement des télomères est compensé par la télomérase (ou transcriptase inverse de la télomérase, ou TERT), une enzyme induisant la synthèse et l’extension des télomères. Cependant, l’activité de cette enzyme diminue avec l’âge. Des études ont par exemple mis au jour une corrélation entre la diminution de cette enzyme et des pathologies liées à l’âge, telles qu’Alzheimer. Des souris chez lesquelles les allèles TERT ont été désactivés présentent des syndromes progériques (vieillissement prématuré) et des affections inflammatoires et dégénératives chroniques.
« La répression épigénétique du TERT joue un rôle majeur dans le déclin cellulaire observé au début du vieillissement, en régulant les gènes impliqués dans l’apprentissage, la mémoire, la performance musculaire et l’inflammation », explique dans un communiqué Ronald DePinho, du MD Anderson Cancer Center de l’Université du Texas. DePinho et ses collègues ont alors suggéré qu’en restaurant les taux de TERT à des niveaux équivalents à ceux des individus jeunes, il est possible d’inverser divers processus liés au vieillissement. Dans une nouvelle étude publiée dans la revue Cell, ils ont identifié un composé ciblant spécifiquement le gène TERT à cet effet.
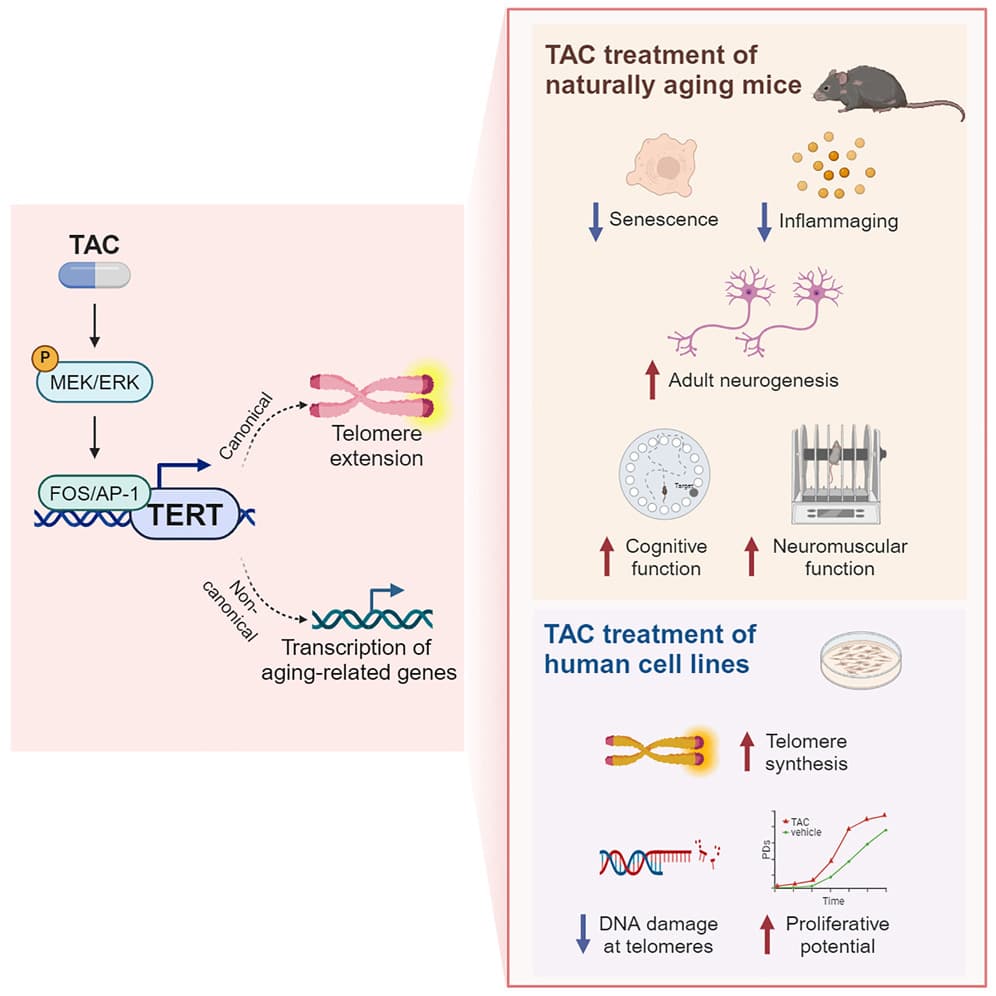
Une formation de nouveaux neurones après 6 mois
Pour identifier le nouveau composé, l’équipe de recherche a réalisé un criblage à haut débit incluant plus de 650 000 molécules candidates pouvant potentiellement « déréprimer » le gène TERT et restaurer son expression à un niveau équivalent à celui des jeunes cellules. Après avoir identifié le bon composé activateur de TERT (TAC), les chercheurs ont effectué des essais sur des modèles précliniques (des souris) dont l’âge équivalait à des adultes humains de plus de 75 ans, ainsi que sur des cellules humaines sénescentes.
Une augmentation de la synthèse des télomères au niveau des lignées cellulaires humaines a été observée. Cette augmentation était accompagnée d’une réduction des dommages à l’ADN, ce qui a amélioré la capacité des cellules à se multiplier. Ces constats suggèrent que le composé est facilement absorbé par les cellules et interagit efficacement avec les gènes présents.
Chez les souris, il a été constaté que le composé induisait la formation de nouveaux neurones au niveau de l’hippocampe (la région cérébrale responsable de la mémoire) en seulement 6 mois de traitement. Ces résultats étaient corrélés à une amélioration des performances cognitives, une augmentation de l’expression des gènes impliqués dans l’apprentissage et la mémoire ainsi qu’à une hausse de la connectivité synaptique.
Une amélioration significative de la fonction neuromusculaire, de la coordination, de la force de préhension (force maximale volontaire de la main) et de la vitesse de déplacement a également été observée. Cela suggère une inversion de la sarcopénie, une condition au cours de laquelle la masse, la force et les performances musculaires se détériorent naturellement avec l’âge.
Ces observations concordent avec les hypothèses de précédentes études, suggérant la capacité de TERT à interagir et à contrôler l’activité de différents facteurs de transcription. « En restaurant pharmacologiquement les niveaux de TERT, nous avons reprogrammé l’expression de ces gènes, ce qui a permis d’améliorer la cognition et les performances musculaires, tout en éliminant les caractéristiques relatives à de nombreuses maladies liées à l’âge », explique DePinho.
D’autre part, le composé TAC a réduit considérablement « l’inflammaging » (un processus au cours duquel les marqueurs inflammatoires liés à diverses maladies augmentent avec l’âge) dans les échantillons de sang et de tissus humains. L’activité du gène p16, un facteur clé de sénescence, a aussi été réduite — ce qui implique une diminution significative des cellules vieillissantes.
Toutefois, bien que ces résultats soient encourageants, davantage de recherches sont nécessaires pour évaluer correctement l’efficacité et surtout l’innocuité du composé. Il est en effet important de savoir qu’un taux élevé de télomérase est associé à la prolifération exacerbée des cellules cancéreuses. Néanmoins, « notre compréhension plus approfondie des mécanismes moléculaires à l’origine du processus de vieillissement a permis de découvrir des cibles médicamenteuses viables, ce qui nous permet d’explorer des possibilités d’intercepter les causes d’une variété de maladies chroniques liées à l’âge », conclut DePinho.