Des chercheurs ont identifié une molécule pouvant restaurer efficacement les fonctions cognitives et la mémoire chez les modèles murins d’Alzheimer — une première pour les stratégies de traitement de la maladie. Le composé stimule notamment les neurones à déclenchement rapide responsables de la génération d’oscillations gamma, essentielles à la mémoire et à la cognition.
Depuis plusieurs décennies, il est largement admis que la pathogénicité de la maladie d’Alzheimer provient notamment de l’accumulation de plaques de protéines bêta-amyloïdes au niveau des neurones (théorie de la « cascade amyloïde »). La plupart des stratégies thérapeutiques, y compris les médicaments approuvés par la Food and Drug Administration (tels que le lécanemab et l’aducanumab), se concentrent ainsi sur l’élimination de ces plaques.
Cependant, bien qu’il ait été démontré que cette approche permettait de ralentir la progression de la maladie, sa capacité à inverser les troubles cognitifs (se traduisant par des états de confusion s’aggravant avec le temps) est considérablement limitée. « Ils laissent derrière eux un cerveau qui est peut-être sans plaques, mais toutes les altérations pathologiques dans les circuits et les mécanismes des neurones ne sont pas corrigées », explique Istvan Mody, professeur de neurologie et de physiologie à l’École de médecine David Geffen de l’Université de Californie à Los Angeles (UCLA Health).
D’autre part, les médicaments visant à éliminer les plaques amyloïdes comportent généralement d’importants effets secondaires. Les essais cliniques ont montré qu’ils pouvaient causer des œdèmes et des hémorragies cérébrales parfois fatales.
Ces constats ont conduit à l’exploration de nouvelles approches thérapeutiques. Dans cette vision, Mody et ses collègues proposent un nouveau composé pouvant réactiver les signaux neuronaux régissant les fonctions cognitives et la mémoire. En d’autres termes, la molécule ne cible pas les plaques amyloïdes, mais intervient plutôt au niveau d’un mécanisme biomoléculaire jusqu’à présent non exploré dans la recherche de traitements anti-Alzheimer. « Il n’existe vraiment rien de tel sur le marché ou expérimentalement qui ait démontré son efficacité », indique Mody.
Une approche inédite ciblant pharmacologiquement les ondes gamma
Pour activer ou suspendre les fonctions neuronales, le cerveau émet de façon rythmique des signaux électriques à différentes fréquences. Parmi ces signaux figurent les ondes gamma (30 à 120 Hz), qui font partie des oscillations à haute fréquence. Générées par des interneurones à déclenchement rapide contenant de la parvalbumine (une protéine fixatrice de calcium), ces oscillations régissent les circuits neuronaux sous-jacents aux processus cognitifs et à la mémoire de travail, le type de mémoire qu’on utilise par exemple pour se souvenir d’un numéro de téléphone.
Des études ont précédemment montré que chez les patients présentant des symptômes précoces d’Alzheimer, les oscillations gamma étaient réduites avant même que les plaques amyloïdes ne s’accumulent et n’altèrent les fonctions cognitives. Cet effet a également été observé pour d’autres troubles neurodéveloppementaux et neurologiques tels que Parkinson, la dépression, les troubles du spectre de l’autisme (TSA), la schizophrénie, l’épilepsie, etc.
Afin de réduire les symptômes d’Alzheimer, des chercheurs ont antérieurement tenté d’utiliser des stimulations sonores et visuelles à 40 Hz (l’équivalent de la fréquence du ronronnement des chats) pour moduler les oscillations gamma. Cependant, bien que les niveaux de plaques amyloïdes aient été significativement réduits, l’amélioration cognitive obtenue était limitée.
Dans le cadre de la nouvelle étude, détaillée dans la revue PNAS, Mody et son équipe ont évalué si une approche pharmacologique pourrait être plus efficace. En effet, en interagissant avec l’acide gamma-aminobutyrique (GABA), certains récepteurs au niveau des interneurones à parvalbumine induisent une réduction des oscillations gamma. La GABA est le principal neurotransmetteur inhibiteur du système nerveux central chez les mammifères et les oiseaux, empêchant l’activation prolongée des neurones.
Les chercheurs ont développé le composé DDL-920 afin d’inhiber ces récepteurs, permettant ainsi aux interneurones d’émettre des oscillations gamma plus puissantes. « Notre approche est unique, car elle vise à améliorer les performances cognitives et la mémoire de travail en engageant et en amplifiant les oscillations gamma endogènes du cerveau, en améliorant la fonction des interneurones paravalbumines », expliquent-ils dans leur document.
Une cognition et une mémoire améliorées après deux semaines de traitement
Afin d’évaluer l’efficacité du composé DDL-920 pour le traitement d’Alzheimer, l’équipe a sélectionné des modèles murins génétiquement modifiés pour leur induire les symptômes de la maladie et âgés de 3 à 4 mois (l’équivalent d’un humain d’environ 26 ans). La molécule a été administrée deux fois par jour par voie orale pendant deux semaines. Leurs performances cognitives ont ensuite été testées par le biais d’un « labyrinthe de Barnes », une plateforme circulaire comportant différents indices visuels et débouchant sur un trou d’évacuation. Les souris devaient se souvenir de l’emplacement de cette ouverture.
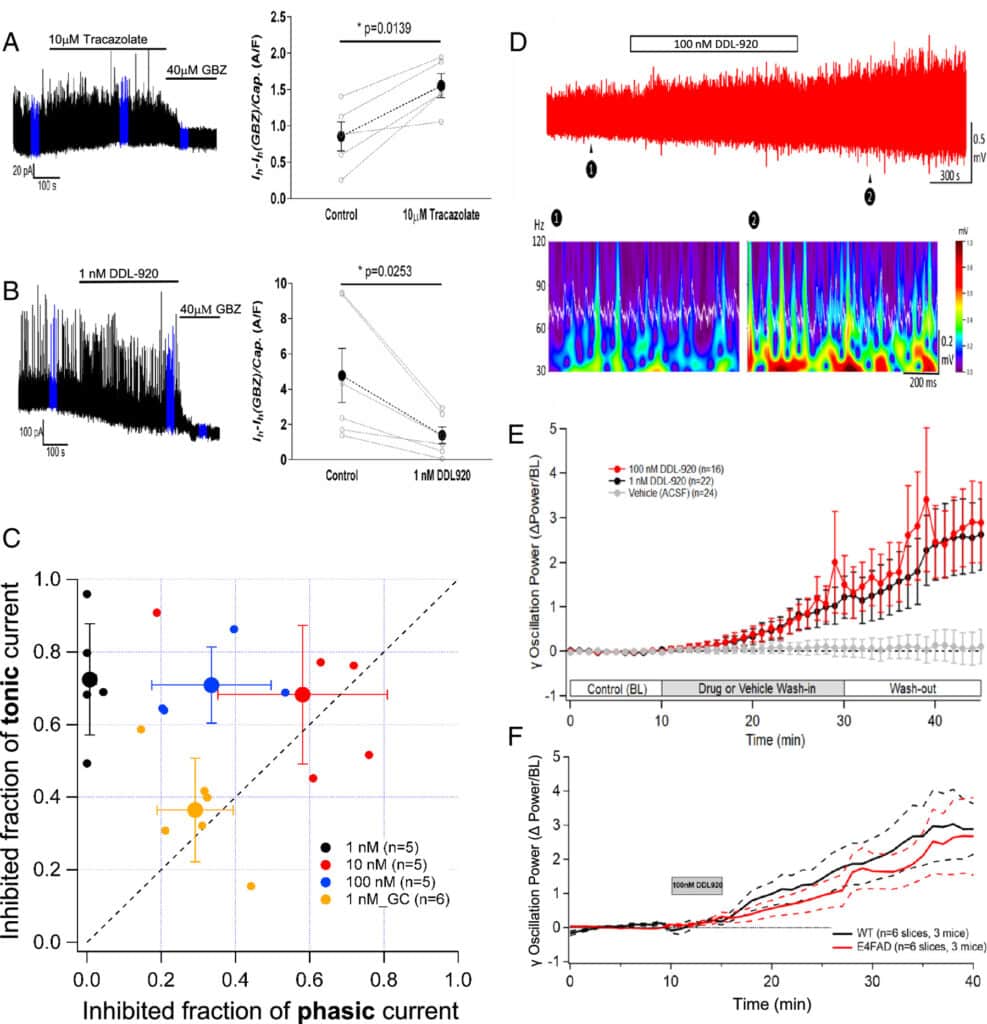


Les chercheurs ont constaté qu’après deux semaines de traitement, les souris malades étaient capables de résoudre le labyrinthe aussi bien que celles saines. D’autre part, aucune anomalie comportementale, hyperactivité ou autres effets secondaires n’ont été observés. Ces résultats suggèrent que les interneurones paravalbumines ont été correctement stimulés et la génération d’oscillations gamma relancée. Cet effet a ensuite été confirmé in vitro.
Toutefois, bien que l’efficacité du traitement soit démontrée chez les souris, davantage de recherches sont nécessaires afin de déterminer si les résultats peuvent être reproduits chez l’Homme — sans compter que les modèles murins de l’étude sont relativement jeunes. Le temps de traitement devra également être prolongé lors des prochains essais afin de s’assurer de l’innocuité du composé. Néanmoins, si les prochains résultats sont concluants, le traitement pourrait aussi être appliqué à d’autres maladies à ondes gamma réduites, telles que la maladie de Parkinson, les TSA et la dépression.