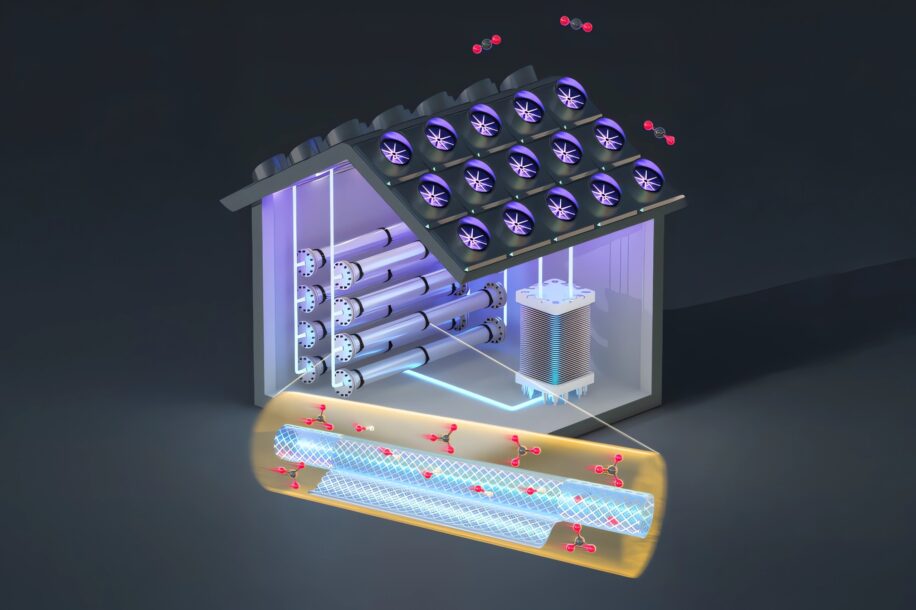
En utilisant un système de nanofiltration spécialisé, des chercheurs sont parvenus à améliorer près de six fois l’efficacité de capture et de libération électrochimique de CO₂. Les deux processus se heurtaient jusqu’ici à des obstacles majeurs, l’optimisation de l’un s’effectuant au détriment de l’autre. La nouvelle technologie de filtration permettrait de réduire les coûts d’au moins 20 %, ouvrant ainsi la voie aux systèmes de séquestration de carbone plus efficaces et plus abordables.
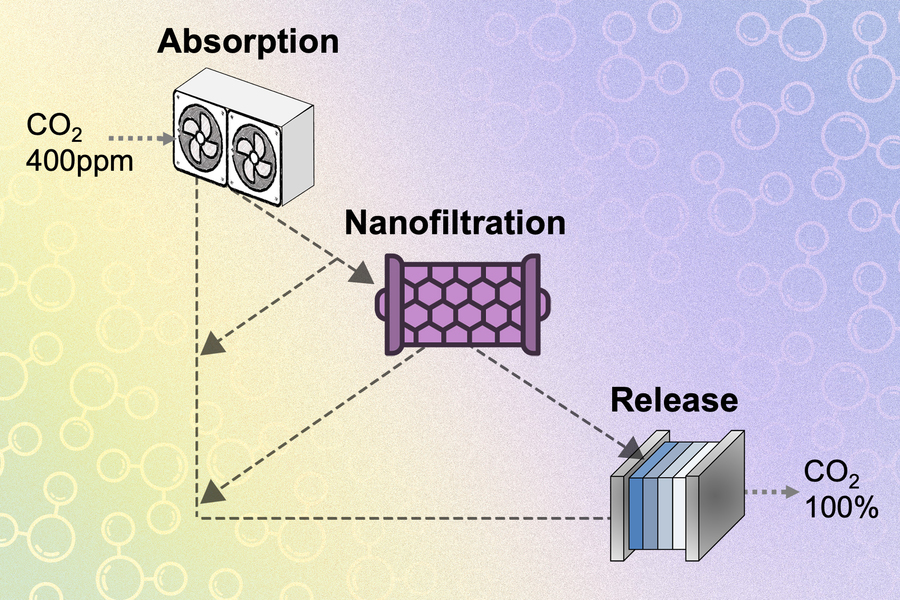
La plupart des systèmes électrochimiques de capture de carbone s’appuient sur des composés chimiques appelés hydroxydes. Ces derniers se combinent aisément au CO₂ pour former du carbonate. À son tour, le carbonate peut ensuite être introduit dans des cellules électrochimiques, où il réagit avec un acide dans une réaction acide-base, formant de l’eau et libérant à nouveau le dioxyde de carbone. Ce cycle fermé permet de traiter l’air ambiant, qui contient en moyenne 400 parties par million (ppm) de CO₂, et de générer un flux de CO₂ pur à 100 % pour diverses utilisations, telles que la fabrication de carburants.
Cependant, leur efficacité se heurte à deux obstacles majeurs : les composés permettant d’éliminer le CO₂ de l’air ne le libèrent pas facilement après l’avoir capturé. Inversement, les composés facilitant la libération du CO₂ ne le capturent pas aussi efficacement. Optimiser l’une des étapes a tendance à altérer l’autre, et inversement.
Les étapes de capture et de libération utilisent toutes deux une solution à base d’eau, mais la première utilise une solution avec une concentration élevée en ions hydroxydes, tandis que la seconde nécessite une solution riche en ions carbonate.
« On voit bien que ces deux étapes sont difficilement compatibles », explique dans un article de blog, Kripa Varanasi, professeur de génie mécanique au Massachusetts Institute of Technology (MIT). « Ces deux systèmes font circuler le même sorbant. Ils utilisent exactement le même liquide. Mais comme ils ont besoin de deux types de liquides différents pour fonctionner de manière optimale, il est impossible d’exploiter les deux systèmes à leur point d’efficacité maximal », indique-t-il.
Pour surmonter ces obstacles, l’équipe de Varanasi propose de découpler les deux étapes en introduisant une troisième entre elles, notamment en utilisant un système de nanofiltration. Les résultats – parus cette semaine dans la revue ACS Energy Letters – montrent une amélioration significative de l’équilibre entre capture et libération de CO₂, sans compromis entre les deux. Cette technique permettrait, à terme, de rendre les systèmes économiquement viables, un aspect essentiel à leur mise à l’échelle.
« Nous devons penser à l’échelle dès le départ en matière de captage du carbone, car pour avoir un impact significatif, il faut traiter des gigatonnes de CO₂ », explique Varanasi. « Adopter cet état d’esprit nous aide à identifier les principaux goulots d’étranglement et à concevoir des solutions innovantes avec un réel potentiel d’impact. C’est le moteur de notre travail », ajoute-t-il.
Une efficacité de séparation ionique de 95 %
Les membranes de nanofiltration développées par Varanasi et ses collègues permettent de séparer les ions de la solution en fonction de leur charge, lorsque les hydroxydes de la première étape de capture sont convertis en carbonate. Les ions carbonate ont une charge de 2 et les ions hydroxydes une charge de 1. « La nanofiltration est capable de séparer ces deux éléments assez bien », affirme Simon Rufer, doctorant au MIT et auteur principal de l’étude.
Une fois séparés, les ions hydroxyde sont réinjectés dans le système d’absorption, tandis que les ions carbonates sont introduits dans l’étape de libération électrochimique. De cette manière, les deux extrémités du système fonctionneraient à leur plus haut niveau d’efficacité. Lors de la libération, des protons sont habituellement ajoutés au carbonate afin de le convertir en CO₂ et en eau dans une réaction acide-base.
Cependant, si des ions hydroxydes sont également présents, les protons réagissent avec eux et produisent uniquement de l’eau. « Si l’on ne sépare pas ces hydroxydes et carbonates, le système échoue : on ajoute des protons à l’hydroxyde au lieu du carbonate, et on ne fait que produire de l’eau au lieu d’extraire du dioxyde de carbone », explique Rufer. « C’est là que l’efficacité est compromise. » Les essais de l’équipe ont montré que la nanofiltration permettait de séparer les ions carbonates des ions hydroxydes avec une efficacité de 95 %.
Un coût global réduit à 450 dollars par tonne de CO₂ capté
Pour évaluer l’efficacité globale et la rentabilité du nouveau procédé, les chercheurs ont développé un modèle technico-économique intégrant différents paramètres, tels que le rendement électrochimique, le taux d’absorption, les coûts d’investissement, l’efficacité de nanofiltration, etc.
Les analyses ont montré que l’ajout de la nanofiltration réduirait les coûts à 450 dollars par tonne de CO₂ capté, contre 600 dollars pour les procédés conventionnels. L’efficacité de la capture et de la libération de carbone serait, quant à elle, multipliée par six. D’autre part, le nouveau système serait beaucoup plus stable et continuerait de fonctionner avec une efficacité élevée, même si la concentration ionique de la solution fluctue.
« Avec l’ancien système sans nanofiltration, on fonctionnait sur le fil du rasoir ; si la concentration varie, même légèrement, dans un sens ou dans l’autre, l’efficacité chute considérablement », explique Rufer. « Mais avec notre système de nanofiltration, il agit comme un tampon et devient beaucoup plus tolérant aux variations. Le régime opérationnel est beaucoup plus large et les coûts peuvent être considérablement réduits », affirme-t-il.
Les chercheurs suggèrent en outre que l’approche pourrait non seulement s’appliquer aux systèmes de capture de CO₂ direct de l’air, mais également aux systèmes directement reliés aux sources d’émissions, comme les centrales électriques. Le nouveau système serait aussi plus sûr, car il permet d’utiliser des solutions qui n’offrent peut-être pas les meilleurs taux d’absorption, mais qui peuvent être améliorées tout en offrant davantage de sécurité.
L’équipe prévoit prochainement d’améliorer le système de sorte à atteindre un coût économiquement viable, soit environ 200 dollars par tonne de CO₂ capté. L’adaptabilité aux installations de captage de carbone existantes sera également étudiée.