En étudiant les mécanismes permettant aux escargots de régénérer leurs yeux après une blessure ou une amputation, des biologistes ont identifié un gène clé impliqué dans leur développement oculaire, également présent chez l’humain. Cela en fait un modèle de choix pour l’étude de la régénération oculaire et pourrait, à terme, déboucher sur des traitements régénératifs pour des pathologies humaines, telles que la dégénérescence maculaire.
Le bon fonctionnement des organes est étroitement lié à leur développement durant le stade embryonnaire. Celui-ci repose sur un processus complexe, obéissant à une succession d’étapes précises et minutées de différenciation cellulaire et d’organisation tissulaire, qui aboutit à la formation d’un organisme fonctionnel. Toutefois, après cette phase, de nombreux animaux — les humains notamment — perdent la capacité à régénérer entièrement leurs organes.
D’autres espèces, en revanche, comme les axolotls, les poulpes ou certains escargots, conservent cette faculté tout au long de leur vie. Les escargots, en particulier, sont réputés depuis des siècles pour leur étonnante capacité de régénération. Dès 1766, un naturaliste observait que ceux de son jardin pouvaient faire repousser entièrement leur tête après décapitation.
Étonnamment, ces mollusques demeurent peu étudiés dans la recherche en biologie régénérative. « Quand j’ai commencé à me documenter sur le sujet, je me suis demandé pourquoi personne n’utilisait encore les escargots pour étudier la régénération », déclare, dans un communiqué, Alice Accorsi, professeure adjointe à l’université de Californie à Davis. « Je pense que c’est parce que nous n’avions tout simplement pas encore trouvé l’escargot idéal. Beaucoup d’espèces sont difficiles, voire très lentes, à élever en laboratoire ; d’autres passent par une métamorphose, ce qui complexifie les protocoles », avance-t-elle.
En collaboration avec le Stowers Institute for Medical Research, Accorsi et ses collègues ont opté pour l’escargot-pomme (Pomacea canaliculata), dont les yeux, bien que ceux d’un invertébré, présentent des similarités structurelles avec ceux des humains. Mais à la différence de l’œil humain, ils peuvent se régénérer intégralement après une lésion ou une ablation.
« Les escargots-pommes sont des organismes remarquables. Ils offrent une opportunité unique pour étudier la régénération d’organes sensoriels complexes. Jusqu’ici, il nous manquait un système permettant d’examiner la régénération complète de l’œil », souligne la chercheuse dans un article de blog publié par l’université.
Des yeux anatomiquement et génétiquement proches de ceux des humains
Originaire d’Amérique du Sud, l’escargot-pomme est une espèce d’eau douce désormais considérée comme envahissante dans de nombreuses régions du globe. Résilient, prolifique, facile à élever, et présentant un temps de régénération très court après blessure, il constitue un modèle de laboratoire particulièrement adapté.
Comme chez les humains et d’autres vertébrés, ses yeux sont de type « caméra » : ils génèrent des images en haute résolution grâce à la présence d’une cornée, d’un cristallin focalisant la lumière, et d’une rétine garnie de cellules photoréceptrices. L’étude, parue dans la revue Nature Communications, montre que ces organes présentent, sur le plan anatomique et génétique, des ressemblances significatives avec ceux des humains — du moins pour certaines structures et certains gènes impliqués.
Les auteurs discutant de la manière dont les escargots-pommes pourraient être utilisé comme modèle pour l’étude de la régénération oculaire :
Une régénération quasi complète en 28 jours
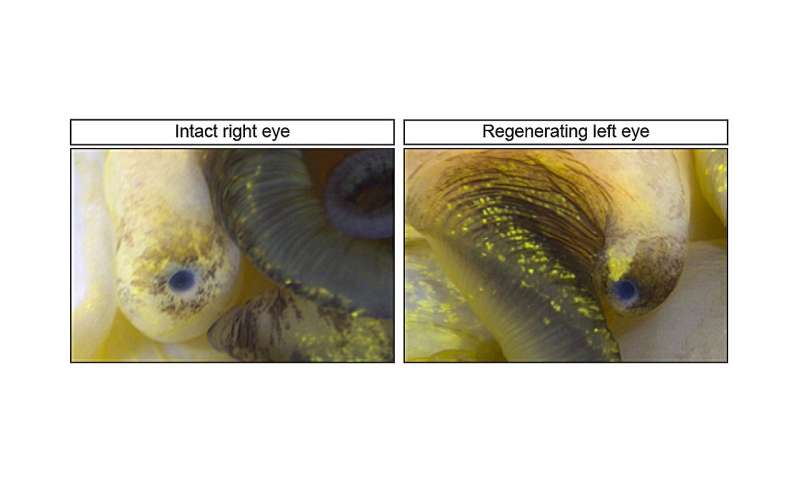
Afin de comprendre le processus de régénération, les chercheurs ont suivi chaque étape, de l’amputation à la reformation complète de l’œil. Ils ont observé que le processus dure environ un mois (le 28e jour de régénération) et comprend plusieurs phases successives.
La première, qui dure environ 24 heures, correspond à la cicatrisation, essentielle pour éviter les infections et la perte de liquide corporel. Ensuite, des cellules indifférenciées migrent vers la zone lésée et s’y multiplient, formant un amas cellulaire.
Après environ dix jours, ces cellules commencent à se spécialiser et donnent naissance aux premières structures : cristallin, rétine, puis nerf optique. À ce stade, toutes les composantes essentielles sont présentes, mais leur maturation se poursuit au fil des semaines. « Nous n’avons pas encore la preuve formelle que les escargots voient des images, mais anatomiquement, ils disposent de toutes les structures nécessaires à la formation d’une image », précise Accorsi.
En analysant l’expression des gènes au fil du processus, les chercheurs ont relevé que, peu après l’amputation, près de 9 000 gènes étaient exprimés à des niveaux différents par rapport aux escargots non blessés. Et le 28e jour, 1 175 gènes restaient encore exprimés différemment dans l’œil régénéré. Cela suggère que, bien que les yeux semblent entièrement régénérés à ce stade, leur maturation fonctionnelle requiert encore plus de temps.


Des perspectives d’application chez l’humain
Chez les vertébrés, seule la phase initiale de régénération — la cicatrisation — peut être accomplie. L’objectif de l’étude est donc d’identifier les mécanismes qui permettent à l’escargot-pomme de franchir les étapes suivantes, dans l’espoir de cibler leurs équivalents génétiques chez l’humain. « Nous avons beaucoup travaillé pour démontrer que de nombreux gènes impliqués dans le développement de l’œil humain sont également présents chez l’escargot », indique la biologiste.
Parmi eux, le gène Pax6, connu pour son rôle crucial dans l’organisation des tissus cérébraux et oculaires chez l’humain, la souris ou encore la drosophile. Les escargots possèdent également le gène Pax6, connu pour être impliqué dans le développement et l’organisation des tissus cérébraux et oculaires chez l’homme, la souris et la drosophile. Tout comme les humains, les escargots possèdent deux copies du gène, chacune héritée d’un parent. L’équipe a désactivé ce gène chez des embryons d’escargots à l’aide de la technologie CRISPR-Cas9 afin d’observer son rôle précis dans le développement oculaire. « L’idée est de muter des gènes spécifiques et de voir ensuite l’effet produit chez l’animal, ce qui peut nous éclairer sur la fonction de différentes séquences du génome », explique Accorsi.
Résultat : lorsque les deux copies de Pax6 sont inactivées, les embryons se développent sans yeux. L’étape suivante consistera à désactiver ce gène chez des escargots adultes pour tester son implication directe dans la régénération. D’autres gènes, codant pour des parties spécifiques de l’œil, seront également étudiés. « Si nous identifions un ensemble de gènes essentiels à la régénération oculaire, et que ceux-ci existent également chez les vertébrés, alors, en théorie, il pourrait devenir possible de les activer chez l’humain pour favoriser une régénération oculaire », conclut la chercheuse.
Vidéo de présentation de l’étude: