Des chercheurs sont pour la première fois parvenus à développer le premier modèle pulmonaire humain sur puce à partir de cellules souches provenant d’un seul donneur. Alors que les modèles précédents s’appuyaient sur une combinaison de cellules d’origines diverses, la nouvelle plateforme simulerait efficacement les mouvements respiratoires tout en reflétant plus fidèlement la dynamique cellulaire chez un individu spécifique. La technologie pourrait ouvrir la voie à de meilleurs traitements contre les affections pulmonaires ainsi qu’une médecine personnalisée.
Les alvéoles pulmonaires constituent un micro-environnement tissulaire complexe et essentiel aux échanges gazeux. Elles constituent aussi une barrière naturelle contre les agents pathogènes respiratoires en abritant notamment des cellules immunitaires spécialisées qui y résident en permanence. Étant donné leur rôle dans le maintien de l’homéostasie et leur potentiel en tant que plateforme d’administration médicamenteuse, des modèles in vitro humains ont été développés afin de pallier les différences anatomiques avec les modèles animaux, ainsi que les préoccupations éthiques.
Les technologies d’organes sur puce sont proposées comme alternatives fiables aux modèles animaux. Il s’agit généralement d’unités en plastique gravées de microcompartiments et de canaux sur lesquels des cellules sont cultivées. Le développement de modèles pulmonaires sur puce humains se heurte cependant à des défis notables. L’un d’entre eux réside dans le fait que la conception de modèles pulmonaires fiables et adaptables dépend de la disponibilité d’une source quasi illimitée de cellules alvéolaires standardisées, en bonne santé et provenant d’un donneur unique.
Les dispositifs pulmonaires sur puces sont jusqu’ici composés de mélanges de cellules provenant d’un donneur humain spécifique et d’autres cellules de culture disponibles dans le commerce. Cette hétérogénéité ne permet pas de reproduire fidèlement les fonctions pulmonaires et les réactions à une maladie ou à un médicament chez un individu spécifique. Bien que l’utilisation de cellules souches pluripotentes induites humaines (iPSC) ait permis des avancées notables, leur intégration aux organes sur puce pour imiter un poumon distal demeure limitée.
Une nouvelle étude de l’Institut Francis Crick et de l’entreprise de biotechnologie Alveolix rapporte pour la première fois la mise au point d’un nouveau modèle de poumon sur puce qui ne contient que des cellules génétiquement identiques dérivées de cellules souches provenant d’un seul donneur.
« Compte tenu du besoin croissant de technologies non animales, les approches d’organes sur puce deviennent de plus en plus importantes pour recréer des systèmes humains, en évitant les différences d’anatomie pulmonaire, de composition des cellules immunitaires et de développement de la maladie entre les animaux et les humains », explique dans un communiqué Max Gutierrez, chef de groupe principal du laboratoire des interactions hôte-pathogène dans la tuberculose à l’Institut Francis Crick et coauteur principal de l’étude publiée le 1er janvier dans la revue Science Advances.
Un poumon sur puce génétiquement homogène
Pour créer leur dispositif alvéolaire sur puce, les chercheurs ont produit des cellules épithéliales alvéolaires de type I et II ainsi que des cellules endothéliales vasculaires à partir de cellules iPSC. Ces dernières peuvent se différencier en pratiquement n’importe quel type de cellules. Les deux lignées cellulaires dérivées des iPSC ont été cultivées séparément sur les faces supérieure et inférieure (respectivement) d’une membrane très fine, à l’intérieur d’un dispositif spécialement développé par Alveolix. L’ensemble vise à reproduire une barrière alvéolaire avec des cellules génétiquement identiques.
Afin de reproduire les contractions naturelles du poumon humain, l’équipe a utilisé des systèmes appliquant des forces d’étirement rythmiques et tridimensionnelles au niveau de la barrière alvéolaire, imitant ainsi le mouvement de la respiration. Outre l’amélioration des échanges gazeux, ce mouvement stimule également la formation de microvillosités, une caractéristique essentielle des cellules épithéliales alvéolaires permettant d’accroître la surface d’échange.
Vers des modèles pulmonaires personnalisés
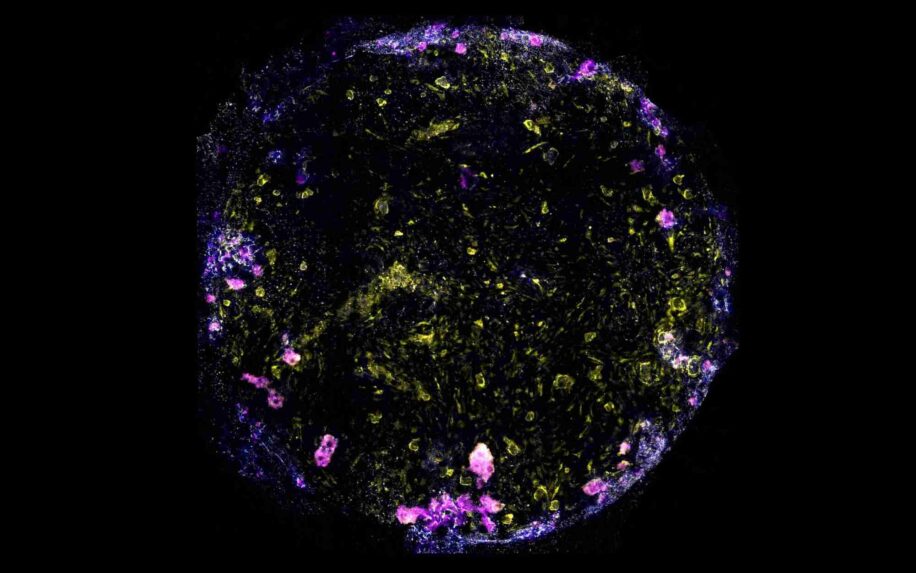
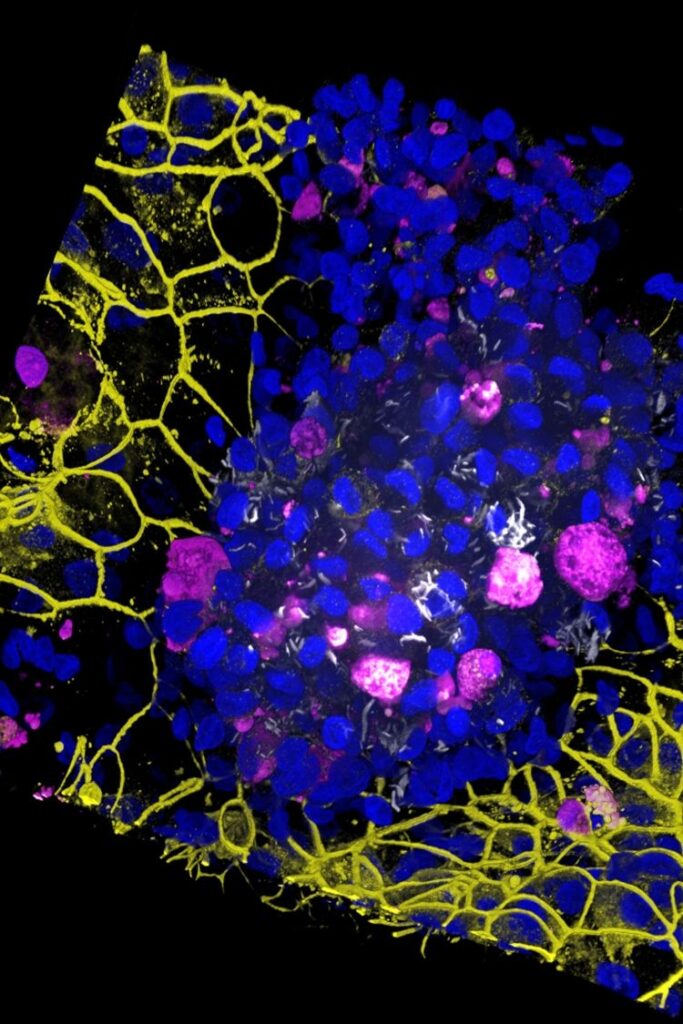
Pour évaluer les réactions de la puce à une infection, les chercheurs y ont ajouté des macrophages produits à partir des cellules souches du même donneur, puis ont inoculé des bacilles de Koch (les bactéries de la tuberculose ou Mycobacterium tuberculosis) pour simuler les premiers stades de la maladie.
« La tuberculose est une maladie à évolution lente, avec des mois entre l’infection et l’apparition des symptômes ; il est donc de plus en plus nécessaire de comprendre ce qui se passe aux premiers stades invisibles », explique Jakson Luk, chercheur postdoctoral au laboratoire de Gutierrez et auteur principal de l’étude.
Les résultats ont révélé que les puces infectées par la tuberculose présentaient de larges amas de macrophages avec des noyaux nécrotiques, c’est-à-dire des agglomérations avec des macrophages morts au centre et entourées de macrophages vivants. Ces observations indiquent que les cellules cultivées au niveau de la puce réagissaient de manière cohérente avec les mécanismes connus de réponse aux bactéries. Puis, cinq jours après l’infection, les barrières cellulaires endothéliales et épithéliales se sont effondrées, ce qui indiquerait une altération de la fonction des alvéoles pulmonaires.
« Nous sommes parvenus à reproduire avec succès ces événements initiaux de la progression de la tuberculose, ce qui nous permet d’obtenir une image globale de la façon dont les différentes cellules pulmonaires réagissent aux infections », affirme Luk.
D’après les chercheurs, le modèle pourrait être utilisé pour un large éventail de recherches, non seulement pour les infections respiratoires, mais également pour les cancers du poumon. Il pourrait ainsi être utilisé pour évaluer l’efficacité des antibiotiques et des traitements anti-cancéreux.
En outre, « composées de cellules génétiquement identiques, ces puces pourraient être fabriquées à partir de cellules souches provenant de personnes présentant des mutations génétiques particulières », souligne Gutierrez. L’équipe travaille actuellement à l’amélioration du modèle en y intégrant d’autres types cellulaires importants.