La recherche d’un vaccin contre le VIH occupe les scientifiques depuis de nombreuses années, et malgré certaines avancées dans le domaine, les échecs ont majoritairement jalonné le parcours des chercheurs. Une nouvelle méthode de vaccination basée sur la modification structurelle de la protéine virale Env a été testée avec succès chez la souris et pourrait représenter l’une des premières véritables avancées dans la lutte contre le VIH depuis ces 30 dernières années.
La nouvelle stratégie de vaccination, décrite dans un article publié dans la revues Science Advances, est basée sur la protéine d’enveloppe du VIH, appelée Env. Cette molécule complexe, à la forme variable, était particulièrement difficile à synthétiser dans les vaccins, de manière à induire une immunité efficace contre le VIH.
Cependant, les scientifiques du Scripps Research ont trouvé une méthode simple et élégante pour stabiliser les protéines Env dans la forme souhaitée, y compris pour diverses souches de VIH.
Montées sur des particules ressemblant à des virus, pour imiter un véritable virus, les protéines Env stabilisées ont provoqué des réponses à base d’anticorps anti-VIH robustes chez les souris et les lapins. Les vaccins candidats basés sur cette stratégie sont maintenant testés chez le singe.
« Nous considérons cette nouvelle approche comme une solution générale aux problèmes de longue date posés par la conception d’un vaccin contre le VIH » déclare Jiang Zhu, professeur associé au département de biologie structurale et informatique intégrative du Scripps Research.
Cibler la protéine de surface virale Env
Étant donné qu’Env joue un rôle crucial dans l’infection et constitue la structure virale la plus exposée au système immunitaire d’un hôte infecté, elle constitue la principale cible des efforts de vaccination anti-VIH. L’idée a été d’inoculer aux personnes la protéine Env entière ou des sous-unités de celle-ci afin de stimuler la production d’anticorps se liant à Env, dans l’espoir que ces derniers empêcheront le VIH d’infecter les cellules hôtes lors de futures expositions au virus.
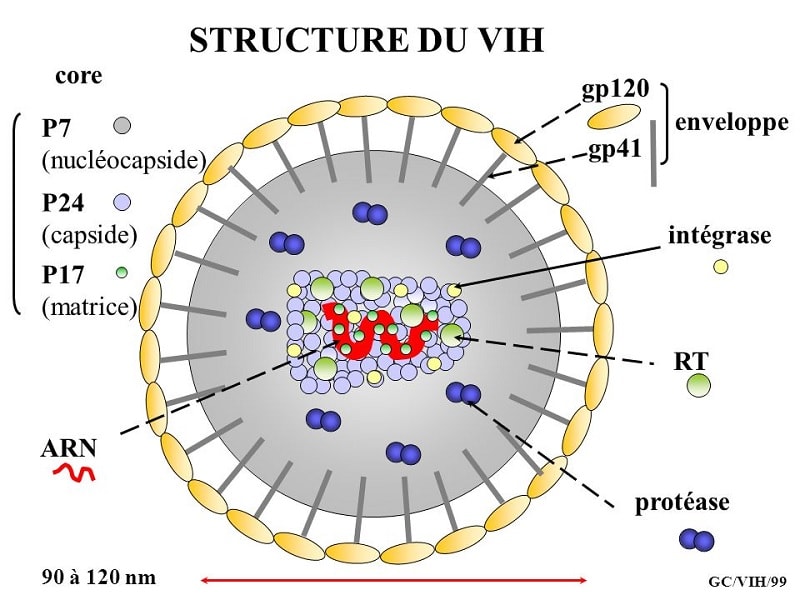
De nombreux chercheurs pensent qu’un vaccin anti-VIH peut fonctionner s’il présente les protéines Env au système immunitaire d’une manière qui ressemble beaucoup à la forme de l’Env sur un véritable virus avant qu’il n’infecte une cellule. Mais présenter correctement cette protéine a été un énorme défi.
Sur le même sujet : Premiers résultats prometteurs pour les essais cliniques humains d’un vaccin contre le VIH
Sur le VIH, Env est présente sur la membrane virale en grappes serrées de trois structures, appelées trimères, et ces structures complexes adoptent des formes radicalement différentes avant et après l’infection de cellules. Les chercheurs, malgré des années et des dizaines de millions de dollars d’expérimentation, n’ont jamais réussi à trouver une méthode efficace pour stabiliser les trimères d’Env dans la forme souhaitée avant l’infection.
« Les solutions de stabilisation du trimère qui ont été rapportées jusqu’à présent ont fonctionné pour quelques souches de VIH, mais n’ont pas pu être généralisées » explique Zhu. « La métastabilité d’Env a vraiment été un problème central pour la conception d’un vaccin anti-VIH à base de trimère ».
Une stratégie basée sur la modification structurale d’Env
Zhu, biophysicien de formation, a cherché une solution plus générale au problème de stabilité d’Env. Dans un article publié en 2016, ses collègues du Scripps Research et lui-même ont suggéré que la modification d’une section courte et linéaire d’Env, appelée HR1, pourrait faire l’affaire.
Dans la nouvelle étude, les chercheurs ont montré que cette stratégie s’avère efficace pour des trimères d’Env provenant de diverses souches de VIH circulant dans différentes régions du monde. Cette approche dite « préfusion non-clivée optimisée » (UFO), permet d’obtenir des trimères d’Env stabilisés dans la forme fermée, et pouvant être produits efficacement avec un besoin étonnamment réduit en purification, dans les types de cellules normalement utilisés dans la fabrication biotechnologique .



Zhu et ses collègues ont optimisé davantage leur stratégie de vaccination en liant génétiquement leurs trimères d’Env stabilisés, jusqu’à 60 à la fois, à des nanoparticules individuelles imitant la forme globulaire d’un virus entier. De cette manière, la molécule de vaccin, bien qu’artificielle et dépourvue du matériel génétique nécessaire à la réplication virale, apparaît au système immunitaire comme un véritable virus envahissant et stimule une réaction plus forte.
En huit semaines seulement chez la souris, Zhu et son équipe ont découvert qu’un échantillon de vaccin Env-sur-nanoparticules avait provoqué l’apparition d’anticorps qui, dans des tests de laboratoire, avaient permis de neutraliser une souche de VIH naturellement en circulation — d’un type contre lequel les vaccins candidats antérieurs avaient généralement échoué.
« C’est la première fois qu’un vaccin candidat contre le VIH induit ce type de réponse en anticorps chez la souris » indique Zhu. De même, des résultats sans précédent ont été obtenus chez le lapin, démontrant que l’approche à base de nanoparticules est nettement supérieure à l’utilisation de protéines Env isolées ; elle induit une réponse beaucoup plus forte, et ce beaucoup plus rapidement.
D’autres tests sont actuellement en cours chez 24 singes au Southwest National Primate Center, sous l’autorité des National Institutes of Health.
« Nous testons actuellement deux vaccins candidats à base de trimères d’Env de différentes souches du VIH, ainsi qu’un troisième vaccin candidat qui consiste en un cocktail de trois vaccins à base d’Env. Nous pensons que cette nouvelle approche représente une véritable avancée après 30 ans de recherche sur un vaccin anti-VIH » conclut Ji Li, directeur d’Ufovax LLC, le laboratoire biotechnologique effectuant actuellement les tests.