Selon les estimations de l’OMS, plus de 800 millions de personnes dans le monde présentent des troubles psychiques à divers degrés. Dans la plupart des cas, afin d’atténuer voire supprimer les symptômes de ces troubles, des psychotropes sont prescrits. Bien qu’ils soient généralement très efficaces, les antidépresseurs et autres molécules ont souvent de puissants effets secondaires comme l’insomnie, des étourdissements ou encore des hallucinations. Pour contourner ce problème, des chercheurs ont synthétisé une nouvelle molécule psychotrope à partir de l’ibogaïne, possédant les mêmes effets qu’un antidépresseur classique sans provoquer d’hallucinations.
Des progrès récents ont montré que les psychédéliques comme la kétamine ont un potentiel puissant pour traiter les problèmes de santé mentale tels que la dépendance, l’anxiété et la dépression. Mais les psychédéliques peuvent avoir des effets secondaires graves, comme la toxicité cardiaque et les hallucinations..
« Les psychédéliques sont parmi les médicaments les plus puissants que nous connaissons qui affectent le cerveau. C’est incroyable à quel point nous en savons peu à leur sujet », déclare le chimiste David Olson de l’Université de Californie. Ainsi, la neuroscientifique Lindsay Cameron, Olson et ses collègues de l’Université de Californie, ont décidé de regarder plus en détail et de voir s’ils pouvaient manipuler un composé psychédélique d’une manière qui leur permette de conserver ses fonctionnalités utiles, mais de supprimer les effets les plus dangereux.
Une nouvelle molécule traitant la dépendance à l’alcool et aux drogues
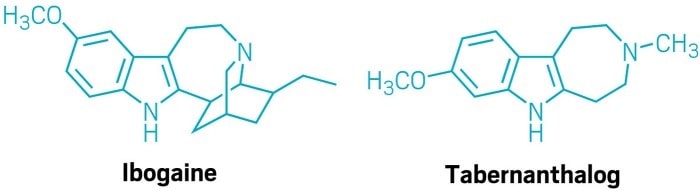
Après avoir extrait le composé psychédélique ibogaïne de l’arbuste de la forêt tropicale africaine Tabernanthe iboga, les chercheurs ont utilisé une technique de conception de médicaments appelée synthèse orientée fonction pour identifier quelle partie de la molécule d’ibogaïne induit des changements structurels dans les cellules du cerveau en culture et chez les animaux. Ils ont nommé leur molécule synthétique obtenue « tabernanthalog » (TBG).
Cameron et son équipe ont ensuite traité des souris alcooliques et des rats dépendants à l’héroïne avec du TBG. Non seulement une dose unique a permis aux souris d’arrêter de réclamer de l’alcool, mais le composé a eu un effet durable sur les rats entraînés à s’autoadministrer des doses d’héroïne, réduisant leur tendance à chercher la drogue. Même lorsqu’on leur présentait des indices qui leur rappelaient leur dépendance, les rats évitaient généralement de rechuter.
Des expériences sur le poisson-zèbre ont également montré que le TBG avait un niveau de toxicité inférieur à celui du composé ibogaïne original. Cela ne fait pas non plus trembler la tête des souris d’une manière qui indique qu’elles hallucinent, et cela semble augmenter la connectivité entre les cellules nerveuses.
Lorsque les souris ont été manipulées et forcées à nager pendant six minutes — des activités connues pour les stresser sans causer de dommages —, une dose de TBG les a aidées à se calmer à nouveau, leur procurant un effet antidépressif similaire à la kétamine. « Non seulement le TBG favorise fortement la croissance neuronale, mais il produit également des réponses comportementales de type antidépresseur et réduit la consommation d’alcool chez les souris », écrit l’équipe dans son article.
Des changements dans les circuits cérébraux
Les effets secondaires persistants des antidépresseurs comprennent l’insomnie, les étourdissements, la prise de poids et, chez certaines personnes, l’effet positif du médicament peut s’atténuer avec le temps. Contrairement à ces médicaments, on pense que les psychédéliques modifient les circuits cérébraux sous-jacents plutôt que de simplement masquer les symptômes. Une étude de 2018 a révélé qu’ils favorisaient des changements neuronaux structurels et fonctionnels dans le cortex préfrontal des rats.
« Cependant, un lien de causalité entre la croissance neuronale induite par les psychédéliques et le comportement n’a pas encore été établi chez les humains ou les rongeurs », prévient l’équipe. Un jour après que les rats ont été traités avec du TBG, on a observé que leurs cellules cérébrales développaient davantage de branches de connexion (épines dendritiques) — mais Cameron et son équipe doivent encore déterminer si ce changement de structure est lié aux changements observés dans le comportement des animaux.
Il reste encore beaucoup à faire, mais ces changements structurels peuvent être utiles pour traiter plus d’un problème. « Nous nous sommes concentrés sur le traitement d’une maladie psychiatrique à la fois, mais nous savons que ces maladies se chevauchent. Il pourrait être possible de traiter plusieurs maladies avec le même médicament », indique Olson.