On estime aujourd’hui que 5 à 8% de la population mondiale est touchée par une maladie auto-immune, pathologies dans lesquelles le système immunitaire attaque des tissus sains du corps. Actuellement, pour la plupart de ces maladies, il n’existe que des traitements pour contrôler les symptômes. Récemment, des chercheurs ont conçu une protéine pouvant activer et augmenter le nombre de cellules immunitaires régulatrices capables de prévenir l’apparition des maladies auto-immunes chez la souris. Même si l’application clinique est encore loin, cette découverte ouvre une nouvelle voie dans la recherche thérapeutique.
De manière générale, si des agents infectieux tels que des bactéries ou des virus pénètrent dans le corps, les cellules immunitaires les tuent ou les submergent, éliminant ainsi l’infection. C’est ce qu’on appelle la réponse immunitaire.
Une maladie auto-immune survient lorsque, au lieu d’attaquer des bactéries, des virus ou d’autres sources d’infection, le système immunitaire attaque des organes et des tissus sains, propres à l’organisme. Il existe plus de 80 types de maladies auto-immunes qui affectent un large éventail de parties du corps.
Certaines sont bien connues, comme le diabète de type 1, la sclérose en plaques, le lupus et la polyarthrite rhumatoïde, tandis que d’autres sont rares et difficiles à diagnostiquer. Avec des maladies auto-immunes inhabituelles, les patients peuvent souffrir des années avant d’obtenir un diagnostic approprié. La plupart de ces maladies sont incurables. Certains nécessitent un traitement à vie pour soulager les symptômes.
Selon l’Institut Pasteur, elles touchent environ 5 millions de personnes en France et constituent le troisième groupe de maladies en termes de morbidité et de mortalité dans les pays industrialisés, après les cancers et les maladies cardiovasculaires.
Les médecins ne savent pas pourquoi les maladies auto-immunes surviennent en premier lieu ou pourquoi les femmes sont plus touchées que les hommes. Cependant, des études indiquent que ces maladies résultent probablement d’interactions entre des facteurs génétiques et environnementaux.
D’un côté, les caractéristiques de genre et d’origine ethnique sont liées à une certaine probabilité de développer une maladie auto-immune. De l’autre côté, un facteur environnemental comme une infection, le stress, la prise de médicaments, l’alimentation ou encore le rayonnement ultraviolet peut également jouer un rôle dans l’apparition de ces pathologies.
C’est dans ce cadre qu’une équipe d’ingénieurs de Johns Hopkins a tenté de mettre au point, au niveau cellulaire, un moyen de prévention et un traitement contre les maladies auto-immunes basé sur les cellules régulatrices. Ils ont conçu une protéine qui active et augmente le nombre de lymphocytes T régulateurs spéciaux (appelés Tregs), qui aident à prévenir de tels troubles. Leurs résultats sont publiés dans la revue Cell Reports.
Lymphocytes T régulateurs, clé des maladies auto-immunes ?
Les cellules T régulatrices, ou Tregs, sont des globules blancs régulant le système immunitaire. Elles inhibent les composants essentiels des réponses immunitaires adaptatives et innées, comme la prolifération des lymphocytes T et la production de cytokines. Cette fonction serait modulée par l’interleukine-2 (IL-2). En effet, les Treg naturels sont caractérisés comme exprimant à la fois le co-récepteur des lymphocytes T CD4 et le CD25, qui est un composant du récepteur IL-2.
Jamie Spangler, professeur adjoint aux départements de génie chimique et biomoléculaire et de génie biomédical et membre de l’équipe de recherche, déclare dans un communiqué : « Les Tregs sont essentiels pour maintenir l’équilibre de notre système immunitaire, et lorsqu’ils sont détraqués, les gens peuvent développer des maladies auto-immunes ».
D’ailleurs, l’IL-2 a d’abord reçu l’approbation de la FDA en tant qu’agent pro-inflammatoire, avec lequel des doses élevées sont administrées pour traiter les cancers métastatiques. En revanche, de faibles doses d’IL-2 ont déjà été utilisées pour traiter certaines maladies auto-immunes telles que le diabète et la colite ulcéreuse, ainsi que le rejet de greffe. Cependant, les stratégies d’IL-2 à faible dose sont limitées par les effets dangereux de l’activation des cellules immunitaires hors cible et par la courte demi-vie sérique de l’IL-2.
Des travaux récents ont montré que des complexes comprenant l’IL-2 humaine (hIL-2) et l’anticorps anti-hIL-2 F5111 surmontent ces limitations en stimulant préférentiellement les Tregs par rapport aux autres cellules immunitaires.
Une protéine fabriquée pour contrôler le système immunitaire
C’est pourquoi les auteurs ont fabriqué une protéine à chaîne unique, appelée immunocytokine F5111 (IC), qui fusionne la cytokine interleukine-2 et l’anticorps anti-cytokine F5111. Cette molécule a été testée chez des souris conçues pour être sensibles à la colite et au diabète sucré.
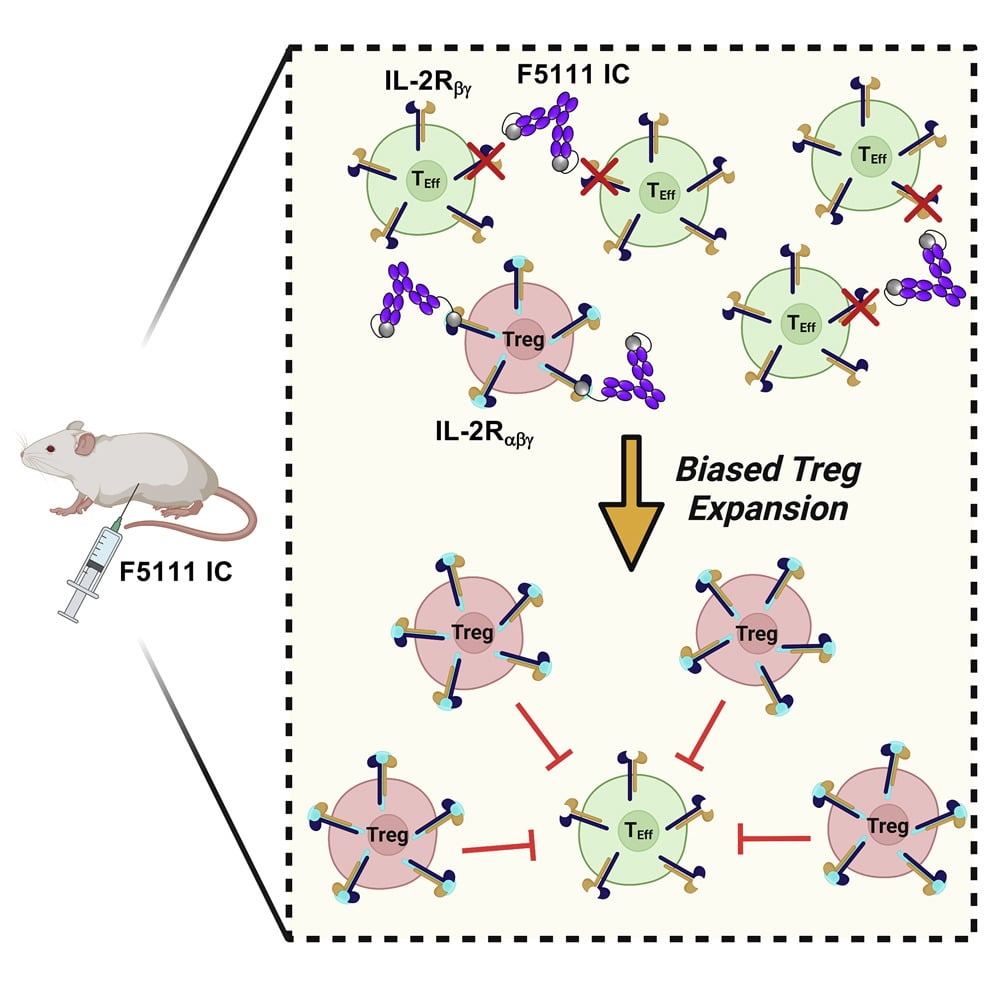


Ils ont découvert que la protéine conférait aux animaux une protection significative contre le développement des maladies auto-immunes respectives. Concrètement, F5111 IC a favorisé l’activation et l’expansion des Treg.
L’auteur principal de l’étude, Derek VanDyke, candidat au doctorat au Département de génie chimique et biomoléculaire, explique : « Dans le cas d’une maladie auto-immune, votre propre système immunitaire s’attaque essentiellement à vous-même, et ces Tregs sont utilisés pour supprimer cette attaque ».
Les auteurs déclarent que parce que les maladies auto-immunes sont le résultat d’un dysfonctionnement du système de défense de l’organisme, la suppression de cette réaction pourrait aider à empêcher la maladie de se manifester. Ils prévoient donc de démontrer la généralité de F5111 IC par des tests dans des contextes supplémentaires, tels que les modèles de rejet de greffes et le modèle expérimental d’encéphalomyélite auto-immune de la sclérose en plaques.
Étant donné que la détection et la prévention précoces ne sont pas toujours possibles, ces résultats fournissent une feuille de route pour la conception d’une immunothérapie à biais Treg qui pourrait être traduite cliniquement pour le traitement des maladies auto-immunes.