La bioimpression 3D est confrontée à des défis techniques et pratiques majeurs, tels que l’utilisation de plusieurs types de bioencres à la fois et la compatibilité mécanique et physicochimique avec le patient à transplanter. Un nouveau dispositif surmonte ces défis en appliquant in situ la bioimpression 3D, via un système portatif ultra polyvalent. Les tissus obtenus sont personnalisés et respectent parfaitement les exigences mécaniques et physicochimiques de chaque patient.
La bioimpression 3D constitue une avancée majeure dans le domaine de la médecine régénérative. Elle apporte des solutions potentielles à la pénurie de dons d’organes et aux risques associés à la transplantation. Cependant, les technologies actuelles comportent encore certaines limites. Développés en laboratoire, les tissus nécessitent par exemple un temps de traitement considérable. Des bioréacteurs sophistiqués et coûteux sont nécessaires pour leur maturation, sans compter qu’ils doivent être à nouveau manipulés lors de la transplantation.
De plus, les échantillons obtenus ne respectent généralement pas les propriétés mécaniques et physicochimiques du milieu in vivo. Certains dispositifs ne sont compatibles qu’avec des types spécifiques de bioencres, tandis que d’autres ne peuvent produire que de petites surfaces de tissus à la fois. En effet, reproduire la complexité structurelle et fonctionnelle d’un véritable tissu biologique nécessite une impression à la fois précise et polyvalente, ainsi que la manipulation de plusieurs bioencres de façon simultanée.
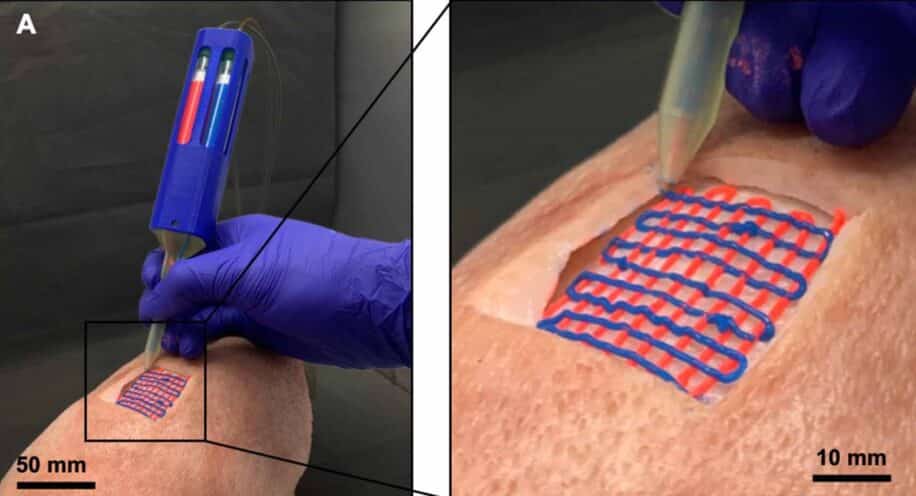
La bioimpression 3D in situ — consistant à imprimer directement les tissus et les organes au niveau du corps du patient — pourrait permettre de surmonter ces limites, selon une nouvelle étude documentée dans la revue Biofabrication. Au cours de la procédure expérimentale, le dépôt de bioencre contenant les cellules est réalisé par le biais d’un dispositif portable. Le corps du patient lui-même fait office de bioréacteur de maturation du tissu ou de l’organe. Ainsi, les échantillons implantés sont conformes aux exigences mécaniques et physicochimiques du patient, sans besoin de manipulation supplémentaire avant ou pendant la transplantation.
Un autre avantage non négligeable de cette approche est qu’elle permet un contrôle direct sur les biomatériaux, en éliminant la nécessité de concevoir préalablement des « gabarits » en 3D de l’implant. Ce qui permet de réduire considérablement les coûts d’équipement et de production.
Le nouveau dispositif portatif de l’Université de Victoria (au Canada) améliore la bioimpression in situ en utilisant plusieurs bioencres simultanément, permettant de réaliser des échantillons biocompatibles à la fois complexes et personnalisés. Cette prouesse est réalisée grâce à la capacité de l’imprimante à intégrer avec une étonnante précision les propriétés physicochimiques des tissus.
De nombreuses perspectives d’utilisation pourront être envisagées, telles que la reconstruction tissulaire à grande échelle suite à un traumatisme important, une chirurgie ou un cancer. « À long terme, cette technologie peut éliminer le besoin de donneurs d’organes, tout en réduisant les risques associés à la transplantation, permettant aux patients de vivre plus longtemps et en meilleure santé », suggère Mohsen Akbari, coconcepteur principal du nouveau dispositif et chercheur à l’Université de Victoria.
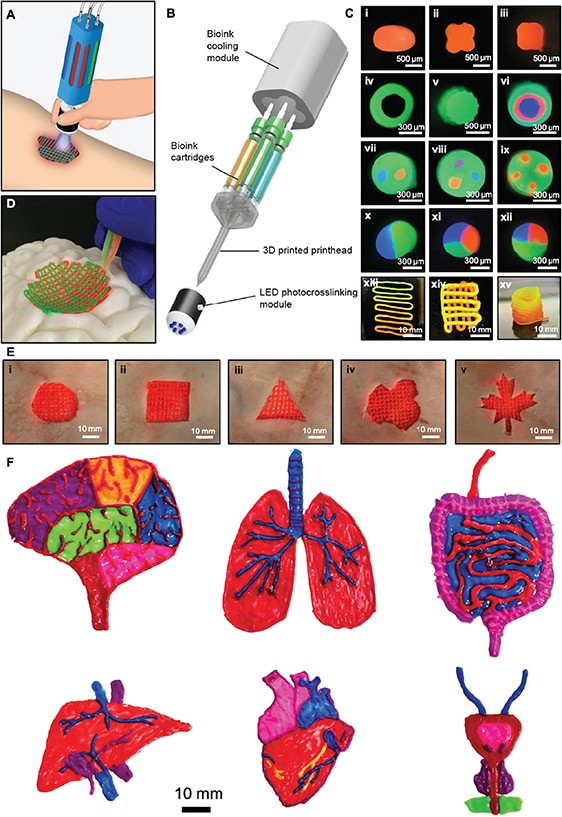
De nombreuses perspectives d’utilisation
Le nouveau dispositif est pourvu de plusieurs cartouches de bioencre, chacune contrôlée de manière complètement indépendante par un système pneumatique. Grâce à ce système, le médecin peut contrôler à volonté le mélange à imprimer, de sorte à concevoir facilement des structures complexes à multiples composants et adaptées à la forme de la zone de greffe. Des modules de refroidissement et de photodurcissement à diode électroluminescente confèrent également un contrôle supplémentaire.
Le nouveau système permettrait ainsi de concevoir de prothèses et des implants sur mesure, correspondant parfaitement à l’anatomie tissulaire d’un patient. Son système portatif confère un gain de précision, améliorant non seulement la fonctionnalité des implants et des prothèses, mais également leur esthétique ainsi que le confort du patient.
La bioimprimante pourrait également être utilisée pour l’administration localisée de médicaments, en concevant des plateformes d’administration à la demande. Les chercheurs ont en effet démontré que les bioencres peuvent transporter des « microporteurs » chargés de molécules thérapeutiques. Le dispositif conçoit ensuite des biostructures libérant la dose nécessaire, directement au niveau de la région (ou microrégion) à traiter. De cette manière, l’administration médicamenteuse gagne considérablement en précision, les molécules actives n’étant plus « filtrées » par la barrière intestinale, par exemple.
Par ailleurs, la bioimprimante pourrait produire des biocapteurs à haute précision, en incorporant aux bioencres des matériaux conducteurs ou des colorants sensibles au pH. La génération de fibres tissulaires composées de cellules spécifiques peut également être utilisée dans la conception de modèles in vitro plus élaborés, pour les essais médicamenteux. Les concepteurs ont testé le dispositif avec succès lors d’une simulation d’invasion de cellules cancéreuses dans les tissus sains adjacents. La livraison localisée de vaccins viraux ou à ARN pourrait également être envisagée.