Après avoir développé et commercialisé avec succès son vaccin anti-COVID, le laboratoirehjBioNTech ne souhaite pas s’arrêter en si bon chemin. Faisant suite à des essais cliniques de phase I menés l’année dernière, l’entreprise a débuté les essais cliniques de phase II pour un premier patient dans le cadre de son vaccin thérapeutique à ARNm contre le cancer. Le vaccin, testé sur des patients atteints de mélanomes avancés, vise à produire une réponse immunitaire efficace contre les marqueurs cancéreux.
Le premier patient a été traité lors d’un essai clinique de vaccin contre le cancer de phase II par BioNTech, évaluant la thérapie à base d’ARNm BNT111 en association avec Libtayo (cemiplimab) chez des patients atteints d’un mélanome de stade III ou IV réfractaire aux anti-PD1/en rechute non résécable. L’essai randomisé ouvert évaluera l’efficacité, la tolérance et l’innocuité du BNT111 en association avec Libtayo. Il recrutera 120 patients et évaluera les effets de la combinaison, ainsi que des agents individuels autonomes.
Un vaccin à ARNm ciblant les antigènes tumoraux
Le BNT111 est le produit candidat principal de la plate-forme FixVac de BioNTech et cible une combinaison fixe d’antigènes associés aux tumeurs codés par l’ARNm, dans le but d’activer une réponse immunitaire forte et précise contre le cancer. Le candidat est détenu à 100% par BioNTech tandis que Libtayo, un anticorps monoclonal anti-PD-1, est co-développé par Regeneron et Sanofi.
« BNT111 est un candidat vaccin intraveineux thérapeutique contre le cancer ciblant un ensemble fixe de quatre antigènes spécifiques du cancer optimisés pour l’immunogénicité et livrés sous forme de formulation ARN-lipoplex », explique BIONTech. Selon le cabinet, plus de 90 % des mélanomes des patients expriment au moins un des quatre antigènes tumoraux codés dans BNT11 : NY-ESO-1, MAGE-A3, tyrosinase et TPTE.
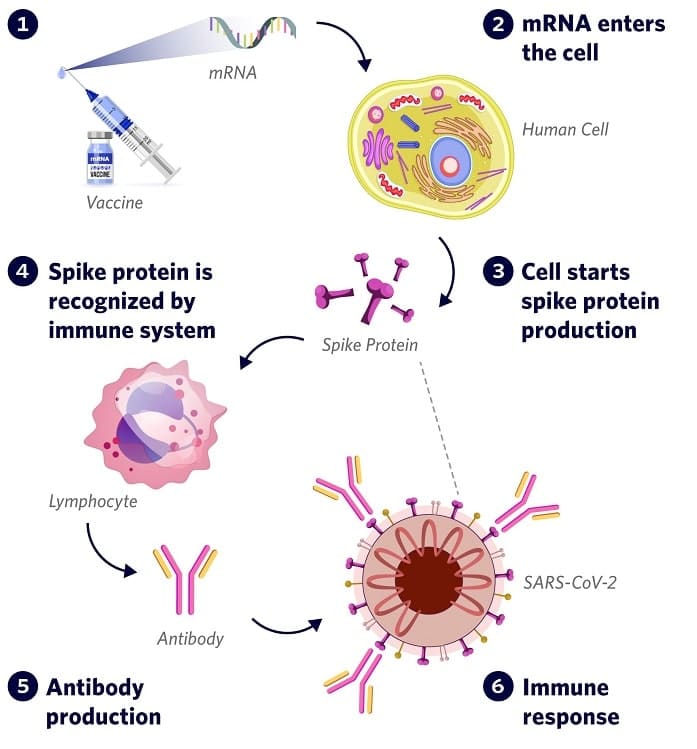
L’essai BNT111-01, qui est mené en collaboration avec Regeneron, a été examiné et approuvé par les autorités réglementaires des pays de l’UE que sont l’Espagne, l’Allemagne, l’Italie et la Pologne ainsi qu’au Royaume-Uni, aux États-Unis et en Australie. Le premier patient a été traité dans l’UE. Le critère d’évaluation principal de l’étude est d’évaluer le taux de réponse global du BNT111 en association avec Libtayo. Les critères d’évaluation secondaires incluent le taux de réponse global en monothérapie, la durée de la réponse et la sécurité.
« Notre objectif est d’exploiter la puissance du système immunitaire contre le cancer et les maladies infectieuses. Nous avons pu démontrer le potentiel des vaccins à ARNm dans la lutte contre la COVID. Nous ne devons pas oublier que le cancer est également une menace pour la santé mondiale, encore pire que la pandémie actuelle », explique le cofondateur et directeur marketing de BioNTech, Özlem Türeci.
La suite d’essais cliniques précédemment concluants
« Le BNT111 a déjà montré un profil d’innocuité favorable et des résultats préliminaires encourageants lors d’une évaluation clinique précoce. Avec le début du traitement des patients dans notre essai de phase II, nous sommes encouragés à poursuivre notre chemin initial pour réaliser le potentiel des vaccins à ARNm pour les patients atteints de cancer ».
Cet essai de phase II est basé sur les résultats antérieurs de l’essai de dose Lipo-MERIT de phase I qui ont confirmé un profil d’innocuité favorable chez 89 patients atteints de mélanome avancé. De plus, l’analyse d’efficacité de l’étude Lipo-MERIT dans un sous-ensemble de 42 patients atteints de mélanome métastatique traités plus tôt avec un inhibiteur de point de contrôle a démontré que le BNT111 induisait des réponses durables, à la fois en monothérapie et en association avec des anticorps anti-PD-1.
Des réponses objectives durables par le BNT111 étaient associées à l’activation et à une forte expansion des cellules T CD4+ et CD8+ spécifiques de l’antigène tumoral. Ces résultats ont été publiés dans la revue Nature en juillet 2020. BioNTech prévoit également de commencer des essais randomisés de phase II avec des vaccins à ARNm dans deux programmes supplémentaires en 2021.
« Dans le cadre de sa stratégie de développement, BioNTech vise à faire progresser rapidement son vaste pipeline d’oncologie et prévoit d’amener des candidats supplémentaires à un stade avancé de développement clinique et à entrer sur le marché au cours des cinq prochaines années », conclut l’entreprise.