Des chercheurs ont identifié un gène dont la désactivation favorise la prolifération rapide des cellules du cancer du pancréas. Cette désactivation serait notamment responsable de l’agressivité de cette forme de cancer, un phénomène qui a longtemps déconcerté les médecins. Cette découverte fournit ainsi de précieuses informations qui pourraient potentiellement découler sur des traitements plus efficaces.
Le cancer du pancréas est l’une des formes de cancer les plus mortelles. Plus de la moitié des patients décèdent dans les trois mois suivant le diagnostic, impliquant un taux de survie à 5 ans de seulement 10 %. Aux États-Unis par exemple, l’adénocarcinome canalaire pancréatique (PDAC) — le type de cancer du pancréas le plus courant — est la deuxième cause de décès par cancer.
Ce faible taux de survie est à la fois lié aux retards de diagnostic et au manque de stratégies thérapeutiques efficaces, surtout pour les formes résistantes à la chimio- et radiothérapie. 80 % des cas de cancer du pancréas ne sont détectés qu’au stade avancé, lorsque les tumeurs ne sont plus opérables et que les options thérapeutiques sont limitées. Au moment du diagnostic, les patients présentent généralement soit un PDAC localement avancé, soit métastatique.
D’un autre côté, le cancer du pancréas est particulièrement agressif et évolue très rapidement en comparaison à d’autres cancers, ce qui explique aussi en partie le taux de survie extrêmement bas. En conséquence, « nous avons désespérément besoin d’options de traitement plus douces et plus efficaces pour le cancer du pancréas », explique dans un communiqué de l’Université de Nottingham Trent, Chris Macdonald, directeur de recherche du Pancreatic Cancer UK.
Il a été suggéré que l’agressivité du cancer du pancréas est due à des altérations génétiques progressives se manifestant dès le début de la formation de la tumeur. Cela induit une cascade d’événements, dont l’activation d’un gène oncogène KRAS et le raccourcissement des télomères. Cependant, les mécanismes exacts sous-tendant cette agressivité demeurent en grande partie incompris.
Or, « améliorer notre compréhension fondamentale des causes de la croissance et de la propagation si rapides du cancer du pancréas est essentiel si nous voulons faire des avancées indispensables », estime Maria Hatziapostolou, du Centre de recherche sur le cancer John van Geest de l’Université de Nottingham Trent, auteure principale de la nouvelle étude.
Désactivation d’un gène suppresseur de tumeur
Afin de comprendre la manière dont les cellules tumorales pancréatiques se multiplient rapidement, Hatziapostolou et ses collègues se sont concentrés sur le facteur nucléaire hépatocytaire 4A (HNF4A), une molécule appartenant à la superfamille des récepteurs nucléaires. Ce récepteur est fortement exprimé au niveau du tissu pancréatique, du foie et du tractus gastro-intestinal et régule la transcription d’une grande variété de gènes impliqués dans de nombreux processus biologiques.
Des études ont précédemment montré que la perturbation ou la perte de l’activité du gène HNF4A est associée à différentes pathologies, y compris le cancer, le diabète et les maladies inflammatoires chroniques de l’intestin. Les chercheurs de la nouvelle étude — publiée dans la revue Gastro Hep Advances — ont alors supposé qu’il pourrait être impliqué dans le processus de formation des tumeurs pancréatiques.
Afin de tester leur hypothèse, les experts ont analysé 11 échantillons de tissus sains et 20 de tissus provenant de patients souffrant d’un cancer du pancréas. Ils ont examiné le niveau de méthylation de l’ADN en supposant que HNF4A pourrait être une cible d’hyperméthylation. La méthylation de l’ADN est un processus désactivant les gènes de manière stable et potentiellement réversible. Pour effectuer leur analyse, les chercheurs ont utilisé une technique de séquençage ciblé au bisulfite (qui consiste à utiliser un traitement de l’ADN au bisulfite de sodium avant d’effectuer le séquençage) et des tests de méthylation in vitro.
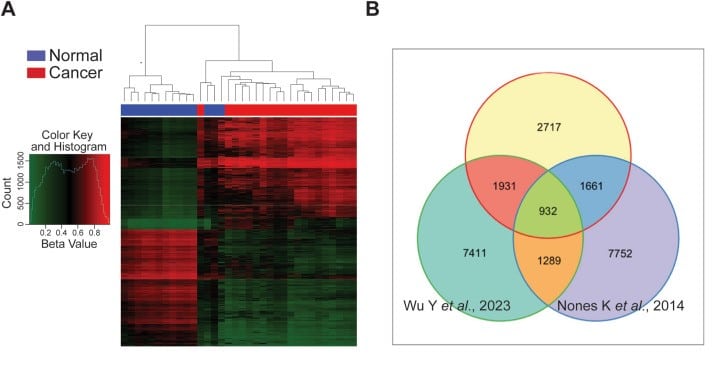


Il a été constaté que le gène HNF4A joue effectivement un rôle suppresseur de tumeur et que sa désactivation favorise l’agressivité du cancer. « Nous avons non seulement découvert le rôle suppresseur de tumeur du gène HNF4A, mais aussi la façon dont il est désactivé dès le stade très précoce de la maladie », explique Hatziapostolou.
En effet, la présence de cellules tumorales induit la méthylation de l’ADN, provoquant ainsi la désactivation de HNF4, ce qui leur permet une prolifération extrêmement rapide. D’autre part, en analysant les données de suivi des patients, les chercheurs ont constaté qu’une faible expression du gène HNF4A était associée à un faible taux de survie.
« La perte de HNF4A est un événement précoce dans le cancer du pancréas et est corrélée à une faible survie des patients », indiquent les chercheurs dans leur document. Ces résultats pourraient ainsi constituer une piste prometteuse pour une intervention thérapeutique aux stades précoces de la maladie. En outre, la facilité de modulation de HNF4A par le biais des ligands à faible masse moléculaire, en fait potentiellement une cible médicamenteuse prometteuse.