L’eau est une substance étudiée depuis des siècles par les scientifiques. Bien qu’elle soit un élément ubiquitaire sur Terre, elle est également l’un des plus complexes et surprenants qui puissent exister. Loin d’avoir livré tous ses secrets, elle révèle continuellement de nouvelles surprises aux chimistes. Récemment, des chercheurs ont découvert par sérendipité que dans des conditions bien particulières, l’eau pouvait produire spontanément du peroxyde d’hydrogène.
Des chimistes américains ont découvert que, lorsque certaines conditions sont réunies, l’eau peut produire spontanément du peroxyde d’hydrogène. « L’eau est l’un des matériaux les plus courants. Elle a été étudiée pendant des années et l’on pourrait penser qu’il n’y avait plus rien à apprendre sur cette molécule. Mais voilà qu’elle nous révèle une nouvelle surprise » déclare le chimiste Richard Zare de l’Université de Stanford.
Microgouttelettes d’eau et peroxyde d’hydrogène
Selon l’équipe, la production spontanée de peroxyde d’hydrogène peut se produire lorsque l’eau est atomisée en microgouttelettes : des gouttelettes d’eau microscopiques mesurant seulement 1 à 20 micromètres de diamètre. À une telle échelle infinitésimale, la formation spontanée de peroxyde d’hydrogène semble avoir lieu — même en l’absence de presque tout autre chose que de l’eau. L’étude a été publiée dans la revue PNAS.
« Ce processus ne nécessite aucun réactif chimique, catalyseur, potentiel électrique appliqué ou rayonnement. Seule de l’eau pure sous forme de microgouttelettes dans l’air est nécessaire à l’apparition du peroxyde d’hydrogène » écrivent les chercheurs. En l’occurrence, l’équipe a découvert ce résultat surprenant par hasard lors de recherches antérieures, en étudiant les moyens de créer des nanoparticules d’or et des nanofils à l’aide de gouttelettes d’eau.
Ces expériences ont révélé que les micro-gouttelettes d’eau accélèrent non seulement la synthèse des nanostructures d’or, mais également leur formation spontanée. Dans cette nouvelle recherche, l’équipe de Zare a effectué un certain nombre de tests, notamment la pulvérisation de micro-gouttelettes d’eau pure sur une bandelette qui deviendrait bleue en présence de peroxyde d’hydrogène.
Sur le même sujet : L’eau est en réalité présente sous deux types de molécules agissant différemment
Un moyen écologique et peu coûteux de production de peroxyde d’hydrogène
Une autre expérience a révélé que le rendement de production de peroxyde d’hydrogène était inversement proportionnel à la taille des microgouttelettes ; en d’autres termes, les microgouttelettes plus petites produisent des concentrations plus élevées de la molécule. Les chercheurs ont émis l’hypothèse que l’oxydation spontanée de l’eau se produit probablement à cause d’un fort champ électrique intrinsèque à l’interface eau-air des microgouttelettes, où un champ électrique génère des radicaux hydroxyles qui se recombinent en peroxyde d’hydrogène.
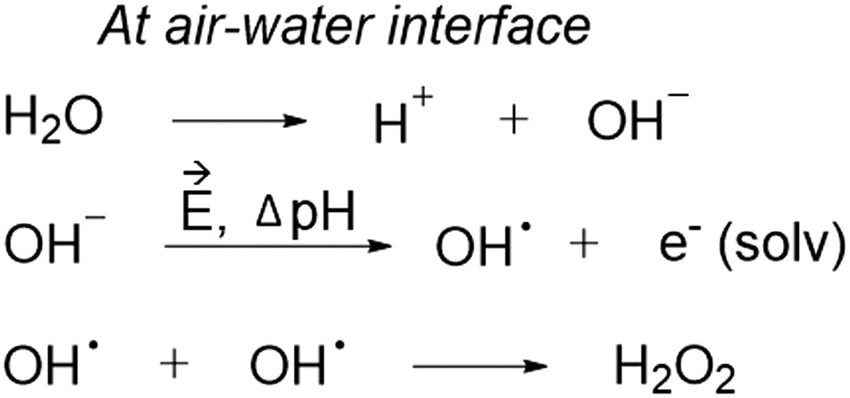
L’équipe estime que la production de peroxyde d’hydrogène elle-même n’est pas ambiguë et qu’elle pourrait déboucher sur de nouvelles méthodes de fabrication plus respectueuses de l’environnement de ce produit chimique courant.
« Nous pensons que cette découverte ouvre diverses possibilités d’innovation, notamment la production verte et peu coûteuse de peroxyde d’hydrogène, la synthèse de produits chimiques verts, le nettoyage sans danger et la transformation des aliments » écrivent les auteurs. Pour Zare lui-même, la découverte est aussi importante que surprenante. « Je pense que cela pourrait être l’une des choses les plus importantes que j’ai jamais faites » conclut-il.
Dans cette vidéo, les chercheurs expliquent le protocole expérimental utilisé et les résultats obtenus :

