Des chercheurs ont réussi à développer in vitro des embryons humains jusqu’au 14e jour de maturation à partir de cellules souches pluripotentes — c’est-à-dire sans fécondation. En effet, pour des raisons initialement techniques et dernièrement plutôt éthiques, les premiers stades de notre développement embryonnaire ont jusqu’ici été peu explorés. La méthode présentée dans le cadre de cette nouvelle étude a pour objectif de fournir une alternative plus éthique de décrypter les mécanismes précoces régissant cette étape.
Le premier mois de grossesse est une étape extrêmement délicate et déterminante pour le développement fœtal. Au cours de cette dernière, l’amas de cellules implanté dans l’utérus devient en 3 à 4 semaines un embryon bien structuré, présentant déjà les prémices de tous les organes du corps. Il s’agit d’une étape organisationnelle essentielle, dont la perturbation peut entraîner des effets dramatiques sur le fœtus. La plupart des malformations congénitales sont amorcées au cours de ce stade. De nombreuses fausses couches surviennent également au cours de ces premières semaines, souvent même avant que la femme ne se rende compte qu’elle est enceinte.
Cependant, notre compréhension du stade embryonnaire précoce est limitée, à la fois pour des raisons techniques et éthiques. La majorité de nos connaissances de cette étape se base en grande partie sur des descriptions histologiques et anatomiques, les modèles pour l’étude de la dynamique du phénomène faisant défaut. Malgré les avancées en matière de culture embryonnaire in vitro, les échantillons obtenus ne sont pas représentatifs du développement normal pouvant aller au-delà du stade précoce.
Dans une nouvelle étude décrite dans la revue Nature, une nouvelle technique, qui se veut plus éthique que les précédentes, permet de décrypter les mécanismes profonds du stade embryonnaire précoce. Il est important de savoir que les lois en vigueur interdisent la culture in vitro d’embryons humains au-delà du 14e jour de maturation. Comme la présente recherche concerne des structures dérivées de cellules souches, elle n’est pas exactement concernée par ces réglementations, sans compter l’absence de fécondation et de transfert in vivo. Dans ce contexte, les embryons obtenus pourraient être utilisés pour explorer des signaux biochimiques potentiellement inédits garantissant le bon développement fœtal ainsi que ceux susceptibles de l’entraver.
Des modèles d’embryon à 14 jours de maturation
Des études ont antérieurement démontré que les cellules souches pluripotentes humaines (PSC) peuvent être développées en modèles embryonnaires tridimensionnels. Cependant, les structures résultantes manquaient de précision et ne présentaient pas les caractéristiques post-implantatoires, essentielles à la progression du développement fœtal (telles que les cellules formant le placenta et le sac chorial).
La nouvelle technique se base sur une expérience précédente concernant la culture in vitro d’embryons de souris, à partir de cellules souches. Pour transposer le protocole aux embryons humains, des PSC ont d’abord été sélectionnées pour leur capacité à se différencier en de nombreux types de cellules (à quelques exceptions près). Une partie provient de cellules cutanées adultes « rajeunies », tandis qu’une autre descend d’une lignée souche humaine, cultivée pendant plusieurs années. Dans un deuxième temps, les PSC ont été stimulées pour revenir à un état dit « naïf », dans lequel la capacité de différenciation n’a pas de limites. C’est-à-dire que ces cellules peuvent se convertir en n’importe quel type de cellules, sans exception.
Ensuite, les cellules souches naïves obtenues ont été divisées en 3 groupes. Celles destinées à former un embryon ont été laissées telles quelles. Les deux autres groupes ont été traités avec des molécules activant certains gènes spécifiques, afin de pouvoir former les structures nécessaires au maintien de l’embryon : le placenta, le sac vitellin (membrane extraembryonnaire du mésoderme) et le sac chorial.
Après traitement, les cellules ont été mélangées dans des conditions optimisées pour leur développement. « Il est essentiel de mélanger dès le début les bons types de cellules, qui ne peuvent être dérivées que de cellules souches naïves ne présentant aucune restriction de développement », mentionne dans un communiqué le coauteur de l’étude Jacob Hanna, de l’Institut scientifique de Weizmann, en Israël. Pour la suite du processus, elles se sont autoassemblées et se sont organisées de sorte à former une structure précise et viable. « Un embryon est autonome, nous n’avons pas besoin de lui dire quoi faire. Nous devons simplement libérer son potentiel encodé en interne », explique-t-il.
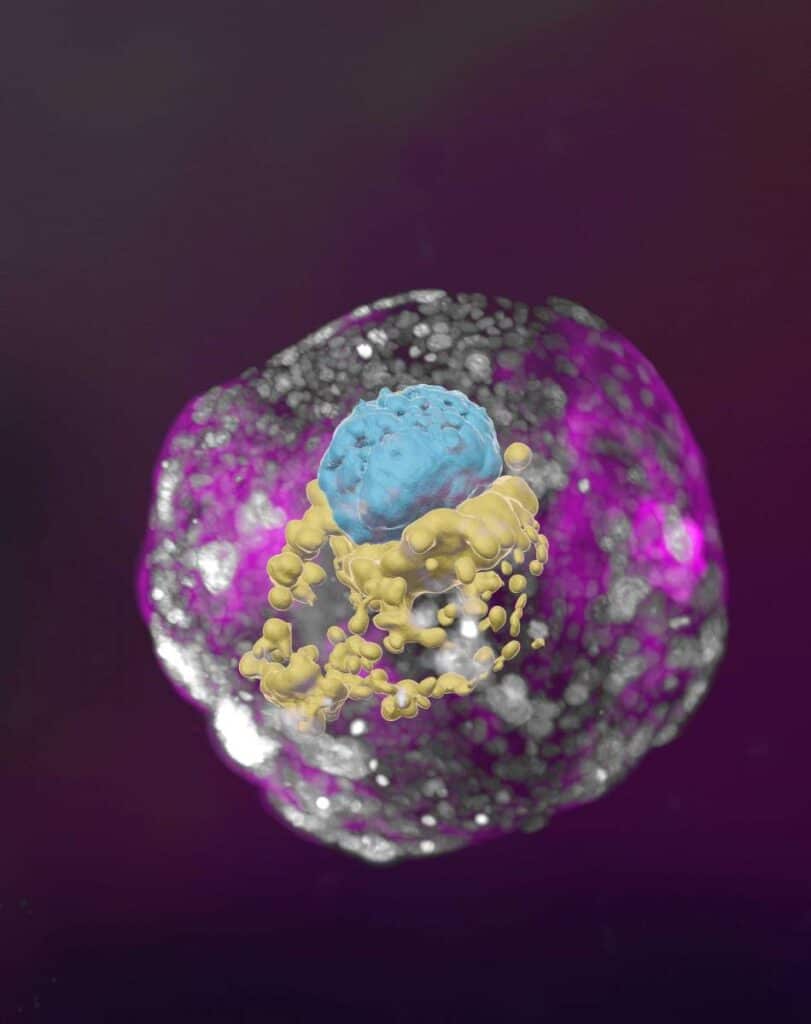
Les cellules se sont regroupées en formant des amas, dont environ 1% se sont autoorganisées en structures comparables à des embryons. Au bout de 8 jours de développement, ces derniers ont atteint un stade de maturité équivalent au 14e jour de l’embryon naturel. En comparant leurs structures artificielles avec les modèles histologiques classiques, les chercheurs ont constaté qu’elles présentaient de fortes ressemblances avec celles naturelles. Les cellules sécrétant l’hormone détectée par les tests de grossesse étaient également présentes. Appliquées sur un test de grossesse standard disponible en pharmacie, les sécrétions de ces cellules ont marqué un signal positif. Ces résultats suggèrent que les embryons présentaient la dynamique nécessaire pour passer au stade de développement suivant.
Une copie loin d’être parfaite…
Toutefois, des chercheurs externes à l’étude ont précisé que ces structures ne devaient pas encore être considérées comme étant de véritables embryons humains. Non seulement le taux de réussite de leur génération est très faible, mais le rapport indique également qu’elles « ressemblaient fortement » aux embryons naturels. Ce qui signifie qu’elles ne sont pas complètement identiques à ces derniers.
Néanmoins, la technique des chercheurs israéliens ouvre la voie à de nombreuses avancées dans le domaine, telles que la compréhension de certains mécanismes liés aux malformations congénitales et aux problèmes d’infertilité. En outre, un précieux indice a été mis en lumière pour potentiellement expliquer les fausses couches précoces : les chercheurs ont découvert que si au 3e jour (correspondant au 10e jour du développement embryonnaire naturel) l’embryon n’est pas correctement enveloppé par les cellules formant le placenta, les autres structures telles que le sac vitellin ne se développent pas correctement et peuvent conduire à un échec de la grossesse.

