Des UV à la nourriture que nous absorbons, en passant par les produits que nous utilisons, notre ADN subit des dommages en permanence. Des mécanismes de réparation travaillent constamment à la restauration des portions d’ADN lésées, car un ADN endommagé signifie un vieillissement cellulaire ou une perte de fonctions physiologiques, comme dans certaines maladies génétiques rares. Récemment, des chercheurs ont découvert un mécanisme de réparation génomique extrêmement efficace, permettant à la cellule de réactiver ses gènes précédemment endommagés et de produire de nouveau les protéines nécessaires à son fonctionnement.
Une équipe de recherche de Cologne a découvert qu’une modification de la structure de l’ADN — plus précisément de la chromatine — joue un rôle décisif dans la phase de récupération après une lésion de l’ADN. La clé est une double fixation de deux groupes méthyle sur l’histone H3 de la protéine d’empaquetage de l’ADN (H3K4me2).
Le changement spécifique permet de réactiver des gènes et de produire des protéines après des dommages : les cellules retrouvent leur équilibre et l’organisme se rétablit. Le rôle protecteur de H3K4me2 a été identifié dans des expériences avec le nématode Caenorhabditis elegans. L’étude a été publiée dans la revue Nature Structural & Molecular Biology.
L’importance des mécanismes de réparation de l’ADN
Le génome de chaque cellule humaine est endommagé quotidiennement, par exemple dans la peau par les rayons UV du Soleil. Les dommages à l’ADN provoquent des maladies telles que le cancer, influencent le développement et accélèrent le vieillissement. Les dysfonctionnements congénitaux dans la réparation de l’ADN peuvent conduire à un vieillissement extrêmement accéléré dans les maladies héréditaires rares.
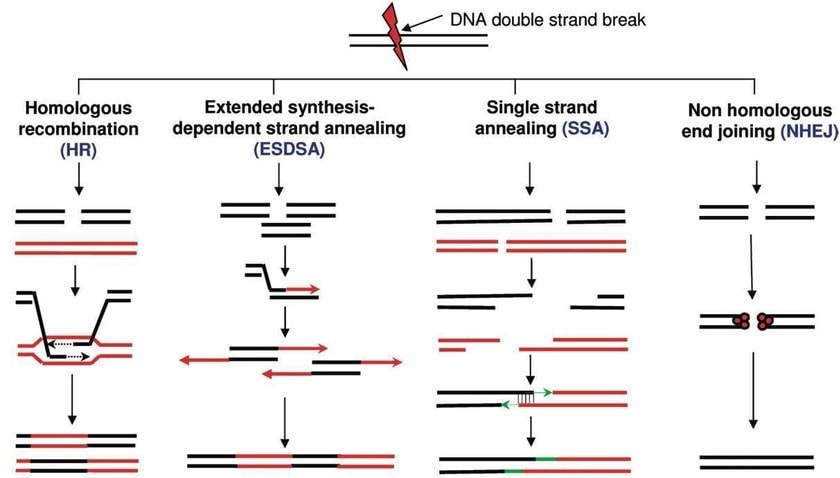
Par conséquent, les processus de préservation et de reconstruction sont particulièrement importants pour assurer le développement et maintenir la fonction tissulaire. L’ADN, qui est enroulé autour de protéines particulières — les histones — est régulé par des groupes méthyle. Diverses protéines sont chargées de placer des groupes méthyle sur les histones ou de les éliminer. Le nombre de groupes sur les histones affecte l’activité des gènes et donc la production de protéines par la cellule.
Groupes méthyle et histones : les acteurs clés de la réparation de l’ADN
Dans des expériences avec le nématode, l’équipe de recherche a montré qu’après la réparation de l’ADN endommagé, deux groupes méthyle étaient de plus en plus présents sur les paquets d’ADN. En outre, ils ont constaté que des erreurs de placement de ces deux groupes méthyle sur les histones (H3K4me2) accéléraient le processus de vieillissement induit par les dommages, tandis qu’une position précise de cette altération d’histone prolonge la durée de vie après des dommages à l’ADN.
En contrôlant les protéines qui fixent ou éliminent ces groupes méthyle, la résistance aux dommages à l’ADN — et donc le processus de vieillissement des animaux — pourrait être influencée. Une analyse plus approfondie du rôle de ces deux groupes méthyle a montré que la fixation sur H3K4 après des dommages au génome de deux groupes méthyle aide les cellules à rétablir l’équilibre après des dommages génomiques.
« Maintenant que nous connaissons les changements exacts de la chromatine, nous pouvons l’utiliser pour limiter précisément les conséquences des dommages à l’ADN. Nous espérons que ces découvertes nous permettront de développer des thérapies pour les maladies héréditaires caractérisées par des troubles du développement et un vieillissement prématuré. En raison de l’importance fondamentale des dommages à l’ADN dans le processus de vieillissement, de telles approches pourraient également contrebalancer le vieillissement normal et prévenir les maladies liées à l’âge », concluent les chercheurs.


 L’acide désoxyribonucléique, communément appelé ADN, est une molécule complexe qui joue un rôle essentiel dans la biologie des organismes vivants. Il contient les instructions génétiques utilisées dans [...]
L’acide désoxyribonucléique, communément appelé ADN, est une molécule complexe qui joue un rôle essentiel dans la biologie des organismes vivants. Il contient les instructions génétiques utilisées dans [...]