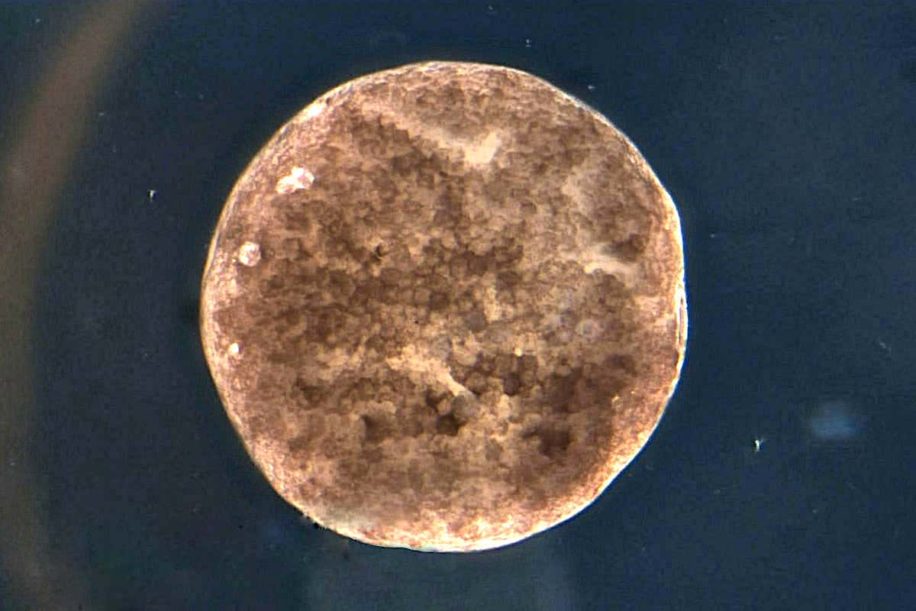
L’an passé, des chercheurs avaient mis au point de minuscules robots sphériques conçus à partir de cellules de grenouille, baptisés xénobots — du nom de l’espèce d’amphibien Xenopus laevis, d’où proviennent les cellules. Ils proposent aujourd’hui une nouvelle version de leur modèle, capable de se déplacer beaucoup plus rapidement que son prédécesseur. Mais cette nouvelle génération de robots présente d’autres améliorations.
Pour créer ces xénobots sphériques, Michael Levin et ses collègues de l’Université Tufts, dans le Massachusetts, ont extrait des tissus d’embryons de grenouilles âgés de 24 heures. Après une légère manipulation, ces derniers ont adopté une structure sphéroïde, puis ont commencé à se déplacer. Le modèle précédent se déplaçait via la contraction des cellules du muscle cardiaque ; ces nouveaux xénobots sont autopropulsés via des cils disséminés à leur surface. Ils s‘avèrent ainsi bien plus rapides.
L’équipe a par ailleurs remarqué qu’ils avaient une durée de vie plus longue : entre trois et sept jours de plus que leurs prédécesseurs, qui vivaient environ sept jours tout au plus. Enfin, ces xénobots sont également capables de réagir à certaines conditions environnementales : ils changent de couleur lorsqu’ils sont exposés à la lumière bleue.
Une plasticité fonctionnelle exceptionnelle
Les xénobots, qui mesurent entre 0,25 et 0,5 millimètre, sont conçus pour fonctionner en essaims. En d’autres termes, cela signifie que plusieurs xénobots peuvent travailler ensemble pour accomplir une même tâche — telle que transporter et connecter des neurones pour former un nouveau réseau neuronal par exemple — ce que l’on appelle l’auto-organisation cellulaire. L’avantage d’un essaim est que si l’un des individus dysfonctionne, les autres peuvent continuer à accomplir leur travail.
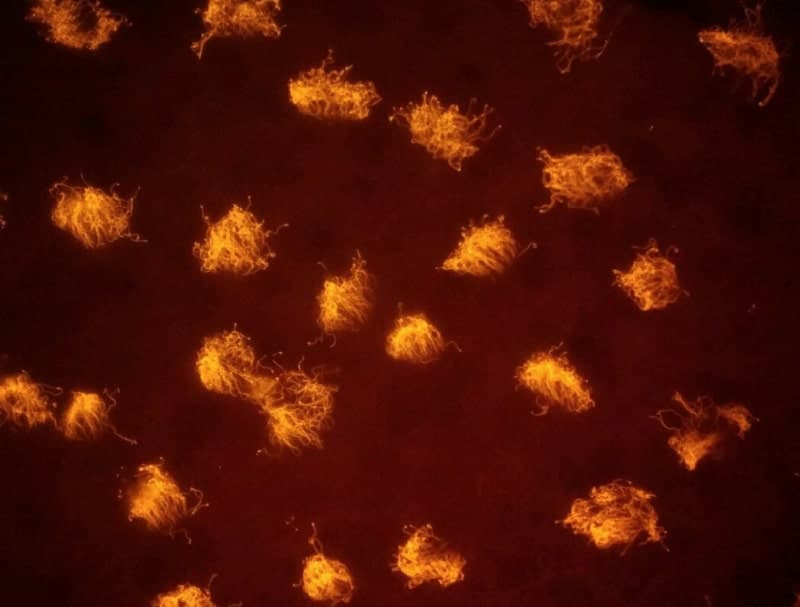
À ce jour, les essaims de robots sont généralement construits à partir de matériaux artificiels. Certaines constructions biologiques mobiles ont été créées à partir de cellules musculaires cultivées sur des échafaudages de forme précise. Cependant, l’exploitation de la plasticité fonctionnelle en une machine vivante autodirigée est restée un défi majeur. Mais l’équipe de Levin est parvenue à créer des robots biologiques in vitro, à partir de cellules de peau de grenouille, capables de se déplacer de manière coordonnée via des cils présents à leur surface.
Ces cils proviennent de la structuration des tissus normaux et ne nécessitent pas de méthodes de construction complexes ou d’édition génomique, ce qui rend la production propice à des projets à haut débit. De plus, parce qu’ils sont créés à partir de cellules, les xénobots finissent par se séparer et sont totalement biodégradables, explique Douglas Blackiston, membre de l’équipe qui a conçu ces microrobots. L’objectif est qu’ils puissent un jour être utilisés en toute sécurité dans le corps humain et/ou pour lutter contre la pollution de l’environnement.
Extraites de leur contexte naturel, les cellules de peau de grenouille se sont en quelque sorte réinventées pour se comporter différemment. « Pour moi, l’une des choses les plus excitantes ici est la plasticité. Cette idée que même les cellules normales, non génétiquement modifiées, avec un génome de grenouille normal, sont en fait capables de construire quelque chose de complètement différent », souligne Levin.
Une machinerie biologique inclassifiable
Au cours de leurs expérimentations, les chercheurs ont constaté que les xénobots étaient capables de naviguer dans des environnements aqueux de diverses manières et de guérir après des dommages « corporels ». En outre, ils affichaient des comportements de groupe émergents. L’équipe a ainsi construit un modèle de calcul pour prédire les comportements collectifs utiles pouvant être obtenus à partir d’un tel essaim de xénobots.
Par ailleurs, ces microrobots se sont avérés sensibles aux changements dans leur environnement. En effet, en utilisant une protéine photoconvertible, qui devient rouge lorsqu’elle est exposée à la lumière bleue, les chercheurs ont mis en évidence l’existence d’une mémoire moléculaire inscriptible : celle-ci permet aux xénobots d’enregistrer l’exposition à une longueur d’onde spécifique. Observez les capacités de ces minuscules robots dans cette vidéo publiée par l’Université Tufts :
Finalement, l’ensemble de ces résultats suggèrent que ces xénobots nouvelle génération peuvent être utilisés pour étudier de nombreux aspects de l’autoassemblage, du comportement des essaims et de la bio-ingénierie synthétique. Ils pourraient également servir de machines vivantes polyvalentes à corps mou dans de nombreuses applications pratiques en biomédecine et en sciences de l’environnement.
Les tentatives précédentes de création de robots vivants, telles qu’un cafard ou un papillon contrôlés sans fil, impliquaient la manipulation d’animaux vivants, ce qui soulevait évidemment des préoccupations éthiques. Les xénobots diffèrent de ceux-ci, car ils reposent sur l’utilisation de cellules vivantes et non de l’animal dans son ensemble. « Tout se passe in vitro, ils commencent juste avec des cellules, ils n’ont pas de neurones, donc ce n’est pas un animal », confirme Auke Ijspeert de l’École polytechnique fédérale de Lausanne, qui n’était pas impliqué dans ce projet.
Dès lors, les xénobots doivent-ils être considérés comme des organismes vivants ou comme des robots traditionnels ? La classification s’avère plus délicate qu’il n’y paraît. « Je ne me sens pas plus proche d’une réponse que d’une autre. Qu’il s’agisse de robots, de grenouilles ou de tout autre chose », déclare Joshua Bongard, co-auteur de la recherche.