Après Alzheimer, la maladie de Parkinson se classe au second rang des pathologies neurodégénératives les plus fréquentes en France. À l’échelle mondiale, sa prévalence a doublé en 25 ans, affectant désormais près de 10 millions de personnes. Si cette maladie détruit les cellules cérébrales, les chercheurs soulignent également le rôle des milliards de microorganismes du tractus gastro-intestinal. Une étude récente révèle notamment une carence notable en biotine et en riboflavine chez les patients, ouvrant la voie à un traitement potentiel à la fois simple et efficace.
La maladie de Parkinson, caractérisée par des tremblements et des troubles de la coordination, affecte le système nerveux central, qui dirige à la fois les mouvements volontaires et certaines fonctions autonomes comme le rythme cardiaque et le transit intestinal. Entre 60 % et 80 % des patients souffrent de constipation, de ballonnements ou de crampes. Plusieurs études ont montré que les symptômes digestifs précédaient souvent le diagnostic, et même l’apparition de troubles moteurs tels que des mouvements lents ou involontaires.
En 2003, le Dr Heiko Braak a émis l’hypothèse qu’un pathogène inconnu peut remonter du système digestif au cerveau via le nerf vague. Cette dernière a été confirmée en 2017 par des chercheurs suédois, qui ont observé que l’ablation du nerf vague réduisait significativement le risque de développer la maladie. Depuis, les interactions entre le microbiote intestinal et le cerveau sont de plus en plus étudiées comme facteur clé dans le développement de la maladie de Parkinson et d’autres maladies neurodégénératives.
Un lien établi entre microbiote intestinal et maladie de Parkinson
Dans une récente étude, une équipe de l’Université de Nagoya, au Japon, a cherché à élucider les relations entre les micro-organismes intestinaux et la maladie de Parkinson. Hiroshi Nishiwaki, auteur principal de l’étude, et son équipe ont mené une méta-analyse sur des échantillons de selles de 167 individus, dont 74 patients atteints de la maladie provenant du Japon, d’Allemagne, de Taïwan, des États-Unis et de Chine. Les 73 autres participants formaient un groupe témoin en bonne santé.
Grâce au séquençage génétique dit shotgun, les chercheurs ont observé une réduction marquée des microorganismes impliqués dans la synthèse de deux vitamines essentielles : la biotine (vitamine B7) et la riboflavine (vitamine B2). Ces vitamines jouent un rôle central dans les processus métaboliques et possèdent également des propriétés anti-inflammatoires.
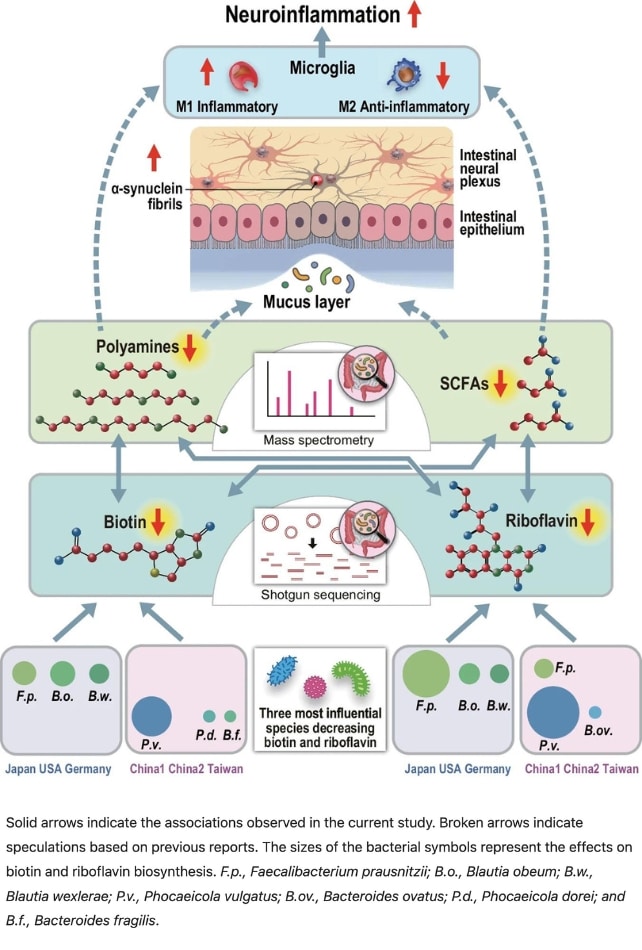
L’équipe a également mis en lumière les conséquences de ces carences sur la production d’acides gras à chaîne courte (AGCC) et de polyamines, des molécules essentielles à l’entretien de la couche de mucus qui protège l’intestin. « Des carences en polyamines et en AGCC peuvent entraîner un amincissement de cette barrière, augmentant la perméabilité intestinale, un phénomène souvent observé chez les patients atteints de la maladie de Parkinson », précise Nishiwaki. Une fois affaiblie, cette protection expose le système nerveux intestinal à des toxines, favorisant l’agrégation anormale de l’alpha-synucléine, une protéine impliquée dans l’inflammation chronique du cerveau.
Les résultats de cette méta-analyse suggèrent qu’un microbiote intestinal équilibré et des suppléments de vitamines B pourraient freiner la progression de la maladie. « Une supplémentation thérapeutique en riboflavine et biotine offre une piste prometteuse pour atténuer les symptômes et ralentir l’évolution de la maladie », conclut Hiroshi Nishiwaki.