Les maladies mitochondriales constituent un éventail de pathologies génétiques entravant la capacité des mitochondries à générer l’énergie requise pour le fonctionnement adéquat des organes. Ces maladies peuvent, dans certains cas, se révéler mortelles. Une technologie innovante de fécondation in vitro (FIV), s’appuyant sur l’utilisation de trois ADN distincts, aspire à prévenir la transmission, par une mère, de gènes défectueux à son enfant par le biais des mitochondries. Bien que cette procédure suscite de nombreux débats, le premier nourrisson issu de cette technique est venu au monde au Royaume-Uni, offrant une lueur d’espoir face à ces maladies incurables.
Les maladies mitochondriales regroupent une variété de troubles médicaux engendrés par des anomalies génétiques au sein de l’ADN mitochondrial. Ces organites cellulaires, présents dans quasiment toutes les cellules du corps, sont responsables de la production d’environ 90% de l’énergie nécessaire au fonctionnement optimal de l’organisme. Lorsque ces véritables centrales énergétiques dysfonctionnent, les conséquences peuvent sérieusement compromettre la survie du patient. On estime à environ 200 le nombre de nouveaux cas détectés chaque année en France, et un enfant sur 6500 serait touché à l’échelle mondiale.
Les manifestations des maladies mitochondriales varient considérablement en fonction des cellules affectées. Les symptômes peuvent inclure des convulsions, une fatigue chronique, une perte de la vue ou de l’ouïe, des troubles cognitifs ou encore des problèmes respiratoires. Tous les organes et systèmes corporels sont susceptibles d’être touchés, y compris le cerveau, le cœur, les poumons, les intestins, le foie et la peau.
Aujourd’hui, il n’existe aucune thérapie capable de guérir ces maladies. C’est pourquoi le don mitochondrial est envisagé comme une option innovante de fécondation in vitro, qui pourrait permettre aux familles touchées par une maladie mitochondriale d’éviter de la transmettre à leur enfant. Récemment, le premier bébé britannique conçu avec l’ADN de trois individus, grâce à cette procédure, est né en pleine santé. Cette avancée représente un espoir considérable pour toutes les personnes atteintes de maladies héréditaires et incurables.
Trois ADN pour un bébé
Le nouveau-né est issu d’un père et de deux mères génétiques, suite à l’autorisation accordée en 2017 aux chercheurs du Newcastle Fertility Center de tester cette procédure sujette à controverse. Le Royaume-Uni se distingue comme le premier pays à réguler le don de mitochondries.
Le premier nourrisson à voir le jour grâce au traitement par don mitochondrial (MDT) est né au Mexique en 2016. Sa mère était porteuse de gènes responsables du syndrome de Leigh. Cette affection neurométabolique rare touche le système nerveux central et s’avère souvent fatale.
Il est important de noter que l’ADN mitochondrial est transmis par la mère et ne représente que 0,1% de l’héritage génétique d’un enfant. En effet, au stade embryonnaire, l’essentiel du matériel génétique est concentré dans le noyau de la cellule. Cependant, chaque noyau d’un ovule fécondé est entouré de milliers de mitochondries qui possèdent leurs propres gènes.
Dans un embryon sain, le rôle principal des mitochondries est de fournir de l’énergie aux cellules qui formeront les différents organes. Ainsi, si ces dernières sont endommagées ou présentent des mutations, le fonctionnement des organes vitaux pourrait être affecté lors de la croissance de l’individu.
Pour les femmes concernées, la conception naturelle est souvent un pari risqué. Certains bébés peuvent naître en bonne santé, n’héritant que d’une infime partie des mitochondries mutées, tandis que d’autres développeront des maladies graves, progressives et souvent mortelles. Le don de mitochondries représente une option précieuse pour ces individus.
Concrètement, la procédure implique l’utilisation d’ovules provenant à la fois d’un donneur en bonne santé et d’une femme atteinte d’une maladie mitochondriale. Premièrement, le sperme du père est utilisé pour féconder les ovules de la mère et de la donneuse. Le matériel génétique nucléaire de l’ovule du donneur est ensuite retiré et remplacé par celui de l’ovule fécondé du couple.
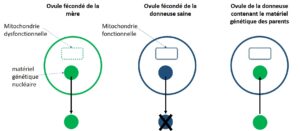
Cela signifie que tout futur enfant hérite de l’ADN nucléaire de ses deux parents (et est donc génétiquement lié à la mère et au père) tout en présentant un risque nettement réduit de maladie mitochondriale grâce à l’ADN mitochondrial sain de l’ovule donneur. Ce dernier est ensuite implanté dans l’utérus. C’est cette combinaison d’ADN de trois individus qui a conduit à l’expression « bébé de trois personnes », fréquemment employée pour décrire cette technique.
Une procédure d’avenir, ou trop risquée ?
Dans un article du Guardian, qui a été le premier à annoncer la naissance issue du MDT après avoir formulé une demande d’accès à l’information auprès de la Human Fertilisation and Embryology Authority (HFEA) du Royaume-Uni, le régulateur HFEA a révélé que le nombre de naissances était « inférieur à cinq ». Il a refusé de donner un chiffre précis, invoquant son « devoir de confidentialité envers les individus susceptibles d’être identifiés ». Aucun autre détail sur ces naissances n’a été fourni.
Les scientifiques disposent donc de preuves limitées sur les risques et les taux de réussite de cette procédure. Les bilans de santé des enfants nés de ce traitement contribueront à éclairer la compréhension de la maladie et de la procédure en question.
En effet, cette dernière ne réussit pas toujours, à cause d’un phénomène que les scientifiques nomment « la réversion ». Une équipe dirigée par Dagan Wells, biologiste de la reproduction à l’Université d’Oxford, a tenté de déterminer la sureté de la procédure. Il est possible que le petit nombre de mitochondries anormales, inévitablement transférées de l’ovule de la mère à l’ovule du donneur, puisse se multiplier et prendre le dessus sur les mitochondries saines, lorsque le bébé est dans l’utérus, avec de graves conséquences pour sa santé.
Peter Thompson, directeur général de la HFEA, conclut : « Le traitement par don mitochondrial offre aux familles atteintes d’une maladie mitochondriale héréditaire grave la possibilité d’avoir un enfant en bonne santé ». Il ajoute : « Ce sont encore les prémices du traitement par don de mitochondries, et la HFEA continue d’examiner les développements cliniques et scientifiques ».

 L’acide désoxyribonucléique, communément appelé ADN, est une molécule complexe qui joue un rôle essentiel dans la biologie des organismes vivants. Il contient les instructions génétiques utilisées dans [...]
L’acide désoxyribonucléique, communément appelé ADN, est une molécule complexe qui joue un rôle essentiel dans la biologie des organismes vivants. Il contient les instructions génétiques utilisées dans [...]