Les maladies cardiovasculaires font partie des causes de décès les plus répandues dans le monde. Une partie de ces maladies peuvent affecter les individus dès le stade fœtal lorsqu’elles sont congénitales. Pour mieux comprendre le développement des cardiopathies congénitales, et comment les traiter, les chercheurs ont besoin d’avoir accès à du matériel fœtal, flirtant parois avec les limites de l’éthique. Pour éviter ces situations floues, des chercheurs américains ont créé le premier organoïde cardiaque humain — un mini-cœur contenant toutes les fonctions primaires d’un véritable cœur et permettant d’étudier en détail le développement fœtal d’un cœur humain.
Les chercheurs de la Michigan State University ont créé pour la première fois un modèle de cœur humain miniature en laboratoire, complet avec tous les types de cellules cardiaques primaires et une structure fonctionnelle de chambres et de tissus vasculaires. Aux États-Unis, les maladies cardiaques sont la première cause de décès.
« Ces mini-cœurs constituent des modèles incroyablement puissants dans lesquels étudier toutes sortes de troubles cardiaques avec un degré de précision jamais vu auparavant », explique Aitor Aguirre, professeur de génie biomédical à l’Institut MSU pour les sciences et l’ingénierie de la santé.
Les organoïdes de cœur humain, ou hHO en abrégé, ont été créés au moyen d’un nouveau cadre de cellules souches qui imite les environnements de développement embryonnaire et fœtal.« Les organoïdes sont des constructions cellulaires 3D autoassemblées qui reprennent les propriétés et la structure des organes dans une large mesure », indique Yonatan Israeli.
Les organoïdes cardiaques : un moyen éthique peu coûteux d’étudier le développement du cœur humain
L’innovation déploie un processus de bio-ingénierie qui utilise des cellules souches pluripotentes induites, générant un mini cœur fonctionnel après quelques semaines. Les cellules souches sont obtenues d’adultes consentants et sont donc exemptes de préoccupations éthiques. Ce processus permet aux cellules souches de se développer fondamentalement comme elles le feraient dans un embryon, dans les différents types et structures cellulaires présents dans le cœur.
« Nous donnons les instructions aux cellules et elles savent ce qu’elles doivent faire lorsque toutes les conditions appropriées sont remplies », explique Aguirre. Parce que les organoïdes ont suivi le processus de développement embryonnaire cardiaque naturel, les chercheurs ont étudié, en temps réel, la croissance naturelle d’un cœur humain fœtal. Cette technologie permet la création de nombreuses hHO simultanées avec une relative facilité, contrairement aux approches d’ingénierie tissulaire existantes, qui sont coûteuses et difficilement évolutives.
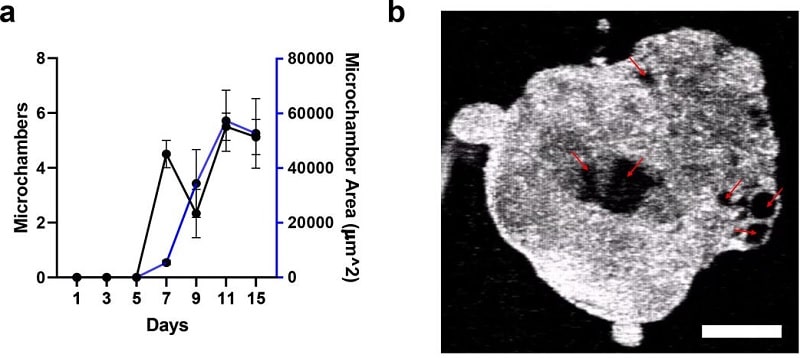
L’un des principaux problèmes auxquels est confrontée l’étude du développement cardiaque fœtal et des malformations cardiaques congénitales est l’accès à un cœur en développement. Les chercheurs se sont limités à l’utilisation de modèles de mammifères, de restes fœtaux donnés et de recherches cellulaires in vitro pour se rapprocher de la fonction et du développement réel d’un cœur.
« Maintenant, nous pouvons avoir le meilleur des deux mondes, un modèle humain précis pour étudier ces maladies, sans utiliser de matériel fœtal ni violer les principes éthiques. Cela constitue un grand pas en avant », déclare Aguirre. Et après ? Pour Aguirre, le processus est double.
Sur le même sujet : Comment les « mini-cerveaux » cultivés en laboratoire aident-ils à mieux comprendre le cerveau humain ?
Vers un perfectionnement progressif des organoïdes cardiaques et de leur étude
Premièrement, l’organoïde cardiaque représente un regard sans précédent sur les rouages du développement d’un cœur fœtal. « Dans le laboratoire, nous utilisons actuellement des organoïdes cardiaques pour modéliser les cardiopathies congénitales — la malformation congénitale la plus courante chez l’Homme, affectant près de 1% de la population de nouveau-nés. Avec nos organoïdes cardiaques, nous pouvons étudier l’origine des cardiopathies congénitales et trouver des moyens de les arrêter ».
Et deuxièmement, bien que le hHO soit complexe, il est loin d’être parfait. Pour l’équipe, l’amélioration de l’organoïde final est une autre piste clé de la recherche future. « Les organoïdes sont de petits modèles du cœur fœtal avec des caractéristiques fonctionnelles et structurelles représentatives. Cependant, ils ne sont pas encore aussi parfaits qu’un cœur humain. C’est quelque chose vers quoi nous travaillons », indique Israeli.
Ces organoïdes offrent une large gamme de possibilités d’étude et d’applications. Ils permettent une capacité sans précédent d’étudier de nombreuses autres maladies cardiovasculaires — de la cardiotoxicité induite par la chimiothérapie à l’effet du diabète, pendant la grossesse, sur le cœur du fœtus en développement.
Vidéo de la MSU montrant un organoïde cardiaque battre :