Un nouveau traitement à base de cellules souches pluripotentes induites a restauré la vision chez trois patients souffrant de troubles oculaires sévères opacifiant la cornée. L’acuité visuelle des patients a été considérablement améliorée, même un an après la transplantation. En outre, aucun rejet immunitaire n’a été observé après la procédure (durant la période de suivi de deux ans), même chez ceux qui n’avaient pas reçu de médicaments immunosuppresseurs.
La cornée est entourée d’un tissu épithélial stratifié essentiel à la vision. La couche située au niveau de l’anneau limbique (l’anneau sombre entourant l’iris) constitue un réservoir de cellules souches assurant le renouvellement continu des cellules épithéliales composant ce tissu. Le déficit en cellules souches limbiques (DCSL) provoque une opacification de la surface de la cornée par un tissu cicatriciel fibreux, ce qui peut conduire à une perte de la vision.
La DCSL est soit d’origine immunitaire, soit génétique (DCSL bilatérale), soit d’origine traumatique (DCSL unilatérale). Le traitement de la maladie consiste généralement à effectuer une ablation du tissu cicatriciel opacifiant la cornée et à transplanter un tissu épithélial sain. Le choix du matériau à transplanter dépend cependant du type de maladie. Pour la DCSL unilatérale, la procédure standard consiste en une transplantation autologue, c’est-à-dire utilisant le tissu provenant de l’œil sain du patient lui-même. En revanche, le traitement de la DCSL bilatérale consiste à transplanter des cellules souches limbiques provenant de donneurs décédés, ou des feuillets de cellules épithéliales cultivés à partir de la muqueuse buccale du patient.
Ces approches présentent de nombreux inconvénients liés principalement à l’incertitude quant au succès de la transplantation et au risque de rejet immunitaire. D’autre part, la néovascularisation après transplantation de feuillets de cellules épithéliales de la muqueuse buccale est inévitable, ce qui peut conduire à des complications post-opératoires.
L’étude ayant abouti au traitement, codirigée par l’Université d’Osaka (au Japon), propose une nouvelle approche basée sur les cellules souches pluripotentes induites (iPS), dont le potentiel n’a jusqu’à présent pas été exploré dans le cadre du traitement de la DCSL. « À notre connaissance, il s’agit de la première utilisation de cellules épithéliales cornéennes dérivées d’iPSC en chirurgie de transplantation », indiquent les chercheurs dans leur document, publié dans la revue The Lancet.
Une amélioration persistante de la vision après un an chez 3 patients sur 4
Pour effectuer les essais, les chercheurs japonais ont utilisé des iPS produites à partir de cellules sanguines provenant d’un donneur sain. Les iPS peuvent être produites à partir de n’importe quelle cellule qui, une fois reprogrammée génétiquement, peut retrouver un état embryonnaire, puis se différencier en toutes sortes de cellules. L’équipe a cultivé les iPS pour obtenir un fin feuillet de cellules épithéliales cornéennes.
Les feuillets ont été transplantés chirurgicalement chez 4 patients, dont une femme de 44 ans (patient 1) et un homme de 72 ans souffrant d’une LSCD idiopathique (patient 3), un homme de 66 ans (patient 2) atteint d’une pemphigoïde de la muqueuse oculaire (une maladie auto-immune entraînant l’apparition d’un tissu cicatriciel au niveau de la conjonctive et de la cornée) et une femme de 39 ans (patient 4) atteinte de nécrose épidermique toxique (une affection cutanée similaire à des brûlures étendues et pouvant opacifier la cornée).
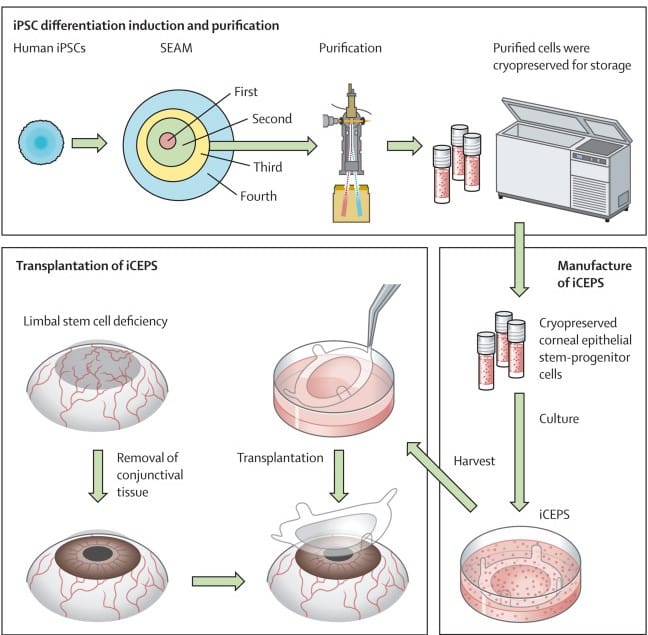
La procédure a été réalisée en grattant la couche de tissu cicatriciel de l’œil endommagé, en suturant les feuillets épithéliaux au niveau de la zone grattée, puis en plaçant une lentille protectrice souple afin d’isoler la région et de favoriser la cicatrisation. Les patients 1 et 2 ont bénéficié d’un traitement immunosuppresseur (de la cyclosporine) à faible dose, tandis que les patients 3 et 4 non. L’ensemble a été suivi sur une période de 52 semaines, avec une surveillance de sécurité supplémentaire d’un an.
Après la transplantation, l’ensemble des patients a présenté une amélioration presque immédiate de leur vision et une réduction de la zone de cornée opacifiée. À 52 semaines, ces améliorations ont persisté et l’acuité visuelle était considérablement améliorée. Toutefois, l’un des patients a montré de légères récidives après un an d’observation. « Dans l’ensemble, les résultats d’efficacité bénéfiques obtenus pour les patients 1 et 2 étaient meilleurs que ceux obtenus pour les patients 3 et 4 », indique l’équipe.
On ne sait pas exactement ce qui a induit l’amélioration de la vision, mais il est possible qu’elle soit due à la prolifération des cellules transplantées, soit à l’élimination du tissu cicatriciel lors de l’intervention chirurgicale. Les greffons peuvent aussi déclencher la migration des cellules saines des patients depuis d’autres régions de l’œil, « rajeunissant » ainsi la cornée.
Pas de rejet de greffe, même sans traitement immunosuppresseur
Par ailleurs, l’équipe a enregistré 26 événements indésirables au cours de la période de suivi de 52 semaines, mais aucun effet secondaire grave. Aucun symptôme de rejet de greffe ou tumorigène n’a été observé après deux ans, même chez les patients qui n’ont pas bénéficié d’immunosuppresseurs.
Selon Kapil Bharti, chercheur en cellules souches translationnelles au National Eye Institute des National Institutes of Health, à Bethesda, « il est important et soulageant de constater que les greffons n’ont pas été rejetés ». Cependant, davantage d’essais sont nécessaires afin de confirmer que l’intervention est sécuritaire. L’équipe prévoit d’autres essais cliniques à cet effet dès le mois de mars prochain.


