Des chercheurs sont parvenus à créer les premiers œsophages fonctionnels cultivés en laboratoire et à les implanter avec succès chez des porcs. Les implants ont notamment permis de restaurer leur capacité à avaler et à s’alimenter pendant plusieurs mois et ce, sans avoir besoin d’une immunosuppression. Ce type d’implants pourrait à terme être utilisé pour traiter les enfants souffrant de malformations de l’œsophage ou les personnes dont l’organe a été endommagé à la suite d’un cancer.
L’œsophage, le conduit reliant la bouche à l’estomac, est essentiel à la nutrition et à la croissance. Les enfants nés avec une pathologie œsophagienne telle que l’atrésie de l’œsophage (qui touche un enfant sur 3500) ont un large espace manquant entre les segments supérieurs et inférieurs de l’organe, ce qui entrave leur capacité à déglutir et donc leur alimentation. Ces enfants ne peuvent survivre sans intervention chirurgicale, mais l’espace manquant est généralement trop important pour être refermé juste après la naissance.
En attendant la chirurgie, les nourrissons souffrant de cette pathologie doivent être alimentés à l’aide d’une sonde reliée directement à leur estomac. L’approche chirurgicale standard consiste ensuite à repositionner l’estomac pour combler l’espace et le relier directement à la gorge, ou à transplanter une partie du côlon pour servir de substitut à l’œsophage.
Ces interventions sont cependant complexes et invasives et peuvent provoquer d’importantes complications à court et à long terme, telles que des problèmes gastro-intestinaux et un risque de cancer. La transplantation via des dons d’organes n’est pas non plus envisageable en raison de la complexité de l’organe et du manque de greffons de taille adaptée.
« L’œsophage est un organe très complexe, dépourvu de vascularisation propre ; il ne peut donc pas être transplanté au sens classique du terme », explique dans un communiqué, Paolo De Coppi, titulaire de la chaire NIHR et Nuffield de chirurgie pédiatrique à l’Institut de santé infantile University College of London-Great Ormond Street (UCL GOS ICH) et chirurgien pédiatrique consultant au Great Ormond Street Hospital (GOSH).
Des matrices tissulaires de porcs servant d’échafaudage pour les cellules des receveurs
L’ingénierie tissulaire est explorée depuis des décennies pour la régénération des organes ou des tissus difficiles à restaurer comme la trachée et l’œsophage. L’équipe de De Coppi propose une approche consistant à cultiver des œsophages artificiels créés à partir des propres tissus des receveurs chez des modèles animaux.
« Pour développer des alternatives, il est essentiel de travailler avec des modèles animaux qui reproduisent fidèlement l’anatomie et le fonctionnement humains. À cet égard, l’œsophage du porc ressemble beaucoup à celui de l’homme. Grâce au succès de cette recherche, nous espérons pouvoir proposer d’ici cinq ans une alternative tissulaire bio-ingénierée aux enfants qui en ont désespérément besoin », indique l’expert.
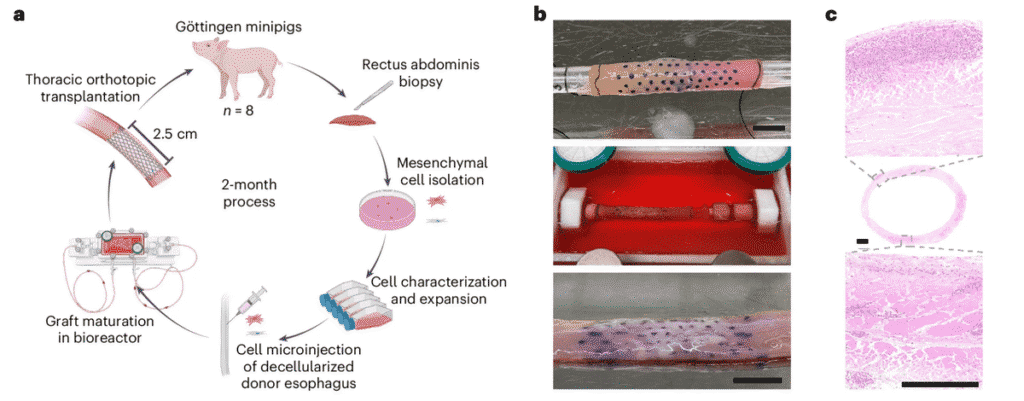
Pour cultiver les œsophages en laboratoire, les chercheurs ont prélevé ceux de jeunes porcs d’environ 10 kilogrammes afin de se rapprocher de la taille de ceux des enfants qui pourraient un jour en bénéficier. Les tissus ont été débarrassés de toutes leurs cellules pour ne garder que la matrice extracellulaire servant d’échafaudage. Cette matrice a ensuite été recolonisée avec les cellules musculaires prélevées sur les animaux receveurs à l’aide d’une biopsie.
Les greffons ont été placés à l’intérieur d’un bioréacteur contenant des solutions de croissance spécifiques pendant une semaine, au cours de laquelle les cellules des receveurs prolifèrent, s’implantent et s’adaptent à leur nouvelle matrice. Les cellules ont pris deux mois pour coloniser entièrement la nouvelle matrice.
Une fois cultivés, les greffons ont été transplantés chez huit porcs receveurs dont des segments d’œsophage de 2,5 centimètres ont été sectionnés. Les implants ont également été recouverts d’un tube en maille biodégradable afin de stimuler la vascularisation.
Des organes artificiels imitant efficacement les fonctions naturelles
D’après les résultats détaillés dans la revue Nature Biotechnology, les huit porcs ont survécu pendant les 30 premiers jours suivant la transplantation, mais seuls cinq ont survécu jusqu’à la fin de l’étude, soit six mois, les trois ayant été euthanasiés pour des raisons humanitaires. Chez les cinq survivants, les greffons transplantés ont développé avec succès des muscles, des nerfs et des vaisseaux sanguins fonctionnels. La cartographie des gènes de la structure transplantée a montré que ceux activés correspondaient à ce qui est attendu dans un tissu naturel.
Une fois entièrement constitué, l’œsophage cultivé pouvait se contracter correctement et générer suffisamment de pression et de coordination pour faire descendre les aliments vers l’estomac des animaux, à l’instar des organes naturels. Les animaux transplantés pouvaient s’alimenter normalement et leur croissance était saine. Bien que certains aient développé des sténoses (un rétrécissement anormal des conduits), celles-ci ont été traitées avec succès par endoscopie.
« La capacité à générer un œsophage doté des composants nécessaires et fonctionnant normalement est impressionnante », a déclaré à la revue Nature, Andrew Barbour, chirurgien universitaire à l’Institut Frazer de l’Université du Queensland à Brisbane, en Australie, qui n’a pas participé à l’étude. « Les greffes ont développé du tissu cicatriciel, ce qui entraîne des difficultés à avaler, mais celui-ci s’est atténué avec le temps, ce qui est également prometteur. Il s’agirait d’une intervention beaucoup moins invasive si nous parvenions à la rendre efficace », a-t-il ajouté.
La transplantation n’a en outre nécessité aucune immunosuppression car le greffon est entièrement composé des cellules des donneurs. « Notre technologie pourrait permettre de reconstruire l’œsophage d’un enfant à partir de ses propres cellules, prélevées lors d’une intervention chirurgicale de toute façon, et associées à une matrice pré-conçue à base de tissu porcin », explique dans le communiqué de l’UCL, Marco Pellegrini, chercheur principal à l’UCL GOS ICH et co-auteur de l’étude.
« Puisque la greffe contient les propres cellules progénitrices musculaires de l’enfant, elle serait reconnue comme son propre tissu. Elle pourrait ainsi évoluer avec lui au fil du temps, sans risque de rejet et sans nécessiter d’immunosuppression à long terme. »
Les chercheurs travaillent actuellement sur l’amélioration du procédé pour pouvoir cultiver des greffons plus longs jusqu’à 10 à 15 centimètres, standardiser le protocole de fabrication, réduire les interventions manuelles et effectuer des tests de sécurité supplémentaires. L’obtention de greffons plus longs représentera un défi supplémentaire car les réseaux de vaisseaux sanguins artificiels devront fonctionner une fois implantés, ce qui est complexe pour des implants plus longs. Les chercheurs estiment néanmoins pouvoir réaliser les premiers essais cliniques d’ici trois à quatre ans.


