Un prototype de rein artificiel a été implanté avec succès chez des porcs, conservant un fonctionnement optimal pendant 7 jours. Composé d’un bioréacteur contenant des cellules tubulaires rénales, le dispositif n’a déclenché aucune réaction immunitaire, même en l’absence de traitement immunosuppresseur. Peut-être en passe de révolutionner les traitements contre l’insuffisance rénale, l’implant pourrait à terme assurer complètement toutes les fonctions d’un véritable rein.
Dans le monde, plus de 2 millions de personnes sont chaque année diagnostiquées d’une insuffisance rénale terminale, dont l’incidence augmente parallèlement aux facteurs de risque tels que le diabète et l’hypertension artérielle. L’hémodialyse est généralement recommandée en tant que traitement de première intention. Cependant, elle ne peut malheureusement pas remplacer entièrement les fonctions rénales perdues. En conséquence, les patients sous dialyse continuent souvent de présenter des symptômes d’insuffisance rénale ainsi que des séquelles telles que le dysfonctionnement endocrinien et cognitif.
Par rapport à la dialyse, la transplantation rénale offre de meilleurs résultats avec une survie à 5 ans supérieure à 80% pour les receveurs d’organes vivants. Mais les risques de rejet de greffe sont élevés et nécessitent la prise à vie d’immunosuppresseurs, pouvant entraîner de graves complications. De plus, l’offre peine considérablement à satisfaire la demande, non seulement en raison du prix, mais également du nombre de donneurs.
Le « Kidney project » de l’Université de Californie à San Francisco (UCSF) ambitionne de surmonter en partie ces défis, en développant un dispositif de rein artificiel. « Nous nous concentrons sur la reproduction en toute sécurité des fonctions clés d’un rein. Le rein bioartificiel rendra le traitement des maladies rénales plus efficace et également beaucoup plus tolérable et confortable », explique Shuvo Roy, le directeur du projet.
Il s’agit d’un dispositif basé sur un bioréacteur renfermant des cellules rénales, destiné à terme à remplacer entièrement un véritable rein, et ce sans besoin d’immunosuppresseur. D’après les résultats détaillés dans la revue Nature Communications, le premier prototype s’est montré prometteur lors de transplantations sur des porcs, en parvenant à conserver ses fonctions pendant une semaine sans déclencher de réponse immunitaire.
Une fonction conservée à plus de 90 %
Un essai clinique de phase 2 a précédemment démontré que les dispositifs d’assistance aux tubules rénaux (RAD) amélioraient les traitements de remplacement rénal. Il s’agit d’appareils de thérapie cellulaire, composés d’un hémofiltre conventionnel tapissé d’une monocouche de cellules tubulaires rénales (régulant l’homéostasie volumétrique). La technique a réduit de 50% le risque de décès des patients.
Le rein bioartificiel implantable de l’UCFS est quant à lui une approche biohybride de la RAD, imitant la physiologie du rein humain. Il comprend un hémofiltre en silicium pouvant assurer une perméabilité sélective comparable à celle du glomérule, inséré dans un bioréacteur. À l’intérieur de ce dernier sont également encapsulées des cellules rénales tubulaires, pouvant réabsorber les solutés et l’eau et recréer les fonctions métaboliques et endocrinologiques des tubules rénaux dans l’organisme.
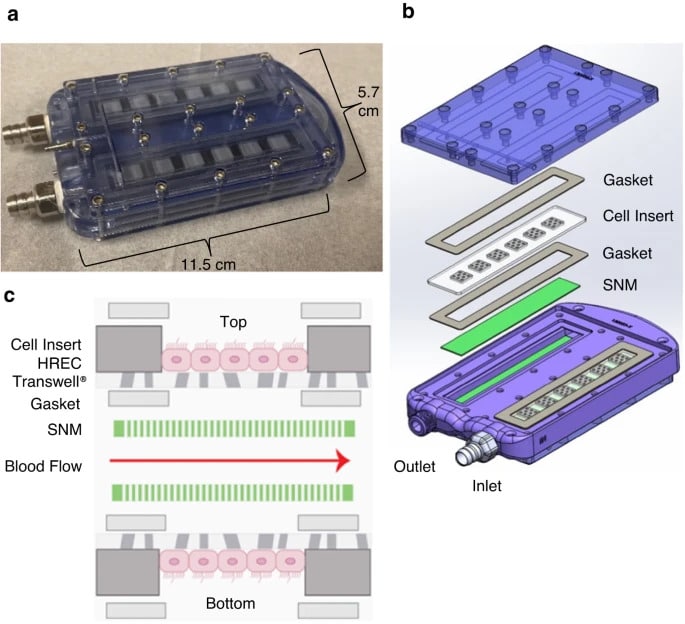


Plus précisément, l’hémofiltre en silicium est conçu de sorte à servir de membrane biomimétique, ponctuée de nanopores dispersés à l’échelle nanométrique. Combinée à une technique spéciale de microfabrication de semiconducteurs, cette porosité permet d’obtenir une sélectivité moléculaire élevée — permettant d’empêcher la diffusion de cytokines inflammatoires — ainsi qu’une meilleure biocompatibilité. Plus important encore, la membrane permet une filtration sanguine sans pompe et s’appuie uniquement sur la pression de perfusion naturelle fournie par le cœur. Ensuite, les cellules tubulaires traitent en temps réel l’ultrafiltrat généré par l’hémofiltre et renvoient sélectivement les ions sodium et l’eau dans le système circulatoire, afin d’assurer l’homéostasie volumétrique et ionique. Les toxines et solutés en excès sont rejetés dans l’eau restante pour être évacués vers la vessie.
Le dispositif a été implanté chez des porcs adultes et en bonne santé (immunocompétents), sans anticoagulant ni immunosuppresseur. Après sept jours, les cellules tubulaires ont conservé une viabilité et une fonction supérieures à 90%, ainsi qu’une expression normale ou élevée du gène codant pour la vitamine D. Malgré un protocole de xénogreffe (une transplantation s’effectuant entre deux espèces différentes), les cellules ne présentaient que des dommages mineurs et les cytokines exprimées n’indiquaient pas de rejet de greffe.
« Nous devions prouver qu’un bioréacteur fonctionnel ne nécessiterait pas de médicaments immunosuppresseurs, et nous l’avons fait », affirme Roy. « Nous n’avons eu aucune complication et pouvons désormais itérer, atteignant l’ensemble des fonctions rénales à l’échelle humaine », conclut-il. En prochaine étape, les chercheurs comptent étendre les essais sur les animaux à un mois et espèrent rapidement passer aux essais cliniques en adaptant le dispositif à l’échelle humaine.