Depuis quelques années, les scientifiques tentent de « corriger » les mutations génétiques à l’origine de la rétinite pigmentaire en utilisant la technique d’édition génétique CRISPR, mais les résultats sont encore insatisfaisants. Cependant, une version améliorée de CRISPR présentée dans une nouvelle étude va peut-être changer la donne, en permettant de rectifier une grande variété de mutations génétiques grâce à sa plus grande polyvalence. La nouvelle technique a notamment permis de restaurer la vision chez des souris atteintes de la maladie, et ce même à un âge avancé.
À l’heure actuelle, aucun traitement curatif n’existe contre la rétinite pigmentaire, une maladie génétique rare et héréditaire affectant 1 personne sur 4000 dans le monde. La maladie a en effet pour origine la mutation de plus de 100 gènes différents intervenant dans le développement des cellules rétiniennes ou photoréceptrices. Apparaissant généralement entre l’enfance et l’âge de 30 ans, les symptômes les plus couramment observés dans la maladie se traduisent par une perte visuelle progressive dans un environnement sombre ou tamisé, une perte partielle de la vision périphérique et une perte d’acuité visuelle globale. Ces déficits visuels sont respectivement dus au dysfonctionnement puis à la perte des photorécepteurs en bâtonnets et en cônes, et aboutissent à une perte de vision irréversible au stade le plus avancé de la maladie.
Pour tenter de restaurer durablement la vision chez les personnes souffrant de rétinite pigmentaire, la technique CRISPR serait la piste la plus prometteuse à ce jour. En « coupant » avec précision un brin d’ADN ou d’ARN par le biais d’enzymes ou de bactéries, la technologie permet de modifier, de remplacer ou de supprimer un gène sans altérer le génome. De ce fait, elle peut être utilisée dans les tentatives de correction d’un grand nombre de mutations génétiques.
Nombre de défis restent cependant à surmonter avant l’application clinique de la technologie CRISPR, surtout dans la rétinite pigmentaire autosomique dominante. En effet, dans le cas d’un trouble autosomique dominant, l’individu hérite des ses parents d’une seule copie d’un gène muté et d’un gène normal sur une paire de chromosomes autosomiques. Ainsi, la difficulté réside dans l’application de CRISPR pour éditer uniquement la copie mutante sans endommager celle qui est saine. L’opération rencontre moins de difficultés dans le cas où la mutation génétique est de nature autosomique récessive, car les personnes concernées héritent de deux copies du gène mutant.
Et bien que des chercheurs aient déjà utilisé l’édition génétique pour restaurer la vision de souris atteintes de troubles génétiques, cela se limitait aux cellules non neuronales soutenant les photorécepteurs. Or, la plupart des dégénérescences oculaires héréditaires — y compris la rétinite pigmentaire — sont causées par des mutations génétiques au niveau des photorécepteurs neuronaux.
Dans le cadre de la nouvelle étude, parue dans la revue Journal Of Experimental Medicine, les chercheurs, de l’Université des sciences et technologies de Wuhan (en Chine), ont développé une version plus polyvalente et ainsi plus performante de CRISPR. Baptisée PESpRY , la nouvelle technologie peut corriger une grande variété de mutations génétiques pathogènes quelque soit leur emplacement dans le génome.
« La capacité d’éditer le génome des cellules rétiniennes neurales, en particulier les photorécepteurs malades ou mourants, fournirait des preuves beaucoup plus convaincantes des applications potentielles de ces outils d’édition du génome dans le traitement de maladies telles que la rétinite pigmentaire », explique dans un communiqué Kai Yao, professeur à l’Université des sciences et technologies de Wuhan et coauteur principal de la nouvelle étude. En ciblant précisément la mutation d’un gène codant pour une enzyme appelée PDE6β, les chercheurs ont réussi à restaurer la vision chez des souris où l’on avait induit une rétinite pigmentaire.
Une guérison conservée en vieillissant
Pour tester leur technologie, Yao et ses collègues ont corrigé la mutation génétique empêchant le codage de l’enzyme (précédemment mentionnée) chez des souris atteintes de rétinite pigmentaire. Une fois le génome des souris réparé, la reprise de l’activité de l’enzyme a permis d’empêcher la perte des photorécepteurs en cônes et en bâtonnets dans les rétines des rongeurs. Les observations microscopiques ont montré une importante régénération des cellules photoréceptrices en bâtonnets. Il a également été constaté que la lumière a pu être transformée correctement en stimuli électriques véhiculant l’information visuelle au cerveau (par le biais du nerf optique).
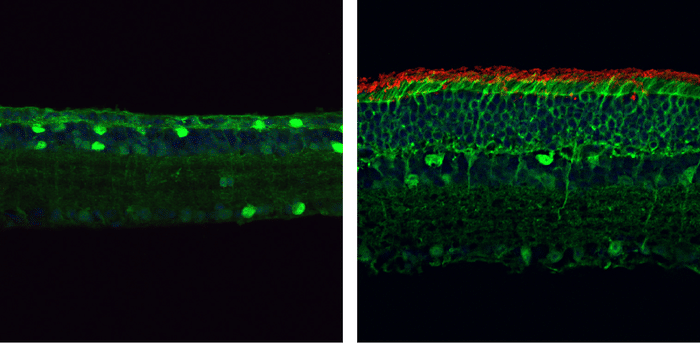


Pour confirmer si les souris avaient vraiment recouvré la vision (évaluer leur acuité visuelle), des tests comportementaux ont été effectués. Elles ont notamment pu sortir d’un labyrinthe aquatique en étant guidées par des signaux lumineux. Elles ont également effectué des mouvements de la tête en réponse à des stimuli visuels. Par ailleurs, les chercheurs ont pu constater que les performances visuelles ont pu être conservées même chez les animaux atteignant un âge avancé.
Toutefois, les chercheurs soulignent que de nombreux travaux sont encore nécessaires pour évaluer correctement l’innocuité et l’efficacité de leur nouvelle méthode d’édition génétique avant de pouvoir l’appliquer chez l’Homme. Mais, « notre étude fournit des preuves substantielles de l’applicabilité in vivo de cette nouvelle stratégie d’édition du génome et de son potentiel dans divers contextes de recherche et thérapeutiques, en particulier pour les maladies rétiniennes héréditaires », estime Yao.