Le trouble du déficit de l’attention avec ou sans hyperactivité (TDAH) concerne des millions de personnes (environ 6% des enfants scolarisés et 3% des adultes). Ce trouble peut avoir de lourdes répercussions sur la vie scolaire, sociale, familiale et professionnelle, auxquelles s’ajoute désormais un nouveau fardeau : une étude américaine révèle que la prédisposition génétique au TDAH influence positivement le risque de déclin cognitif et de maladie d’Alzheimer.
Le TDAH est un trouble du neurodéveloppement, caractérisé par des niveaux élevés d’inattention, et/ou d’agitation et d’impulsivité, qui peuvent nuire sévèrement à la qualité de vie. Pendant longtemps, ce trouble était considéré comme une « maladie infantile », qui disparaissait à l’âge adulte. On sait désormais qu’il persiste tout au long de la vie — même si les symptômes se font plus variés et plus subtils à l’âge adulte.
Quelques études épidémiologiques récentes ont suggéré que le TDAH pouvait être un facteur de risque de troubles cognitifs et de la maladie d’Alzheimer. « Cependant, ces résultats reposent principalement sur les dossiers de santé électroniques et peuvent présenter des estimations biaisées de la prévalence de la maladie », notent des chercheurs de la faculté de médecine de l’Université de Pittsburgh (UPMC), qui ont entrepris d’examiner plus avant ce lien potentiel.
Une combinaison de plusieurs facteurs génétiques
Il est crucial d’identifier tout facteur de risque afin de prendre en charge au plus tôt les patients susceptibles de développer la maladie d’Alzheimer. L’absence d’études à grande échelle suivant les patients atteints de TDAH jusqu’à un âge avancé a néanmoins limité l’étude du déclin cognitif lié à l’âge dans le cas du TDAH. Pour contourner cette difficulté, les chercheurs se sont appuyés ici sur la prédisposition génétique au TDAH dans leur cohorte d’étude, et non sur un diagnostic clinique confirmé. Ils disposaient ainsi d’une base de données de 212 adultes, âgés de 55 à 90 ans, qui ne présentaient aucun trouble cognitif au départ.
Cette base de données comprenait des scintigraphies cérébrales, les niveaux de protéines β-amyloïde et tau mesurés sur des scintigraphies TEP et dans le liquide céphalo-rachidien, ainsi que les résultats d’évaluations cognitives régulières réalisées au cours de six années consécutives. Les chercheurs ont également eu accès aux séquences du génome de ces patients.
Pour chacun d’entre eux, ils ont estimé le score de risque polygénique du TDAH, qui représente la probabilité génétique de développer le trouble, compte tenu de la séquence entière du génome. Une accumulation de facteurs génétiques (et environnementaux) est en effet vraisemblablement à l’origine du TDAH ; ces facteurs entraînent de légères modifications au niveau des neurones qui contrôlent les processus cognitifs, motivationnels et émotionnels.
Cette étude visait ainsi à déterminer si la prédisposition génétique au TDAH, telle que mesurée par le score de risque polygénique, est associée ou non au déclin cognitif et au développement de la physiopathologie de la maladie d’Alzheimer. « Cette étude met en évidence ce dont beaucoup de personnes dans le domaine discutent déjà : l’impact du TDAH peut être observé tout au long de la vie, et il pourrait être lié à des conditions neurodégénératives », a déclaré le Dr Douglas Leffa, résident en psychiatrie à l’UPMC.
La prédisposition au TDAH est liée au déclin cognitif
En comparant le score de chaque patient avec les éventuels signes de maladie d’Alzheimer, l’équipe a constaté qu’un score polygénique plus élevé peut prédire une détérioration cognitive ultérieure et le développement de la physiopathologie du cerveau d’Alzheimer chez les personnes âgées qui, jusque-là, ne souffraient pas de troubles cognitifs. « Un score élevé était associé à un déclin cognitif plus important sur 6 ans », notent-ils.
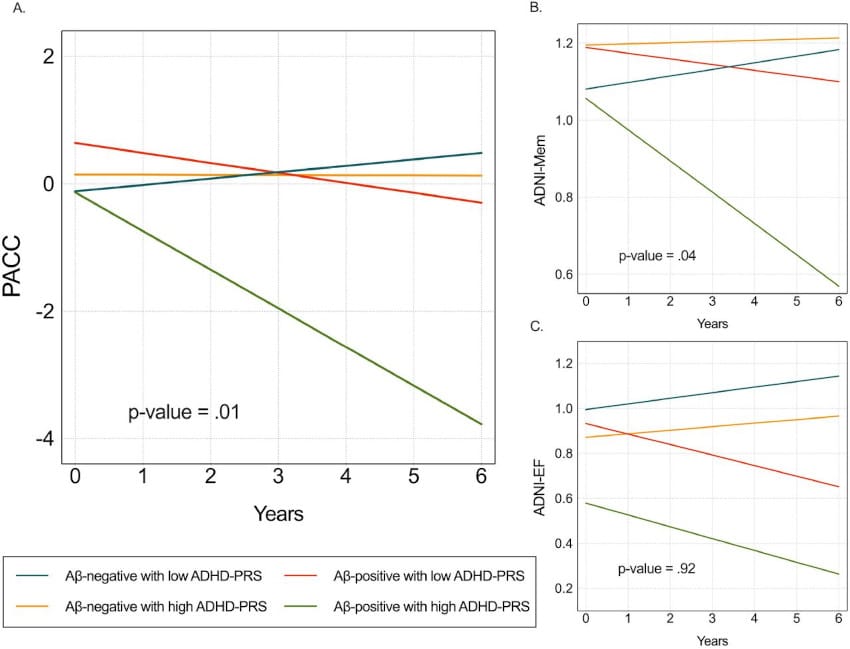
En outre, l’effet combiné d’un risque polygénique élevé de TDAH et des dépôts de protéine β-amyloïde (Aβ) dans le cerveau sur la détérioration cognitive était plus significatif que l’effet produit par chacune de ces conditions considérées individuellement. Un risque plus élevé était également associé à des niveaux plus élevés de protéine tau dans le liquide céphalo-rachidien et à une atrophie fronto-pariétale, ajoutent les chercheurs.
L’équipe précise que ces résultats ont été principalement observés chez les individus Aβ-positifs, suggérant que la prédisposition génétique pour le TDAH augmente la susceptibilité aux effets néfastes de la pathologie Aβ.
Si le lien semble bien réel, il doit encore faire l’objet de recherches plus approfondies, sur une cohorte plus large et plus diversifiée (les données démographiques de la base de données utilisée étaient limitées aux patients de race blanche et ayant effectué en moyenne plus de 16 ans d’études). Des recherches supplémentaires sont également nécessaires pour déterminer si les interventions visant à corriger le TDAH peuvent influencer le risque de maladie d’Alzheimer.
L’équipe s’efforce déjà de recruter davantage de participants issus de milieux sous-représentés, atteints de TDAH dans l’enfance, afin de commencer des suivis à long terme et rechercher des biomarqueurs de la maladie d’Alzheimer. « Ces études sont longues à réaliser, mais elles sont importantes pour notre compréhension des maladies neurologiques multifactorielles et de la façon dont elles affectent les troubles cognitifs », conclut le Dr Tharick Pascoal, professeur adjoint de psychiatrie à l’UPMC et co-auteur de l’étude.


