VERVE-101, un traitement basé sur l’édition génique CRISPR, offre une potentielle solution sur le long terme à l’hypercholestérolémie, en désactivant le gène PCSK9. Cette approche a démontré une réduction notable du mauvais cholestérol (LDL) avec une unique dose dans le cadre d’essais cliniques. Toutefois, elle soulève des préoccupations relatives à la sécurité, l’éthique et la disponibilité, nécessitant des évaluations approfondies.
La médecine moderne se confronte régulièrement à des défis complexes, notamment dans la gestion des maladies cardiovasculaires et de leurs facteurs de risque. Parmi ces derniers, l’hypercholestérolémie, caractérisée par un taux élevé de cholestérol dans le sang, représente une préoccupation majeure pour la santé publique.
Face à cette problématique, la récente mise au point de VERVE-101, un traitement basé sur l’édition génique CRISPR, se montre prometteuse. Verve Therapeutics, société de biotechnologie basée à Boston, dans le Massachusetts, a rapporté qu’une seule injection de ce traitement réduisait de manière significative le cholestérol LDL, communément appelé « mauvais cholestérol » (contrairement au HDL), en ciblant directement sa cause génétique.
L’équipe de recherche a présenté ses résultats lors des sessions scientifiques 2023 de l’American Heart Association du 11 au 13 novembre (à Philadelphie). Leurs travaux sont également disponibles dans la revue Circulation.
L’édition génique contre le cholestérol
Les chercheurs se sont intéressés à l’hypercholestérolémie familiale hétérozygote. Cette condition génétique, caractérisée par des niveaux élevés de cholestérol LDL dès la naissance, augmente considérablement le risque de développer des maladies cardiovasculaires.
Le traitement VERVE-101 exploite la technologie d’édition génique CRISPR pour cibler et désactiver spécifiquement le gène PCSK9 dans le foie. Ce gène joue un rôle crucial dans la régulation du cholestérol LDL. En désactivant ce gène, VERVE-101 réduit la capacité du corps à produire le cholestérol LDL, entraînant ainsi une baisse significative de son niveau dans le sang.
Plus précisément, il s’agit d’utiliser la machinerie CRISPR-Cas9 pour apporter des modifications très précises à ce gène — en modifiant chimiquement les bases d’un seul nucléotide — sans casser les doubles brins de l’ADN. La technique a été développée par une équipe dirigée par le biologiste chimique David Liu de l’Université Harvard (Massachusetts), en 2018.
VERVE-101 désactive donc le gène PCSK9, affectant ainsi l’enzyme qu’il code. Normalement, cette enzyme limite le nombre de récepteurs du cholestérol LDL à la surface des cellules, augmentant le cholestérol dans le sang. En désactivant PCSK9, les niveaux de LDL diminuent, réduisant le risque de crise cardiaque et d’accident vasculaire cérébral. Comme l’explique Sekar Kathiresan, PDG de Verve, maintenir un faible taux de LDL réduit considérablement le risque de problèmes cardiaques.
Le traitement utilise deux molécules d’ARN encapsulées dans une nanoparticule lipidique : un ARN messager qui modifie l’ADN et un ARN guide ciblant PCSK9. Injectées, ces nanoparticules sont absorbées par les cellules hépatiques et modifient le gène PCSK9, empêchant la production de la protéine PCSK9 et réduisant ainsi le cholestérol LDL.
Des résultats pleins d’espoir avec une seule dose
Les essais cliniques de VERVE-101 ont été particulièrement prometteurs. Les patients ayant reçu une seule injection de ce traitement ont montré une réduction impressionnante de leur taux de cholestérol LDL, allant jusqu’à 55%. Cette performance est particulièrement notable lorsqu’on la compare aux résultats obtenus avec les traitements conventionnels, tels que les statines, qui sont actuellement la norme dans la gestion de l’hypercholestérolémie. D’ailleurs, les statines constituent un traitement controversé selon de nombreux chercheurs, comme cela est expliqué dans le documentaire Cholestérol, le Grand Bluff disponible sur notre chaîne Trust My Science TV (pour le voir gratuitement, utilisez le code promo TMS1).
En plus de la baisse du cholestérol LDL, les essais ont également révélé une diminution significative des protéines PCSK9 dans le sang des patients traités. Cette observation est cruciale, car elle indique non seulement l’efficacité immédiate du traitement, mais aussi son potentiel à induire des effets bénéfiques durables sur le long terme.
Notons que les chercheurs ont testé différentes doses de VERVE-101. La première cohorte (n=3) a reçu une faible dose de 0,1 mg/kg et les autres cohortes des doses croissantes, après consultation d’un comité indépendant de surveillance de la sécurité. La dose la plus élevée reçue était de 0,6 mg/kg.
En outre, dans une étude préclinique impliquant des singes, la réduction du cholestérol LDL a duré 2,5 ans après une dose unique du traitement.
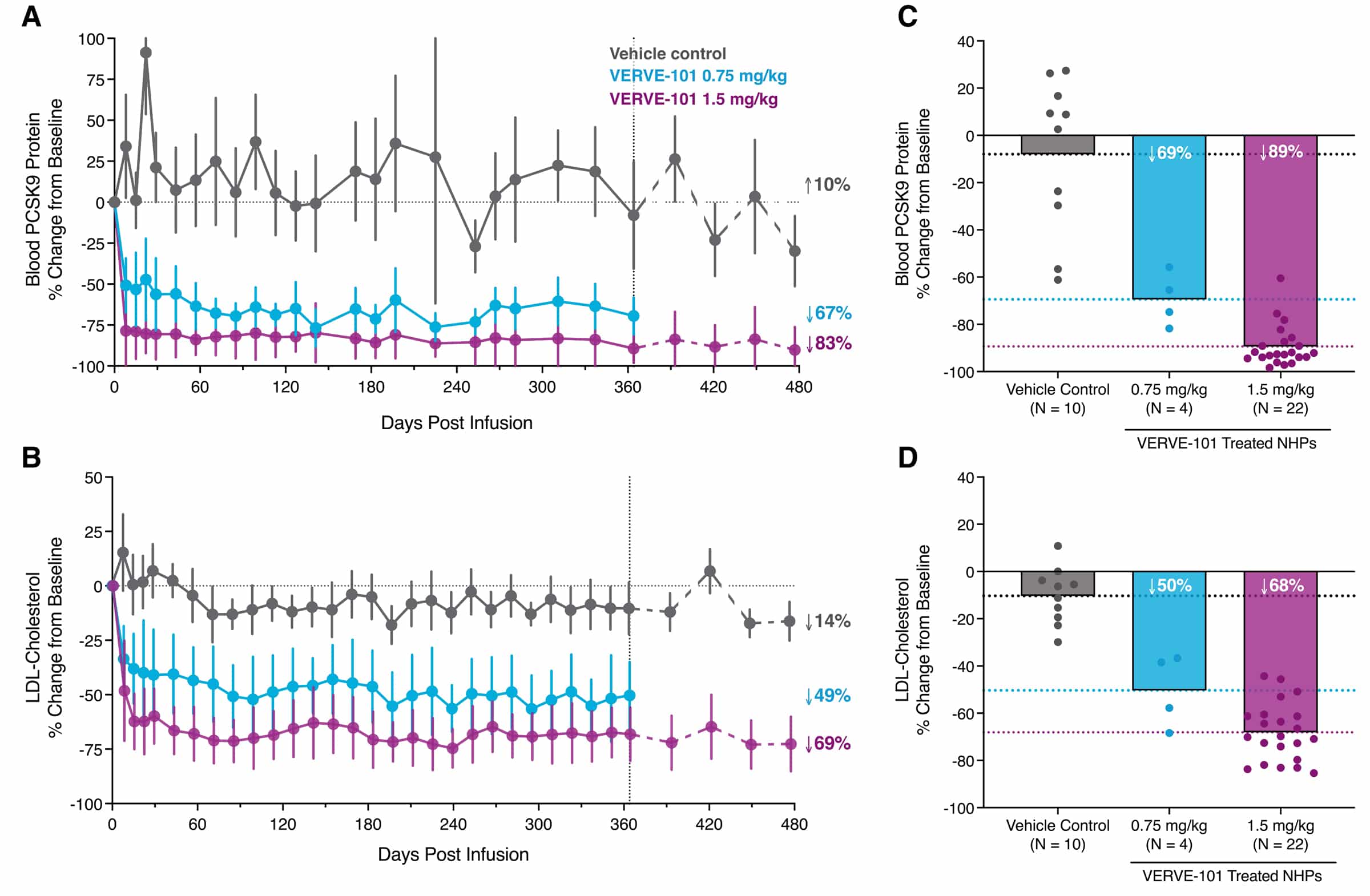


Ces résultats suggèrent que VERVE-101 pourrait constituer une alternative prometteuse aux traitements actuels, offrant une option plus durable et potentiellement plus efficace pour les patients souffrant d’hypercholestérolémie, en particulier ceux avec des formes génétiques de la maladie.
Implications éthiques et réglementaires
Bien que les événements indésirables graves liés à cette thérapie soient rares (un décès est à déplorer), leur occurrence soulève des inquiétudes quant aux risques. Le cours de l’action de Verve a chuté de près de 40% après la publication des résultats. La Food and Drug Administration (FDA) des États-Unis, consciente de ces risques, a imposé un suivi rigoureux de 14 ans pour tous les participants aux essais d’édition génique. Cette mesure vise à surveiller les effets à long terme et à garantir que les bénéfices du traitement l’emportent sur les risques.
Au-delà de la sécurité, la modification génétique permanente, bien qu’offrant des avantages thérapeutiques potentiels, interpelle sur le plan de l’éthique médicale. Modifier l’ADN d’un individu soulève des questions sur le consentement, les implications à long terme pour la personne traitée et les générations futures, ainsi que sur la définition même de ce qui est considéré comme une intervention médicale acceptable. Cela nécessite une collaboration étroite entre les chercheurs, les praticiens médicaux, les régulateurs et les patients.