DoriVac, une technologie basée sur l’origami d’ADN qui agit à la fois comme vaccin et comme adjuvant, pourrait constituer une alternative prometteuse aux vaccins à ARNm, selon une récente étude. Lors d’essais sur des souris et des organes humains sur puce, la technologie a induit des réponses immunitaires comparables à celles des vaccins standards à ARNm, mais offrirait l’avantage supplémentaire d’être plus facile à concevoir et plus stable et donc plus facile à conserver.
Les vaccins à ARNm sont au centre des préoccupations en matière de santé publique depuis la pandémie de Covid-19. D’un côté, leur polyvalence et leur rapidité de conception ont permis de développer des vaccins en un temps record, évitant probablement des millions de décès dans le monde. Cette polyvalence tient au fait qu’ils peuvent être mis à jour plus rapidement que les vaccins traditionnels, les rendant ainsi particulièrement adaptés aux virus grippaux qui mutent rapidement et qui sont susceptibles de déclencher des pandémies.
Cette adaptabilité a également fait qu’ils sont actuellement explorés pour la lutte contre d’autres maladies infectieuses, tels que le VIH/sida, le virus Zika et la tuberculose, ainsi que pour le traitement d’autres pathologies telles que le cancer et les maladies auto-immunes.
D’un autre côté cependant, la pandémie de Covid-19 a également fait office de test pharmacoépidémiologique, mettant notamment en lumière leurs limites. L’une d’entre elles est que les réponses immunitaires induites par les vaccins à ARNm anti-Covid peuvent varier significativement d’un individu à l’autre, sans compter que leur durée est limitée. Ces facteurs, combinés à l’évolution rapide du virus, sont probablement à l’origine des controverses entourant actuellement les vaccins à ARNm, en particulier aux États-Unis.
Il existe d’autres inconvénients, notamment leur complexité et leurs coûts de fabrication, un contrôle limité du nombre de molécules d’ARNm encapsulées dans les nanoparticules lipidiques de délivrance, la nécessité d’un stockage à froid et des effets hors cible potentiels. Ces limites ont motivé l’identification d’approches vaccinales alternatives.
Une équipe de recherche multidisciplinaire de l’Institut Wyss de l’Université Harvard, du Dana-Farber Cancer Institute (DFCI) et d’autres institutions, propose une approche alternative consistant en une nanotechnologie d’origami d’ADN très polyvalente, à la fois vaccin et adjuvant.
« Grâce à la plateforme DoriVac, nous avons développé un châssis extrêmement flexible présentant de nombreux avantages essentiels, notamment un contrôle sans précédent sur la composition du vaccin et la capacité de programmer la reconnaissance immunitaire dans les cellules immunitaires ciblées au niveau moléculaire afin d’obtenir de meilleures réponses », explique dans un billet de blog William Shih, co-auteur correspondant de l’étude et membre du corps professoral du Wyss Institute.
Une polyvalence et une adaptabilité accrues
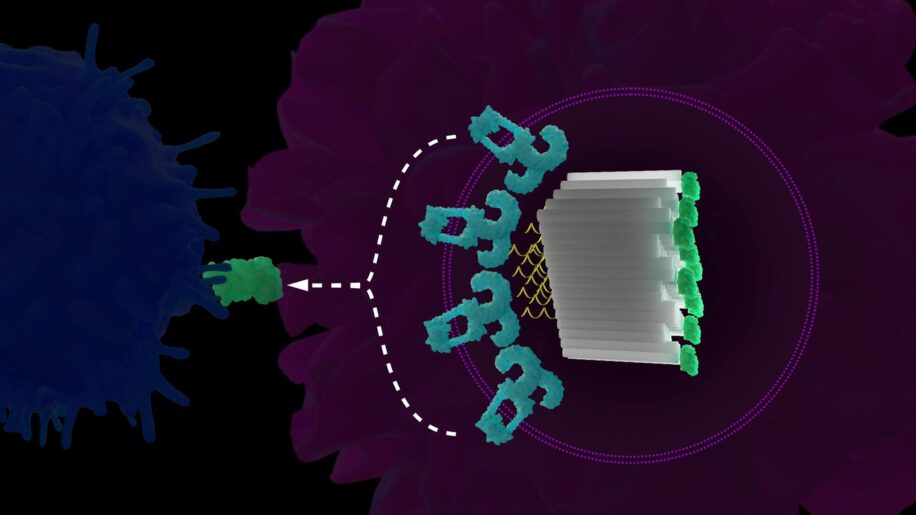
Initialement développés par l’équipe de Shih en 2024 pour le cancer, les vaccins DoriVac sont constitués de nanostructures carrées d’ADN qui s’auto-replient et s’auto-assemblent, d’où l’appellation origami. Ces structures présentent au niveau de l’une de leurs faces des molécules adjuvantes dont les espacements nanométriques sont optimisés. Sur la face opposée sont placés des antigènes au choix tels que des peptides et des protéines dérivés de tumeurs ou de pathogènes.
Les premiers essais sur des souris dans le contexte du cancer ont montré que les souris traitées avec le vaccin présentaient des réponses immunitaires améliorées, notamment grâce aux molécules adjuvantes qui stimulent l’immunité avec une grande précision. Les chercheurs ont ensuite cherché à déterminer dans quelle mesure la technologie pourrait être transposée aux maladies infectieuses.
« Alors que nous développions la plateforme pour les applications en cancérologie, la pandémie de COVID-19 faisait toujours rage. La question s’est donc rapidement posée de savoir si l’activité adjuvante supérieure de DoriVac pouvait également être exploitée dans le contexte des maladies infectieuses », explique Yang (Claire) Zeng, auteur principal de la nouvelle étude et aujourd’hui cofondateur et PDG/CTO de DoriNano, où il dirige la transposition de la technologie en applications cliniques.
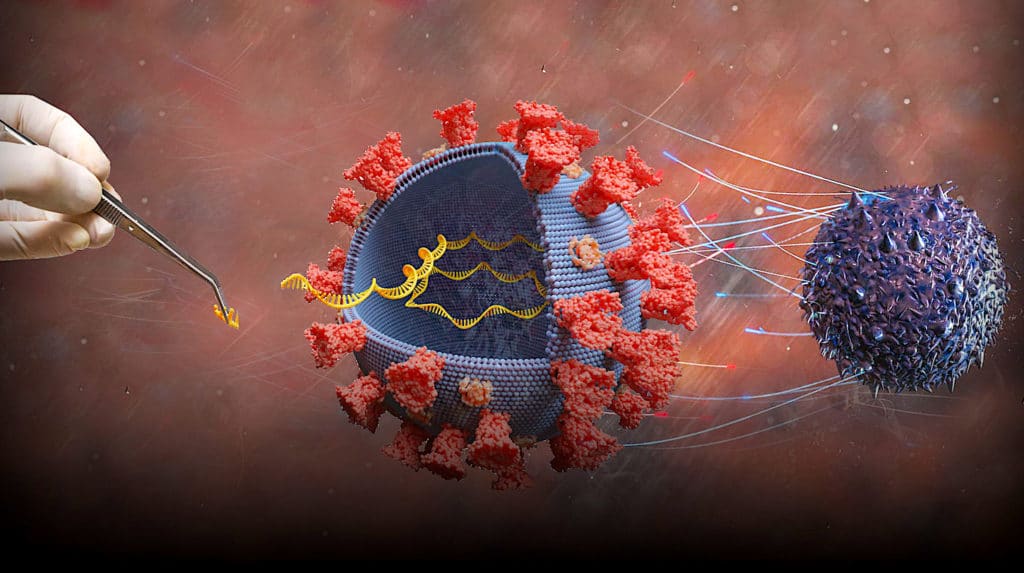
Les vaccins DoriVac antiviraux ciblent une région peptidique appelée HR2 et conservée dans les protéines de pointe (ou protéine Spike, qui agit comme une clé pour se fixer au récepteur ACE2 des cellules humaines), régulant le potentiel infectieux d’une gamme de virus, dont le SARS-CoV-2, le VIH et Ebola. Le vaccin a induit des réponses immunitaires prometteuses lors d’essais sur des modèles murins de vaccination contre le SARS-CoV-2. Plus précisément, le vaccin a induit d’importantes réponses immunitaires à médiation humorale et cellulaire spécifiques à l’antigène.
« Notre analyse des réponses immunitaires provoquées par ces premiers vaccins DoriVac chez la souris a conduit à plusieurs observations encourageantes, notamment une activation significativement plus importante et plus large de l’immunité humorale et cellulaire dans un éventail de types de cellules immunitaires pertinents que ce que les antigènes et adjuvants sans origami pouvaient produire », indique Zeng.
Des réponses immunitaires comparables à celle des vaccins à ARNm
Étant donné que les réponses aux agents pathogènes peuvent différer chez les souris et les humains, les chercheurs ont reproduit les tests du vaccin DoriVac anti-SARS-CoV-2-HR2 sur un ganglion lymphatique humain sur puce, qui offrirait une prédiction préclinique rapide des réponses immunitaires chez l’homme.
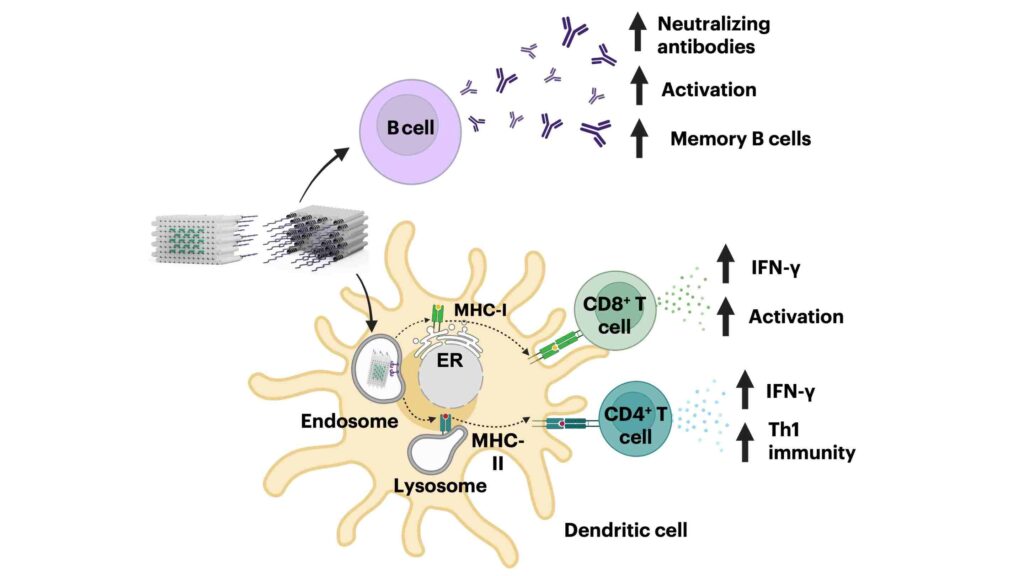
Les résultats — décrits dans l’étude publiée récemment dans la revue Nature Biomedical Engineering — ont montré que le vaccin activait efficacement les cellules dendritiques humaines et augmentait leur production de cytokines inflammatoires à des niveaux beaucoup plus élevés que les composants du vaccin sans origami. La concentration de lymphocytes T CD4+ et CD8+ protecteurs a également augmenté.
L’équipe a également évalué les effets du vaccin lorsqu’il intègre la protéine Spike complète du SARS-CoV-2 et l’ont comparé aux vaccins à ARNm standards à base de nanoparticules lipidiques, produits par Moderna et Pfizer/BioNTech. Les réponses observées des lymphocytes T antiviraux et des lymphocytes B producteurs d’anticorps étaient comparables pour les deux types de vaccin.
« Cela a mis en évidence le potentiel de DoriVac en tant que plateforme vaccinale auto-adjuvantée basée sur la nanotechnologie de l’ADN. Mais les vaccins DoriVac présentent plusieurs autres avantages : ils ne sont pas soumis aux mêmes exigences de chaîne du froid que les vaccins à ARNm-LNP et pourraient donc être distribués beaucoup plus efficacement, notamment dans les régions aux ressources limitées ; et ils pourraient surmonter certaines des complexités de fabrication considérables des vaccins formulés en LNP, pour ne citer que deux avantages majeurs », conclut Shih.