L’émergence du Zosurabalpin, une substance ultraefficace contre certaines souches, répond à l’urgence sanitaire posée par les bactéries résistantes aux antibiotiques. La molécule se montre particulièrement efficace contre les pathogènes Gram-négatifs.
Face à l’augmentation alarmante des infections bactériennes résistantes aux antibiotiques, de nombreux chercheurs tentent de trouver des solutions innovantes. Récemment, des chercheurs de l’Université Harvard et de la société suisse de soins de santé Hoffmann-La Roche, ont affirmé que leur nouvel antibiotique, le Zosurabalpin, est très efficace contre Acinetobacter baumannii. Cette bactérie, également connue sous le nom de CRAB, peut provoquer de graves infections pulmonaires, des voies urinaires et du sang, selon les Centres pour le contrôle et la prévention des maladies des États-Unis. Elle est résistante, entre autres, aux carbapénèmes, une classe d’antibiotiques à large spectre.
Selon une récente étude publiée dans la revue Nature, la nouvelle molécule représente une avancée significative dans la lutte contre les bactéries Gram-négatives, particulièrement résistantes aux traitements actuels. Son action unique, bloquant le transport des lipopolysaccharides, promet de renforcer l’arsenal médical contre les infections mortelles et résistantes tout en soulignant la nécessité d’innovations continues face à l’évolution rapide de la résistance bactérienne.
Un bouclier contre les superbactéries
Le Zosurabalpin possède un mécanisme d’action unique. Contrairement aux antibiotiques traditionnels, il cible spécifiquement les bactéries Gram-négatives, un groupe notoirement difficile à traiter en raison de la double membrane cellulaire. Cette structure complexe agit comme une barrière défensive, empêchant de nombreux médicaments d’atteindre leur cible.
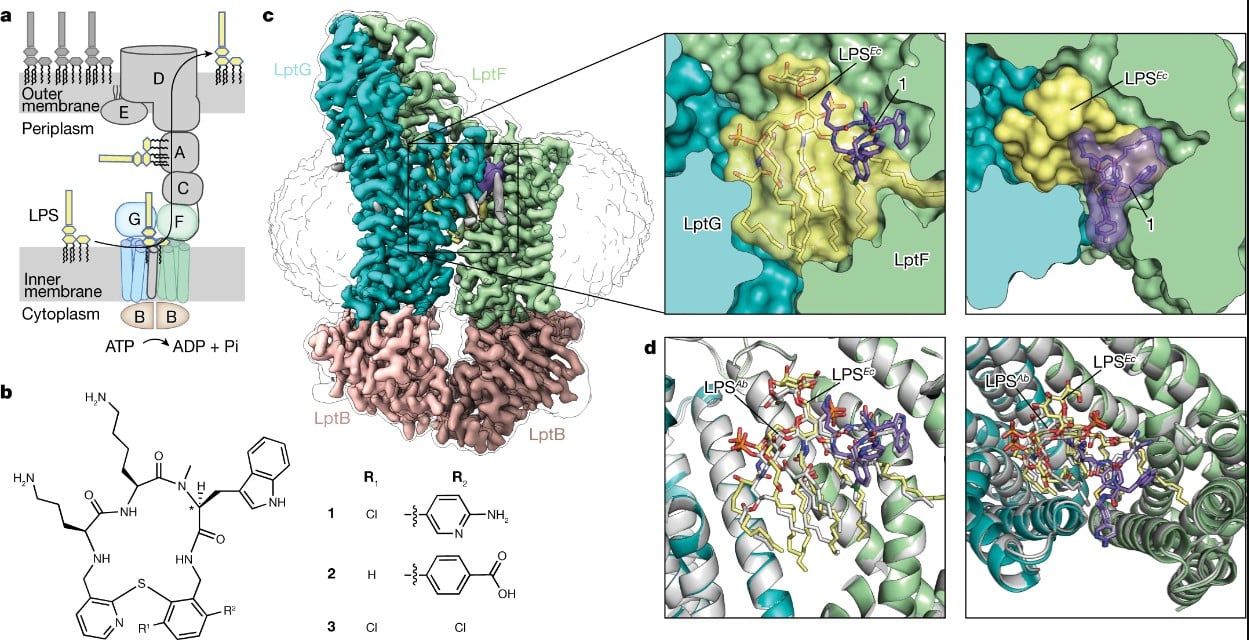
Le Zosurabalpin contourne ce problème en intervenant dans le processus de transport des lipopolysaccharides (LPS), des molécules essentielles à la construction et au maintien de la membrane externe de ces bactéries. En bloquant le transport des LPS, le Zosurabalpin compromet l’intégrité de la membrane externe, entraînant ainsi la mort de la bactérie.
Les essais précliniques du Zosurabalpin, notamment sur des modèles animaux, ont démontré son efficacité contre des infections sévères. Dans des études sur des souris, l’antibiotique a significativement réduit les niveaux de Carbapenem-resistant Acinetobacter baumannii (CRAB), une bactérie particulièrement résistante et dangereuse. Les souris atteintes de pneumonie induite par CRAB ont montré une diminution notable de la charge bactérienne après traitement avec le Zosurabalpin.
Plus notable encore, chez les souris souffrant de sepsis causé par CRAB, l’antibiotique a non seulement réduit la présence bactérienne, mais a également évité la mort. Ces résultats sont d’autant plus significatifs que CRAB est connu pour sa résistance aux traitements existants et sa capacité à causer des infections mortelles, en particulier dans les environnements hospitaliers. L’efficacité du Zosurabalpin dans ces modèles précliniques suggère un potentiel considérable pour le traitement des infections humaines résistantes aux antibiotiques.
Un pas vers de nouveaux traitements
La mise au point du Zosurabalpin ouvre des perspectives inédites pour le développement d’antibiotiques ciblant les mécanismes de défense spécifiques des bactéries Gram-négatives. En ciblant des processus cellulaires clés spécifiques aux bactéries Gram-négatives, il est possible d’élaborer des traitements plus efficaces contre une gamme plus large de pathogènes résistants, y compris ceux qui sont actuellement considérés comme des menaces critiques pour la santé publique.
Cependant, le chemin vers l’application clinique du Zosurabalpin est jonché de défis. Le développement d’un nouvel antibiotique, de sa conception en laboratoire à son approbation pour usage clinique, est un processus long et coûteux, impliquant des études approfondies pour assurer son efficacité et sa sécurité. Le Zosurabalpin est actuellement en phase 1 d’essais cliniques pour évaluer la sécurité, la tolérabilité et la pharmacologie de la molécule chez l’homme, selon les auteurs de l’étude.
Dans un article de CNN, le Dr César de la Fuente, professeur à l’Université de Pennsylvanie, explique : « Cela pourrait prendre plusieurs années. Néanmoins, je pense que d’un point de vue universitaire, il est passionnant de voir un nouveau type de molécule qui tue les bactéries d’une manière différente. Nous avons certainement besoin de nouvelles façons originales de penser la découverte des antibiotiques, et je pense que ceci en est un bon exemple ».
De plus, le paysage de la résistance aux antibiotiques est en constante évolution, ce qui exige une adaptation continue des stratégies thérapeutiques. Les chercheurs affirment que l’approche utilisée pour inhiber la croissance d’Acinetobacter pourrait aider contre d’autres bactéries difficiles à éradiquer, comme E. coli.
La communauté scientifique doit donc rester vigilante et innovante, non seulement pour développer de nouveaux médicaments, mais aussi pour anticiper et contrer les mécanismes de résistance bactérienne émergents.