Des physiciens suggèrent dans une nouvelle étude que plutôt que d’être parfaitement symétriques, le chauffage et le refroidissement se manifestent de façon asymétrique et ainsi fondamentalement différente — contrairement à ce que nos modèles avancent. Leurs expériences ont notamment montré qu’un système chauffe toujours plus vite qu’il ne refroidit, selon un processus appelé « relaxation thermique » — ce qui est en contradiction avec les lois de la thermodynamique. Selon les chercheurs, cet effet pourrait potentiellement être considéré comme une loi supplémentaire de la thermodynamique.
Selon les lois conventionnelles de la thermodynamique, tout système en contact avec son environnement se détend pour correspondre à la température de celui-ci et ainsi atteindre ce que l’on appelle « l’équilibre thermodynamique ». Ce processus d’adaptation, connu sous le nom de « relaxation thermique », est dû aux flux de chaleur irréversibles résultant des différences de température entre le système et son environnement. Par exemple, si l’on extrait une pièce de monnaie d’un bain d’eau glacée, celle-ci se réchauffe progressivement pour atteindre la température de l’air ambiant. À l’inverse, si cette pièce sort d’un bain d’eau bouillante, elle se refroidit jusqu’à atteindre également la température ambiante.
Si la différence de température initiale entre le système et l’environnement est mineure (c’est-à-dire que le système est proche de l’équilibre), la relaxation se produit de façon quasi linéaire. La relaxation thermique s’effectuerait également de façon symétrique, conformément à la théorie de la « thermodynamique linéaire irréversible ». Cela implique, selon nos théories actuelles, que deux systèmes chauffés et refroidis se trouvant à « équidistance » de l’équilibre thermodynamique devraient se relaxer exactement au même rythme.
Cependant, la relaxation thermique est beaucoup plus complexe lorsque les systèmes sont amenés loin de l’équilibre thermodynamique, par exemple en cas d’ébullition ou de congélation. S’ils sont loin de l’équilibre, l’hypothèse de la thermodynamique linéaire irréversible n’est pas cohérente. Des phénomènes contre-intuitifs peuvent notamment survenir selon les conditions thermiques initiales, telles qu’une relaxation anormale (ou effet Mpemba). Cette dernière se manifeste par exemple lorsque l’eau chaude gèle plus rapidement que l’eau froide, notamment dans un environnement externe extrêmement froid.
En 2020, des chercheurs de l’Institut Max Planck (MPI) pour les sciences multidisciplinaires de Göttingen (en Allemagne) et de l’Université de Grenade (en Espagne) ont suggéré que la loi de la thermodynamique conventionnelle est incomplète. Leur hypothèse est qu’à égale distance de l’équilibre thermodynamique, les petits systèmes chauffent plus vite qu’ils ne refroidissent, ce qui contredit les théories actuelles. En conséquence, une pièce gelée de quelques nanomètres ou micromètres chaufferait plus rapidement jusqu’à la température ambiante qu’une autre, chauffée et de la même taille, refroidirait jusqu’à cette même température. Leur hypothèse a été éprouvée empiriquement dans le cadre de leur nouvelle étude, récemment parue dans la revue Nature Physics.
Une relaxation thermique déséquilibrée
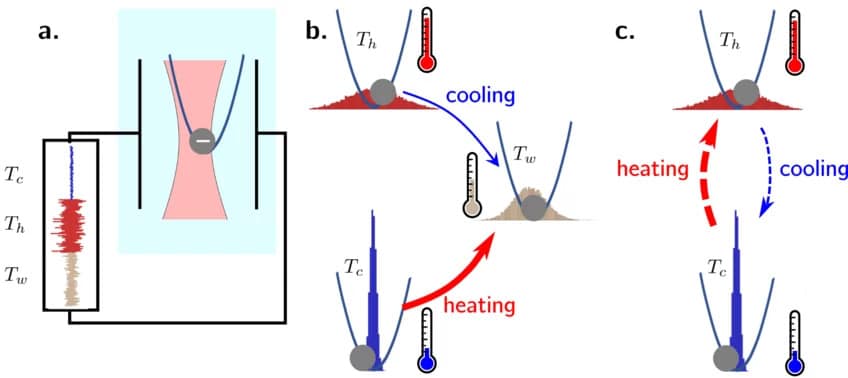
Pour éprouver leur hypothèse, les experts de la nouvelle étude ont isolé une particule de silice colloïdale piégée optiquement (par un laser) afin d’y appliquer des gradients de température (chaudes et froides) par le biais d’un champ électrique. En effet, effectuer les mesures sur une seule particule permet d’évaluer un seul micro-état, ce qui serait impossible à réaliser avec un matériau complexe composé de nombreuses particules. Un micro-état est la spécificité détaillée de la configuration microscopique d’un système. Le système passe d’un micro-état à un autre au cours de ses fluctuations thermiques. Les processus de chauffage et de refroidissement ont été répétés des dizaines de milliers de fois.
L’équipe a constaté qu’effectivement, le système chauffe et se refroidit de manière déséquilibrée et fondamentalement différente. « Si un système est préparé à deux températures, une plus froide et une plus chaude que l’environnement, choisies de telle sorte que le système soit thermodynamiquement équidistant de l’équilibre, le chemin emprunté par le système lorsqu’il se réchauffe est toujours plus long que le chemin emprunté lorsqu’il se refroidit », ont-ils expliqué dans un communiqué. Cependant, en raison de la phase rapide d’évolution initiale, le chauffage s’effectue plus rapidement que le refroidissement.


Afin d’expliquer les importants écarts observés par rapport au principe de la thermodynamique linéaire irréversible, les chercheurs proposent un nouveau cadre théorique appelé « cinématique thermique ». Cela introduit notamment de nouvelles variables, telles que la distance métrique et la vitesse thermique (le rythme auquel le système se réchauffe et se refroidit) du système par rapport à son environnement. « Entre autres choses, la nouvelle théorie révèle des écarts imprévus entre la différence de température, la distance thermodynamique et la distance thermocinématique », avancent-ils.
Cette découverte pourrait avoir d’importantes implications non seulement pour la physique, mais également pour l’étude des mécanismes biologiques tels que les réactions chimiques ou le repliement des protéines. L’effet pourrait également permettre d’améliorer l’efficacité des micromoteurs thermiques et des matériaux thermosensibles capables de s’auto-réparer. L’effet pourrait d’ailleurs être considéré comme une loi supplémentaire de la thermodynamique, complétant celle conventionnelle, indiquent les chercheurs. Cette dernière ne tient en effet pas compte de certains paramètres essentiels, tels que la vitesse thermique.


