Des chercheurs ont conçu une capsule ingérable capable d’interagir in vivo avec des bactéries intestinales, via une simple application pour smartphone et une connexion Bluetooth. Grâce à un système de signaux lumineux, un dialogue bidirectionnel s’établit entre la capsule et les micro-organismes, permettant non seulement de surveiller l’activité microbienne en temps réel, mais aussi de déclencher des interventions ciblées à la demande.
Les micro-organismes qui peuplent le tractus gastro-intestinal sont à la fois influencés par leur environnement complexe et exercent, en retour, une action notable sur la santé de leur hôte. Un nombre croissant d’études met en évidence une communication bidirectionnelle entre cette flore microbienne, le cerveau et d’autres systèmes physiologiques. Si cette interaction peut s’avérer bénéfique, certaines souches bactériennes intestinales sont également soupçonnées d’être impliquées dans des pathologies telles que la maladie de Parkinson ou les troubles du spectre de l’autisme.
Face à cette influence déterminante du microbiote intestinal sur l’organisme, la question de sa surveillance et de son contrôle devient centrale. Ces dernières années, l’ingénierie microbienne a été explorée pour détecter certains biomarqueurs ou administrer localement des composés thérapeutiques. Des recherches antérieures ont montré qu’il était possible de modifier génétiquement certaines bactéries intestinales pour qu’elles détectent des biomarqueurs inflammatoires ou des agents pathogènes.
Mais le contrôle de ces agents une fois à l’intérieur du corps reste un défi majeur, du fait de la complexité de l’environnement in vivo, qui rend difficile toute intervention dynamique. De fait, l’état des micro-organismes modifiés ne peut généralement être analysé qu’après leur expulsion des zones cibles. Autrement dit, les microagents agissent en grande partie à l’aveugle, sans possibilité de contrôle précis, ce qui limite leur efficacité.
Pour contourner ces obstacles, une équipe de l’université de Tianjin, en Chine, a mis au point un dispositif bio-optoélectronique permettant une interaction bidirectionnelle entre des bactéries intestinales modifiées et des instruments électroniques extérieurs. « Nous proposons une stratégie reposant sur des capsules optoélectroniques ingérables, permettant un dialogue bidirectionnel avec des micro-organismes génétiquement modifiés à des fins thérapeutiques contrôlables », détaillent les chercheurs dans leur étude parue lundi 28 juillet dans la revue Nature Microbiology.
Une capsule connectée par Bluetooth pour communiquer avec les bactéries intestinales
Plusieurs méthodes ont été envisagées pour contrôler in vivo des micro-organismes modifiés, notamment l’usage d’inducteurs chimiques. Mais ceux-ci, une fois dans l’organisme, ont tendance à se diffuser de manière aléatoire et à se dégrader rapidement, limitant leur efficacité. À l’inverse, les signaux lumineux présentent une stabilité et une précision spatio-temporelle bien supérieures.
Dans cette étude, les scientifiques ont modifié génétiquement une souche spécifique, Escherichia coli Nissle 1917 — une souche probiotique bien documentée pour sa capacité à coloniser l’intestin humain et généralement considérée comme sans danger. Ce micro-organisme a été conçu pour communiquer, à l’aide de signaux lumineux, avec une capsule électronique ingérable. Le tout est piloté par une application mobile, qui établit la liaison avec la capsule via le Bluetooth.
« Nous combinons une souche d’Escherichia coli Nissle 1917 modifiée par génie optogénétique, une capsule optoélectronique ingérable et un smartphone sans fil afin de créer une chaîne de traitement du signal – biologique, optique et électronique – entièrement bidirectionnelle et contrôlable par l’utilisateur », précisent les auteurs de l’étude.
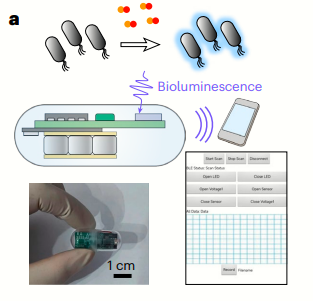
Une boucle de rétroaction contrôlée par signaux lumineux
Les bactéries ont été dotées, grâce à l’optogénétique, de la capacité à détecter un biomarqueur inflammatoire clé : le monoxyde d’azote (NO), étroitement associé à certaines pathologies intestinales comme la colite. Lorsqu’elles perçoivent des concentrations élevées de NO, un circuit génétique s’active, entraînant l’émission de lumière.
Cette bioluminescence est captée par des photodétecteurs intégrés à la capsule, qui convertissent le signal lumineux en impulsions électriques. Les photodétecteurs sont eux-mêmes reliés à un circuit imprimé, alimenté par trois piles boutons. Les signaux électriques ainsi générés sont ensuite transmis à l’application mobile, qui les interprète.
L’application peut alors initier une boucle de rétroaction : en réponse au signal reçu, la capsule active de minuscules diodes électroluminescentes (LED), qui émettent des longueurs d’onde spécifiques. Ces impulsions lumineuses viennent stimuler, à leur tour, les circuits génétiques photosensibles des bactéries, déclenchant la production d’anticorps anti-inflammatoires.
Ce système a été testé sur trois modèles porcins atteints de colite, dont les intestins avaient été colonisés par les E. coli modifiés. Dans chacun des cas, les chercheurs ont observé une production efficace d’anticorps anti-inflammatoires. « Cette approche illustre le potentiel de la biologie synthétique, associée à l’optoélectronique, pour la surveillance numérique de l’état de santé et la réalisation d’interventions ciblées », soulignent les auteurs.
À terme, cette technologie pourrait améliorer la précision des diagnostics ainsi que l’efficacité des traitements fondés sur le microbiote intestinal. Elle pourrait également être adaptée pour intégrer des boucles de communication multiples, élargissant ainsi ses applications potentielles.