L’Australie est une nation sportive. Le nombre de pratiquants, de spectateurs et d’événements sportifs bat tous les records. Football australien (footy) (1.4 million de licenciés, soit 6% de la population), courses hippiques, sports motorisés, rugby, cricket, golf, baseball, sports nautiques… Le pays offre une grande variété de sports et le gouvernement soutient le secteur de manière intensive. Mais qui dit sport, dit risque accru de blessure : l’Australie affiche aussi l’un des taux de blessures aux ligaments croisés les plus élevés au monde ! Des chercheurs de l’Université de Sydney dévoilent aujourd’hui une nouvelle technique de réparation des ligaments, pour limiter les chirurgies de révision.
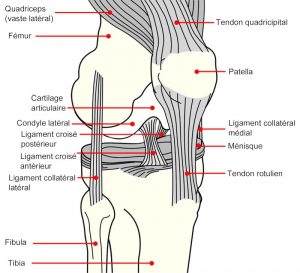
Une rupture ou déchirure du ligament croisé concerne l’un des ligaments qui se situent dans le genou. Cette articulation est particulièrement complexe, car elle doit pouvoir effectuer des mouvements très divers ; les ligaments servent à la stabiliser. Pour rappel, un tendon relie un muscle à un os, tandis qu’un ligament relie deux os dans une articulation. Si un mouvement provoque un dépassement de la tension maximale du ligament, c’est la rupture (partielle ou totale). La rupture du ligament croisé antérieur (LCA) est la blessure ligamentaire la plus courante du genou, mais aussi la blessure du genou nécessitant le plus couramment un traitement clinique.
Une alternative à des méthodes pas toujours efficaces
En Australie, aux États-Unis et dans les pays européens, la réparation des ligaments croisés est une opération fréquente, qui engendre des coûts plutôt conséquents : 1 milliard de dollars par an pour les États-Unis, et entre 200 et 250 millions de francs par an pour la Suisse, à titre d’exemple. Problème : en Australie, un quart de ces opérations nécessitent une chirurgie de révision, ce qui augmente d’autant plus les coûts de réparation.
Une équipe de chercheurs en génie biomédical de l’Université de Sydney, en collaboration avec le Regenerative Engineering Laboratory de l’Université Columbia et le FAU Erlangen-Nurnberg Institute of Medical Biotechnology (en Allemagne), propose aujourd’hui une méthode innovante pour réparer les tendons et les ligaments blessés. Ils ont en effet développé un nouveau type d’implant synthétique pour favoriser leur régénération et espèrent ainsi améliorer les résultats de la chirurgie.
Cet échafaudage synthétique est constitué d’hydrogel renforcé de fibres, une substance qui a la capacité d’imiter la structure hiérarchique du tendon humain et le tissu ligamentaire. Concrètement, les fibres de polyéthylène ont été imprégnées d’un mélange d’alcool polyvinylique et d’hydrogel. Cette technique pourrait largement pallier les défauts de la chirurgie traditionnelle : « Les méthodes conservatrices utilisant des plâtres d’immobilisation et des attelles limitant les mouvements nécessitent souvent plusieurs semaines de rééducation pour obtenir une récupération fonctionnelle minimale », précise le professeur Hala Zreiqat, directrice du centre australien de recherche en bio-ingénierie innovante et directrice de l’étude.
Elle ajoute que les implants actuels comportent un risque plus élevé de rejet et d’infection. Les greffes de tendons synthétiques ont d’ailleurs démontré une croissance tissulaire sous-optimale et une synovite – inflammation de la membrane qui borde l’articulation – due à un phénomène d’abrasion entre les fibres.
Un implant très proche du ligament humain
Imiter les propriétés physiques des ligaments humains n’est cependant pas chose aisée, comme l’explique la spécialiste : « Les tendons et les ligaments humains sont constitués à 70% d’eau ; ce sont des structures complexes qui incluent les vaisseaux sanguins, les nerfs et les vaisseaux lymphatiques, et qui ont pour tâche de relier les os aux muscles et de déplacer le corps ». De ce fait, les implants synthétiques présentent toujours un risque important de défaillance, ainsi qu’une mauvaise intégration des tissus biologiques.
Testé sur des modèles de tendons rotuliens chez le rat, l’échafaudage synthétique conçu par l’équipe du professeur Zreiqat s’est révélé, quant à lui, tout à fait efficace. Il a affiché une teneur en eau d’environ 70%, soit une valeur similaire aux tendons et ligaments humains, ce qui laisse présager d’une meilleure croissance des tissus de collagène. Les tests effectués avec un implant témoin non-imprégné d’hydrogel affichaient une teneur en eau de 50% seulement.
En outre, la résistance à la traction des microstructures synthétiques (comprise entre 77,0 et 81,8 MPa) correspondait aux capacités de traction du tendon d’Achille humain. Enfin, l’implantation in vivo des échafaudages au niveau de défauts du tendon rotulien de rat a montré une bonne croissance du tissu collagène dans ces structures après 6 semaines.
Sur le même sujet : Un nouvel hydrogel qui imite le cartilage pourrait rendre la chirurgie du genou plus simple et plus efficace
Les chercheurs espèrent maintenant étudier le comportement à long terme de ces échafaudages dans des conditions corporelles internes et externes ; ils vont notamment surveiller l’intégration tissulaire et la biomécanique dans des modèles animaux plus grands. Pour que ces échafaudages synthétiques soient bien acceptés par le corps humain, leur architecture physique et chimique doit en effet parfaitement s’aligner sur les tendons et les ligaments humains.
À terme, ils espèrent que leur technologie va permettre d’accélérer la restauration de la fonction mécanique des tendons et des ligaments et soutenir la croissance des tissus de collagène, sans compromettre la réponse biologique de l’organisme. Ce qui permettrait de satisfaire un besoin essentiel de la chirurgie orthopédique. « Dans le monde entier et en particulier en Australie, il existe un immense besoin clinique pour le développement d’échafaudages de tendons synthétiques, disponibles sur le marché et résistants mécaniquement », souligne le professeur Zreiqat.


