Une étude parue en septembre dans The Lancet Respiratory Medicine, signée par une équipe de chercheurs autrichiens, rapportait le cas d’une patiente atteinte d’une forme sévère de COVID-19, traitée avec succès avec une forme soluble de l’enzyme de conversion de l’angiotensine-2 recombinante humaine (notée hrsACE2). Depuis, d’autres essais ont confirmé le potentiel de ce traitement.
L’injection d’ACE2 soluble a entraîné une disparition rapide du virus dans le sérum sanguin, dans les cavités nasales et les poumons de la patiente, ainsi qu’une réduction de l’inflammation due aux niveaux élevés de cytokine. En outre, l’hrsACE2 n’a pas empêché la production d’anticorps neutralisants, ce qui a conduit à une amélioration clinique significative de la patiente.
L’ACE2 soluble comme récepteur compétiteur
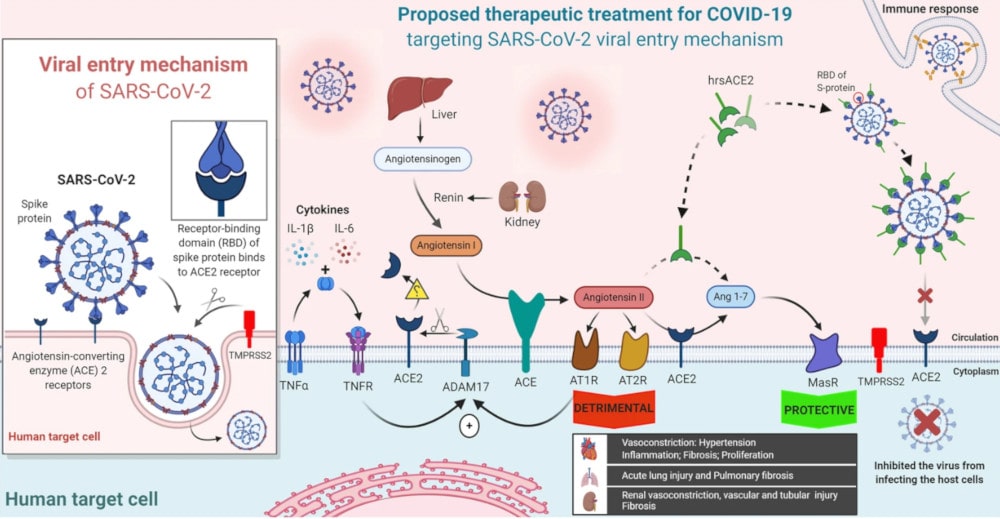
Les recherches pour élaborer un traitement et un vaccin contre la COVID-19 consistent principalement à trouver des inhibiteurs de réplication virale. Mais une autre stratégie consiste également à bloquer la cible cellulaire du SARS-CoV-2 : l’enzyme de conversion de l’angiotensine-2 (ACE2). Située à la surface des cellules, ACE2 est une protéine transmembranaire indispensable au coronavirus : ce dernier s’y fixe au moyen de sa protéine de pointe (spike), suite à quoi il peut pénétrer dans les cellules cibles pour s’y répliquer.
ACE2 est exprimée dans plusieurs organes humains, à des niveaux variables. Elle est fortement exprimée dans les poumons (à la surface des cellules épithéliales alvéolaires de type II), le cœur (sur les cellules myocardiques, les cellules endothéliales vasculaires coronaires et le muscle lisse vasculaire), les reins (sur les cellules du tubule proximal) et l’intestin grêle (sur les entérocytes). Des organes fréquemment atteints dans les formes graves de la maladie.
Alors que l’ACE2 liée à la membrane peut médier l’entrée cellulaire du SARS-CoV-2, une forme soluble génétiquement modifiée d’ACE2, appelée hrsACE2, peut limiter le phénomène en entrant en compétition avec le récepteur cellulaire. En d’autres termes, le virus vient se lier à cette forme soluble plutôt qu’au récepteur cellulaire. Ainsi, son action peut diminuer les lésions pulmonaires et le dysfonctionnement de plusieurs autres organes.
Plus tôt cette année, des études in vitro ont déjà mis en évidence le fait que hrsACE2 réduisait la croissance virale du SARS-CoV-2 d’un facteur de 1000 à 5000 en culture cellulaire, dans les vaisseaux sanguins humains modifiés et dans les organoïdes rénaux. À ce jour, le traitement à base d’hrsACE2 a été testé chez 89 volontaires sains ou atteints du syndrome de détresse respiratoire aiguë ; il s’est avéré efficace et bien toléré. Le traitement est donc particulièrement prometteur.
Le cas rapporté en septembre par le Dr Alexander Zoufaly, de l’Hôpital Kaiser-Franz-Josef à Vienne, concerne une femme de 45 ans, qui fut hospitalisée avec des antécédents de toux, de fatigue, de douleurs musculaires, de fièvre et d’essoufflement sévère depuis 7 jours ; elle souffrait également de nausée et de diarrhée depuis 4 jours. Un test PCR a confirmé qu’elle était bien atteinte de COVID-19. Elle a tout d’abord été traitée avec de l’hydroxychloroquine et un anticoagulant, la nadroparine. Mais ce traitement s’est avéré inefficace et n’a entraîné aucune amélioration clinique de l’état du patient.
Une charge virale réduite, une réponse immunitaire maintenue
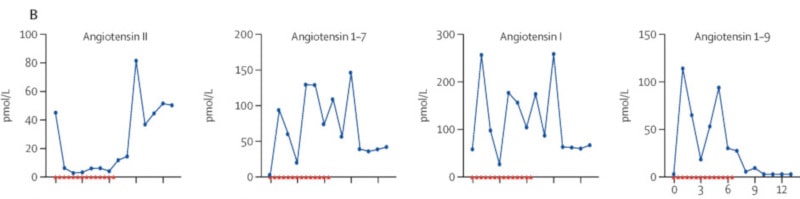
Neuf jours après l’apparition des symptômes, la patiente a reçu une dose d’hrsACE2 (pendant 5 minutes, par perfusion intraveineuse), deux fois par jour pendant 7 jours. Le produit a été bien toléré, sans aucun effet secondaire. Dès la première dose, les chercheurs ont observé une réduction notable des taux sériques d’angiotensine 2, avec augmentations concomitantes d’autres types d’angiotensine, dont l’angiotensine 1–7 et l’angiotensine 1–9 (à savoir que chaque angiotensine a un rôle biologique différent). Ces changements ont perduré tout au long du traitement.
À l’issue du traitement, l’équipe médicale a noté des diminutions marquées des concentrations de cytokines critiques impliquées dans la COVID-19 (à l’origine des « tempêtes » de cytokines). Le nombre de copies de SARS-CoV-2 a quant à lui considérablement diminué, passant de 32’000 copies par millilitre 2 jours avant le traitement, à 2500 puis 270 copies par millilitre après le premier et le deuxième jour de traitement hrsACE2 respectivement.
Par ailleurs, les chercheurs ont souligné que l’injection d’hrsACE2 n’avait pas réduit la production d’anticorps IgA et IgG anti-SARS-CoV-2. Les taux d’angiotensine II sont quant à eux revenus aux niveaux initiaux (avant traitement) dans les 48h suivant l’arrêt du traitement, ce qui correspond aux données précédemment établies sur sa demi-vie chez l’Homme. Au 57e jour, la patiente a finalement pu sortir de l’hôpital, après une amélioration significative de son état de santé.
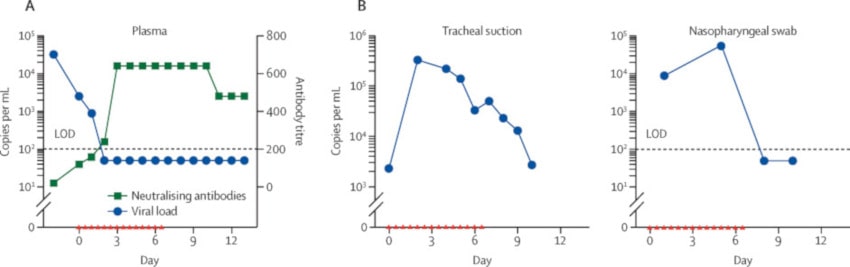


Des données similaires ont été observées chez un deuxième patient présentant des symptômes sévères de COVID-19 qui a reçu deux doses de hrsACE2 pendant 1 jour. Une réduction rapide de la charge virale dans le sérum, ainsi que la génération d’anticorps antiviraux ont aussi été détectées chez ce deuxième patient.
Face à ces observations cliniques très prometteuses, le Dr Tarek Mohamed Abd El-Aziz, du département de physiologie intégrative et cellulaire de l’University of Texas Health San Antonio, et deux collaborateurs, estiment que l’hrsACE2 pourrait véritablement être un outil thérapeutique solide. En plus de réduire la charge virale au niveau du système respiratoire, hrsACE2 semble jouer un rôle majeur dans le ralentissement, voire l’inhibition, de la propagation du virus dans les poumons et autres organes.
Reste à prouver que la diminution de la charge virale soit bien due au traitement et ne résulte pas simplement de l’évolution naturelle de la maladie. De plus, bien qu’aucun effet secondaire néfaste n’ait été rapporté, El-Aziz avertit que la réduction de la formation d’angiotensine II, due à la surexpression de l’ACE2, peut conduire à une hypotension et des lésions rénales aiguës (l’angiotensine 2 joue un rôle fondamental dans le maintien de la pression artérielle : elle entraîne notamment une vasoconstriction et la sensation de soif). Dans tous les cas, le spécialiste insiste sur le fait que l’hrsACE2 mérite de faire l’objet de recherches supplémentaires.