Le microbiote intestinal est depuis peu au coeur de la recherche dans le domaine des maladies auto-immunes. Aujourd’hui, une nouvelle étude menée par une équipe de l’University College London suggère qu’un déséquilibre du microbiote intestinal pourrait jouer un rôle majeur dans le développement de la polyarthrite rhumatoïde.
Dans une étude préclinique, les chercheurs ont constaté que les lésions de la muqueuse intestinale étaient en corrélation directe avec l’inflammation des articulations et la gravité de la maladie. Depuis quelque temps déjà, les scientifiques avaient suggéré un lien constant entre les anomalies du microbiote intestinal et la polyarthrite rhumatoïde, et l’augmentation des populations de certains types de mauvaises bactéries a souvent été associée à la gravité de la maladie.
Un mécanisme encore peu compris
Cependant, la manière exacte dont les bactéries intestinales peuvent influencer l’inflammation des articulations n’est pas encore claire. Plusieurs mécanismes ont été envisagés, allant des bactéries intestinales modulant le développement des cellules inflammatoires spécifiques responsables de l’arthrite à des métabolites bactériens particuliers contribuant à la gravité de la maladie.
Cette nouvelle étude examine une autre hypothèse causale, en se concentrant sur les liens entre la gravité de l’arthrite et l’affaiblissement de la paroi intestinale induit par les bactéries. Les résultats ont été publiés dans la revue Med.
« Nous voulions savoir ce qui se passait dans l’intestin et si les modifications de la paroi intestinale – qui agit habituellement comme une barrière pour protéger l’organisme des bactéries – sont une caractéristique de la maladie et contribuent à son développement », explique Claudia Mauri, co-auteure principale.
Des résultats préliminaires chez la souris avaient montré que les spécimens élevés pour présenter une prédisposition génétique à la perméabilité intestinale développaient également des signes d’arthrite grave. Un autre modèle de souris, conçu pour développer une arthrite induite par le collagène, présentait un gonflement articulaire réduit lorsque la perméabilité intestinale était améliorée.
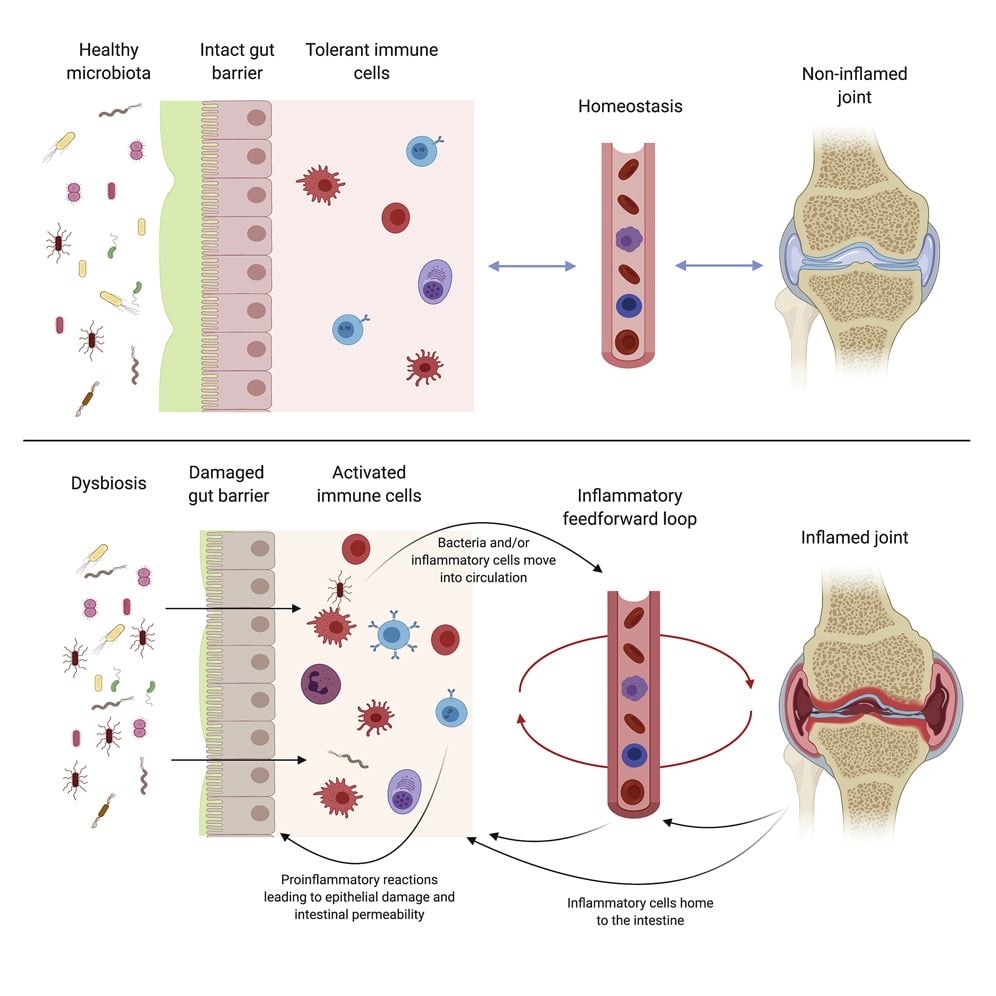
En examinant les patients humains, les chercheurs ont constaté que ceux qui souffraient de polyarthrite rhumatoïde présentaient des taux sanguins plus élevés de lipopolysaccharide (LPS), de protéine de liaison au LPS (LBP) et de protéine de liaison aux acides gras intestinaux. Toutes ces molécules sont des biomarqueurs connus des lésions intestinales, et les niveaux de LBP semblent particulièrement liés à la gravité de la maladie.
Une cible thérapeutique prometteuse
« Les chercheurs de l’University College de Londres ont montré que, dans l’arthrite, la muqueuse intestinale est profondément endommagée et ne fonctionne plus correctement comme barrière, et qu’il y a une accumulation dans l’intestin de globules blancs qui provoquent l’inflammation », peut-on lire dans le document d’étude. « Les auteurs montrent que, dans l’arthrite, les bactéries traversent la frontière interdite de la muqueuse intestinale et que la réparation des défauts de perméabilité intestinale avec des médicaments spécifiques inhibe l’inflammation articulaire ».
Malheureusement, ces travaux ne permettent pas encore d’expliquer complètement la chaîne de mécanismes qui lie cet affaiblissement de la paroi intestinale à la polyarthrite. Ainsi, bien que la modulation du degré de perméabilité intestinale se soit avérée directement liée à l’inflammation articulaire, il reste encore des chaînons manquants dans cette relation, qui n’ont pas encore été décrits.
Mauri précise toutefois que ces résultats indiquent que l’intestin pourrait être une cible thérapeutique utile. Elle pense notamment que l’amélioration de la perméabilité intestinale pourrait constituer un nouveau modèle de traitement efficace. « Nos résultats suggèrent que la muqueuse intestinale est une cible thérapeutique », déclare Mauri.
« Fait important, nous avons constaté que l’utilisation de médicaments existants qui restaurent l’intégrité de la barrière intestinale, c’est-à-dire qui empêchent l’intestin de devenir perméable ou qui inhibent le déplacement des cellules inflammatoires vers et depuis l’intestin, pouvait réduire la gravité de la polyarthrite dans les modèles précliniques », conclut-elle.