Lors de transplantations, la compatibilité des groupes sanguins entre donneur et receveur est cruciale pour éviter tout rejet de l’organe. Mais il est difficile de trouver des donneurs compatibles et les listes d’attente s’allongent, le risque pour les receveurs étant de ne pas être greffés à temps. Des scientifiques canadiens ont récemment tenté une approche visant à éliminer ce problème, en « convertissant » des poumons fonctionnels du groupe sanguin A vers le groupe O, les rendant potentiellement acceptables par n’importe quel receveur en attente de greffe. Cet exploit est le résultat de l’action de deux enzymes particulières.
Récemment, la première greffe sur un homme d’un cœur de porc génétiquement modifié a été couronnée de succès. Cette prouesse technologique se voulait la solution aux écueils rencontrés pour la plupart des demandes de greffes : l’absence de donneur compatible.
Que ce soit pour les transfusions ou les greffes, la compatibilité entre groupes sanguins est obligatoire. Même si la composition du tissu sanguin est la même pour tous, les différents éléments du sang portent à leur surface des marques d’identité individuelle. Il s’agit de molécules, les antigènes, qui varient d’une personne à l’autre.
Les antigènes en cause
L’appariement des groupes sanguins ABO, déterminés par la présence d’antigènes A et B à la surface des globules rouges, est donc une condition préalable aux transplantations. Le sang de type A contient l’antigène A, le sang de type B contient l’antigène B, le sang de type AB contient les deux antigènes et le sang de type O n’en contient aucun. Les antigènes sont également exprimés dans des vaisseaux et des organes solides. Si l’on greffe au malade un composant sanguin d’un groupe non compatible, son système immunitaire le considérera comme étranger, les antigènes induisant le rejet du composant sanguin et une aggravation potentielle de l’état du malade.
Le groupe O, ne comportant aucun antigène, est considéré comme donneur universel. Cependant, les donneurs universels peuvent uniquement recevoir des composants sanguins du groupe O. En conséquence, les patients de type O attendent « en moyenne deux fois plus longtemps pour recevoir une transplantation pulmonaire que les patients de type A », précise le Dr Aizhou Wang, premier auteur de l’article, dans un communiqué, ajoutant que « leur risque de décès est 20% supérieur ».
L’idée de l’équipe de recherche était de transformer le groupe sanguin originel de l’organe du donneur en groupe universel (O). Ce projet a été rendu possible grâce à des efforts interdisciplinaires dans plusieurs organisations au Canada, y compris l’UHN, l’Université de Toronto, l’Université de la Colombie-Britannique et l’Université de l’Alberta. Toronto est une place forte pour la greffe pulmonaire. En effet, l’Hôpital général de Toronto a réalisé la première transplantation pulmonaire au monde en 1983. La première double transplantation pulmonaire s’y est aussi déroulée, en 1986.
Des enzymes intestinales, clés de l’universalité
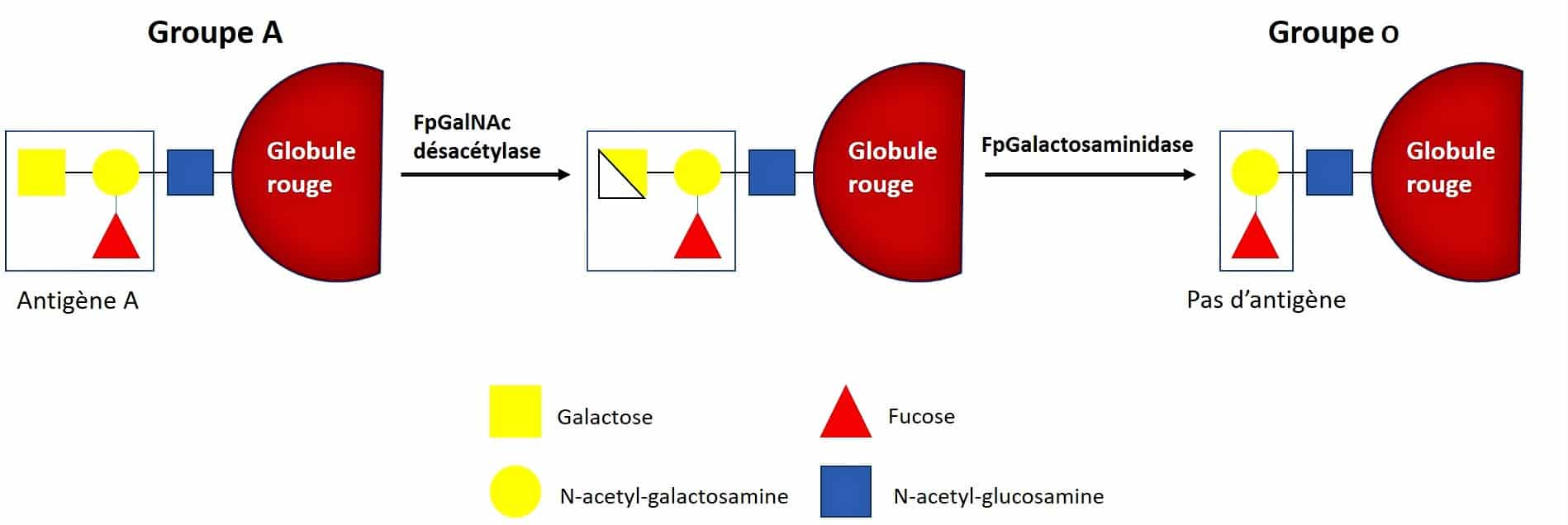
Dans une étude antérieure, Stephen Withers, PhD, professeur de biochimie à l’Université de Colombie-Britannique, avait identifié deux enzymes bactériennes des parois intestinales (FpGalNAc désacétylase et FpG alactosaminidase) qui, lorsqu’elles sont utilisées ensemble, convertissent efficacement les globules rouges du groupe A en groupe O, créant ainsi un sang universel.
« Ce groupe d’enzymes, que nous avons trouvé dans l’intestin humain, peut couper les sucres des antigènes A et B sur les globules rouges, les convertissant en cellules universelles de type O », déclare S. Withers. « Cela a ouvert une passerelle pour créer des organes universels de type sanguin O ».
Wang et al. ont donc utilisé ces deux enzymes pour éliminer l’antigène A des poumons de donneurs humains à l’aide d’une perfusion pulmonaire ex vivo (EVLP). Les travaux ont été publiés dans la revue Science Translational Medicine. Dans un premier temps, ils ont mené une série d’expériences sur des échantillons de globules rouges et d’aorte. Dans un second temps, ils ont testé le procédé sur des poumons humains ne pouvant pas être utilisés pour une greffe.
Le système EVLP (Ex Vivo Lungs Perfusion) est développé au Canada depuis une quinzaine d’années, afin de donner aux médecins le temps de « soigner » les greffons avant leur transplantation. Car, outre le fait de la comptabilité des groupes sanguins, la survie du greffon n’est pas toujours possible, suite à la greffe. Sans compter que, le fait même de transplanter peut provoquer des microlésions pulmonaires. Certains poumons, malgré leur compatibilité, sont jugés irrecevables. L’EVLP tend à maximiser les donneurs potentiels en préparant au mieux les greffons et en les améliorant. Pour ce faire, l’EVLP les réchauffe à 37 °C et les « alimente » avec une solution optimisée (contenant des nutriments). Ils sont ventilés de manière protectrice. Ce protocole a une durée maximale de quatre heures, puis les poumons sont évalués pour la greffe. Dans le cas de l’étude, la solution optimisée comprenait les deux enzymes particulières.
Un poumon a été traité, pendant quatre heures, avec le groupe d’enzymes afin d’ôter les antigènes de sa surface. À la fin du traitement, jusqu’à 97% de l’antigène A avaient été éliminés. Les chercheurs n’ont pas observé de toxicité aiguë liée à la procédure dans les organes et aucun changement manifeste de la santé pulmonaire. Le second poumon, du même donneur, n’a pas subi de traitement.
L’équipe a ensuite testé chacun des poumons en ajoutant du sang de type O (avec de fortes concentrations d’anticorps anti-A) au circuit EVLP, pour simuler une greffe ABO incompatible. Les résultats ont démontré que les poumons traités étaient bien tolérés tandis que ceux non traités montraient des signes de rejet.
Marcelo Cypel, l’un des auteurs de l’étude, chirurgien et directeur du centre de greffe d’Ajmera à l’université Health Network (Toronto), déclare : « Avoir des organes universels signifie que nous pourrions éliminer la barrière de l’appariement sanguin et prioriser les patients par urgence médicale, sauvant plus de vies et gaspillant moins d’organes. Ça va être une sacrée révolution ! ».


Ces résultats montrent que la déplétion de l’antigène A pulmonaire du donneur peut être obtenue avec un traitement EVLP. Cette stratégie a le potentiel d’étendre la transplantation pulmonaire ABO incompatible. Mais il reste du chemin avant d’en arriver là. Il faudra démontrer, dans un premier temps, par des essais cliniques sur des animaux, que la transplantation de ce genre d’organe fonctionne, et ceci sans danger. Les chercheurs ont pour objectif de demander l’autorisation d’essais cliniques sur l’Homme d’ici un an et demi. Ensemble, ces résultats ont le potentiel d’améliorer l’équité dans l’attribution des poumons pour la transplantation.