Une équipe internationale, dirigée par des chercheurs de l’IBM Research Lab de Zürich (Suisse), a développé une méthode permettant de contrôler la sélectivité des réactions chimiques. Leur approche repose sur la formation et la dissociation réversibles et sélectives de liaisons atomiques, induites par une pointe de microscope à effet tunnel. Cette avancée pourrait non seulement permettre d’initier des réactions chimiques avec une résolution spatiale et temporelle sans précédent, mais aussi de découvrir des réactions complètement nouvelles.
Pour créer des molécules ou des machines moléculaires complexes, il faut réunir et connecter de manière précise un ensemble d’atomes. Ceci consiste à mélanger des réactifs, à éventuellement stimuler la réaction au moyen d’un catalyseur, puis à récupérer les produits avec des rendements plus ou moins intéressants. Et s’il était possible de contrôler à volonté des molécules simples et des liaisons chimiques ? C’est l’objectif ultime du projet MolDAM (Single Molecular Devices by Atom Manipulation), lancé par IBM Research il y a deux ans.
Concrètement, il s’agit de construire de la matière « sur mesure » à partir d’atomes individuels en contrôlant les réactions chimiques avec la pointe d’un microscope à sonde à balayage. À l’aide d’impulsions lumineuses ultrarapides, les scientifiques ont observé comment se forment les liaisons et comment les atomes se réarrangent au cours d’une réaction chimique. Aujourd’hui, en appliquant une tension spécifique aux liaisons atomiques, le Dr Florian Albrecht d’IBM Research Europe et ses co-auteurs ont réussi à créer trois produits différents à partir de la même molécule.
Trois nouvelles molécules créées à partir d’une seule
La sélectivité et le rendement des réactions chimiques peuvent être améliorés en ajustant certains paramètres (température, pH, etc.) ou en régulant les donneurs de protons disponibles — ce qui permet d’influer sur la façon dont les atomes échangent des électrons pour former des liaisons. « Par ces moyens, cependant, les conditions de réaction sont modifiées à un tel degré que les mécanismes de base régissant la sélectivité restent souvent insaisissables », notent les chercheurs dans leur étude.
Ils ont donc entrepris de contrôler la formation de liaisons atomiques d’une tout autre manière. Ils ont tout d’abord synthétisé une molécule de 5,6,11,12-tétrachlorotétracène (C18H8Cl4) — une molécule composée d’une rangée de quatre cycles carbonés, auxquels sont liés quatre atomes de chlore — puis l’ont absorbée sur une fine couche de sel cultivée sur du cuivre. Grâce à des impulsions de tension produites par la pointe d’un microscope à effet tunnel (ou STM, pour scanning tunneling microscope) ils ont éliminé les atomes de chlore, brisant de ce fait quatre liaisons C-Cl et la liaison C-C centrale.
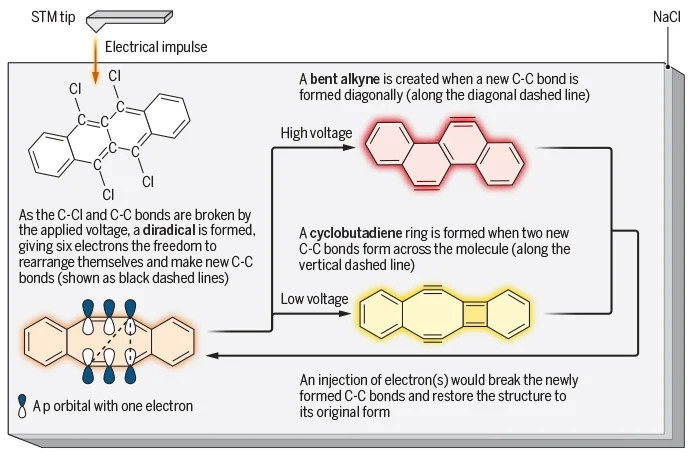
Cette intervention a produit une molécule intermédiaire contenant un diradical — un cycle central de 10 atomes de carbone, dont six dotés d’un électron non apparié (et donc aptes à former de nouvelles liaisons). En appliquant une tension relativement élevée, ils ont forcé l’établissement d’une nouvelle liaison C-C, menant à la formation d’un nouveau cycle, appelé alcyne coudé ; la molécule initiale se transforme alors en une nouvelle molécule composée de quatre cycles.
À noter que le système est conçu de manière à ce que les électrons non appariés restants ne puissent pas se reconnecter pour créer une autre liaison C-C, comme cela se produirait normalement. L’application d’une tension plus faible à la molécule intermédiaire a quant à elle conduit à la formation d’un nouveau cycle à quatre atomes de carbone, appelé cyclobutadiène, au sein de la molécule. L’obtention de ces différents réseaux carbonés n’aurait pas été possible via la chimie traditionnelle.
Une chimie plus sélective et réversible
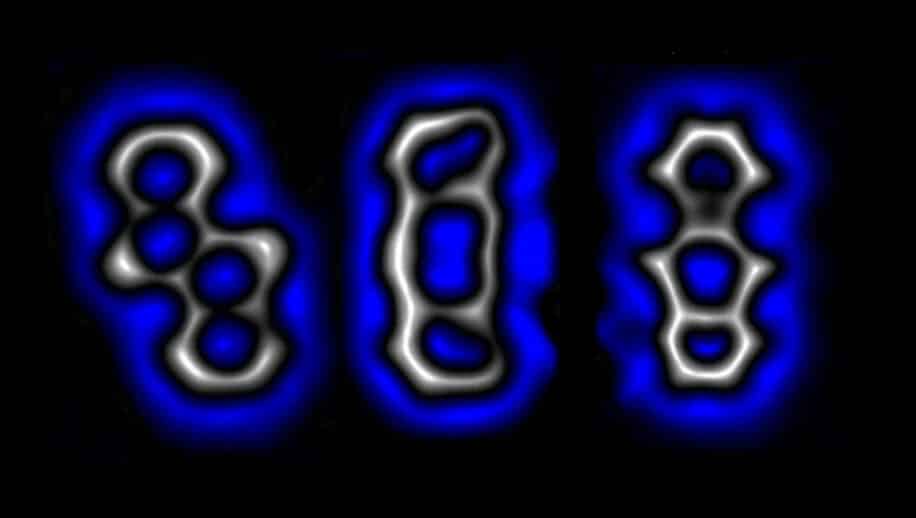
Au total, l’équipe a donc transformé la molécule initiale en trois produits distincts. « Le potentiel d’interaction avec un ensemble différent de partenaires fait de ce système moléculaire polymorphe un couteau suisse doté de trois outils chimiques distincts et utiles », écrivent Igor Alabugin et Chaowei Hu dans un article accompagnant l’étude. Chacun des produits formés est capable de remplir une fonction chimique différente, comme servir de site de liaison aux métaux de transition ou participer à des réactions d’oxydoréduction. Les trois pourraient même être utilisés comme portes logiques dans l’électronique moléculaire.
Gros avantage de la méthode : ces réactions peuvent être inversées avec des impulsions de polarité opposée ; chaque produit a en effet pu revenir à son état d’origine via une nouvelle impulsion d’électrons. En forçant ainsi une seule molécule à adopter différentes formes (ou isomères), via l’application de tensions et de courants précis, les chercheurs peuvent observer directement le comportement des électrons et déterminer les configurations optimales des composés organiques selon le résultat souhaité.
À noter que cette expérience a été menée dans des conditions cryogéniques (à -268° C), une température à laquelle les atomes et molécules sont quasiment immobiles. La reproduction de la méthode à une température proche de la température ambiante pourrait s’avérer plus difficile. Par ailleurs, certaines liaisons atomiques pourraient être bien plus difficiles à briser.
Ces travaux ouvrent toutefois la voie à un contrôle plus précis des réactions chimiques — du moins dans certains cas — et éclairent les mécanismes sous-jacents aux réactions d’oxydoréduction. Cela pourrait par exemple mener au développement de catalyseurs capables de diriger la réaction dans une direction bien spécifique. « Les réactions sélectives à une seule molécule induites par la pointe améliorent notre compréhension de la chimie redox et pourraient conduire à de nouvelles machines moléculaires », concluent les chercheurs.


 L’électron est une particule élémentaire qui, avec les protons et les neutrons, constitue les atomes. C’est donc l’un des composants principaux de la matière baryonique. À ce titre, il revêt... [...]
L’électron est une particule élémentaire qui, avec les protons et les neutrons, constitue les atomes. C’est donc l’un des composants principaux de la matière baryonique. À ce titre, il revêt... [...]