Des scientifiques ont pu éliminer des métastases chez des souris en les transformant en cellules graisseuses. Les premières applications cliniques pourraient s’effectuer rapidement, les traitements utilisés étant déjà approuvés sur le marché.
Une équipe de l’Université de Bâle en Suisse, spécialisée dans le traitement du cancer, a travaillé sur une voie de signalisation appelée transition épithélio-mésenchymateuse (TEM). Elle intervient lors des cicatrisations, ainsi que lors du développement du fœtus, pour transformer des cellules épithéliales en cellules mésenchymateuse, un type de cellule souche qui pourra par la suite se différencier en un autre type de cellule selon les besoins de l’organisme.
Or, cette voie, comme son inverse (la transition mésenchymato-épithéliale ou TME) est aussi activée dans les cellules cancéreuses. Cette dernière leur permet de se répandre dans tout le corps pour former des métastases.
Pour leur recherche, les chercheurs ont implanté une forme agressive du cancer du sein humain sur des souris, et les ont traitées avec deux médicaments : la rosiglitazone, utilisée par les diabétiques, et le trametinib, déjà employé pour traiter le cancer.
Lorsqu’une cellule cancéreuse active la voie de la TEM ou TME après administration des 2 médicaments, elle ne se propage pas dans le corps, mais active l’adipogenèse, c’est-à-dire sa différenciation en cellule adipeuse (ou graisseuse).
« Les modèles utilisés dans cette étude ont permis d’évaluer la dissémination de l’adipogenèse des cellules cancéreuses dans l’environnement tumoral », déclare le groupe dans son étude, publiée cette semaine. « Les résultats indiquent que, dans un contexte adapté au patient, une thérapie combinée à base de rosiglitazone et de trametinib cible spécifiquement les cellules cancéreuses présentant une plasticité accrue et induit leur adipogenèse ».
Le traitement agit comme ceci : le trametinib stimule davantage le processus de transformation des cellules cancéreuses en cellules souches, et également leur différenciation en cellules adipeuses, tandis que la rosiglitazone joue un rôle un peu plus secondaire, mais aide le trametinib à convertir les cellules souches en cellules adipeuses.
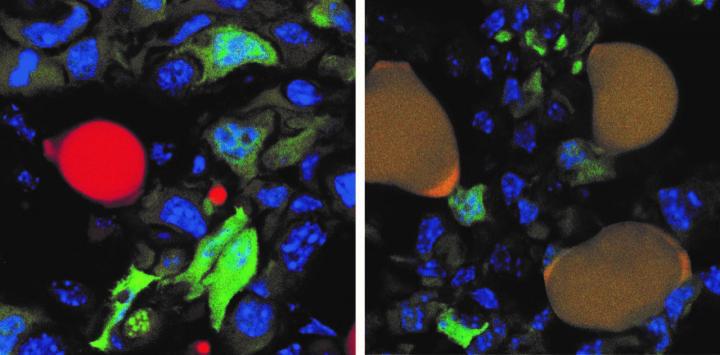
Cependant, cette combinaison de médicaments ne fonctionne pas sur la totalité des cellules cancéreuses présentes, ce qui signifie également que la thérapie a été un échec pour certaines souris, qui n’ont pas survécu. Mais les cellules converties en adipocytes ne redevenaient jamais cancéreuses, et les chercheurs espèrent que des essais cliniques sur les humains montreront également des résultats positifs, étant donné qu’ils ont travaillé sur des cellules humaines.
À lire aussi : Transplantation d’organes : une donneuse transmet son cancer du sein à quatre receveurs
L’avantage pour les futures études sur le traitement, est que les deux médicaments sont déjà approuvés par la FDA, ce qui facilitera dans un avenir certainement proche les accords pour des tests cliniques (sur des humains).
Mais en attendant l’approbation pour cette étape, l’équipe est en train d’étudier si le traitement, combiné à une chimiothérapie, ne pourrait pas supprimer plus efficacement les cellules cancéreuses, et aussi permettre d’agir sur d’autres types de cellules.
« L’évaluation clinique de l’effet répressif du traitement sur les métastases expérimentales du cancer du sein et, par conséquent, de son potentiel dans le traitement du cancer du sein de stade 4, nécessitera des associations adjuvantes avec une chimiothérapie dans des modèles précliniques avancés », explique l’équipe.
« Puisque nous avons utilisé des médicaments approuvés par la FDA pour étudier l’effet préclinique du traitement, une application clinique peut être possible », concluent-ils.