Tout comme un atome, une molécule peut perdre ou gagner des électrons, modifiant ainsi sa charge électrique globale. Ces phénomènes de modification de la charge électrique jouent un rôle crucial dans le transfert d’énergie moléculaire régissant certains processus catalytiques et biochimiques. Pour la première fois, des chimistes ont réussi à observer en temps réel la modification structurelle de molécules, dues à des transitions de charge électrique. Des résultats qui devraient aider à mieux comprendre divers processus biologiques essentiels.
En utilisant certaines des technologies de microscopie les plus avancées au monde, les chimistes ont capturé des images de molécules modifiant leur charge électrique en temps réel. Pour ce faire, ils ont ajouté et enlevé des électrons, observant directement les modifications de la structure de quatre molécules. Les résultats ont été publiés dans la revue Science.
Les changements moléculaires de charge électrique sont connus depuis longtemps, mais il s’agit ici de la première observation directe du phénomène. Cela pourrait nous aider à mieux comprendre plusieurs processus moléculaires, notamment les réactions chimiques, la catalyse et le transport de charges, voire même des processus biologiques.
« Nous avons pu résoudre avec une résolution sans précédent les changements structurels de molécules individuelles » explique le chimiste Leo Gross d’IBM Research-Zurich. « Cette nouvelle compréhension dévoile certains des mystères des relations charge-fonction moléculaires en ce qui concerne la manière dont la biologie convertit et transporte de l’énergie ».
Un microscope à force atomique pour observer les transitions de charge électrique moléculaire
L’équipe a utilisé la microscopie à force atomique. La pointe laser balaye la surface des structures à étudier, détectant tous les changements structurels, même les plus faibles. Ceux-ci sont enregistrés pour créer une image de ce que la sonde numérise. De cette manière, les scientifiques peuvent obtenir une image des éléments trop petits pour être vus par des moyens optiques.
Ainsi, quatre types de molécules — l’azobenzène, le pentacène, le tétracyanoquinodiméthane (TCNQ) et la porphine — ont été examinés au microscope dans une enceinte sous vide froid, afin de s’assurer qu’aucune influence extérieure ne modifierait les résultats. Une seule molécule a été placée sur un film de chlorure de sodium, puis une petite tension a été envoyée à travers la sonde pour transférer des électrons à la molécule, un à la fois.
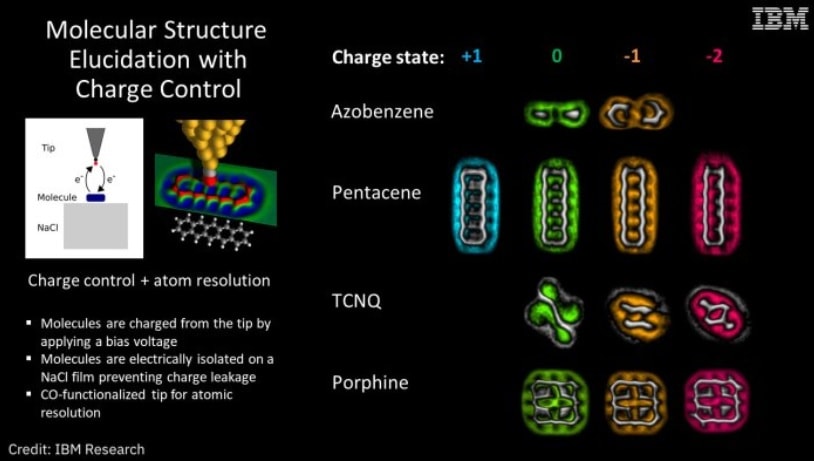
Gross et ses collègues avaient déjà mis au point cette technique de contrôle de la charge et l’ont décrite dans une étude en 2015. Ils ont également décrit leur technique d’imagerie en 2009. Dans ce nouveau travail, l’équipe a cependant trouvé un moyen de combiner les deux techniques pour imager les molécules et contrôler la charge en même temps.
Ils ont imagé les quatre molécules dans au moins deux de ces quatre états : positif (moins un électron), neutre (le même nombre de protons et d’électrons), négatif (plus un électron) et double négatif (plus deux électrons). Les quatre molécules ont réagi différemment aux changements de charge.
Sur le même sujet : Des molécules ont été contrôlées individuellement pendant quelques femtosecondes
Cette vidéo montre comment la molécule de porphine se transforme à mesure qu’elle perd des électrons dans ces conditions contrôlées :
Transition de charge moléculaire et processus biologiques fondamentaux
La molécule d’azobenzène est devenue physiquement tordue. Avec le pentacène, les zones de la molécule sont devenues plus réactives en raison des électrons supplémentaires. Le changement de charge a entraîné un changement du type de liaisons entre les atomes de TCNQ, qui s’est déplacé physiquement sur le film. Et dans la porphine, ce n’était pas seulement le type de liens, mais aussi leur longueur qui changeait.
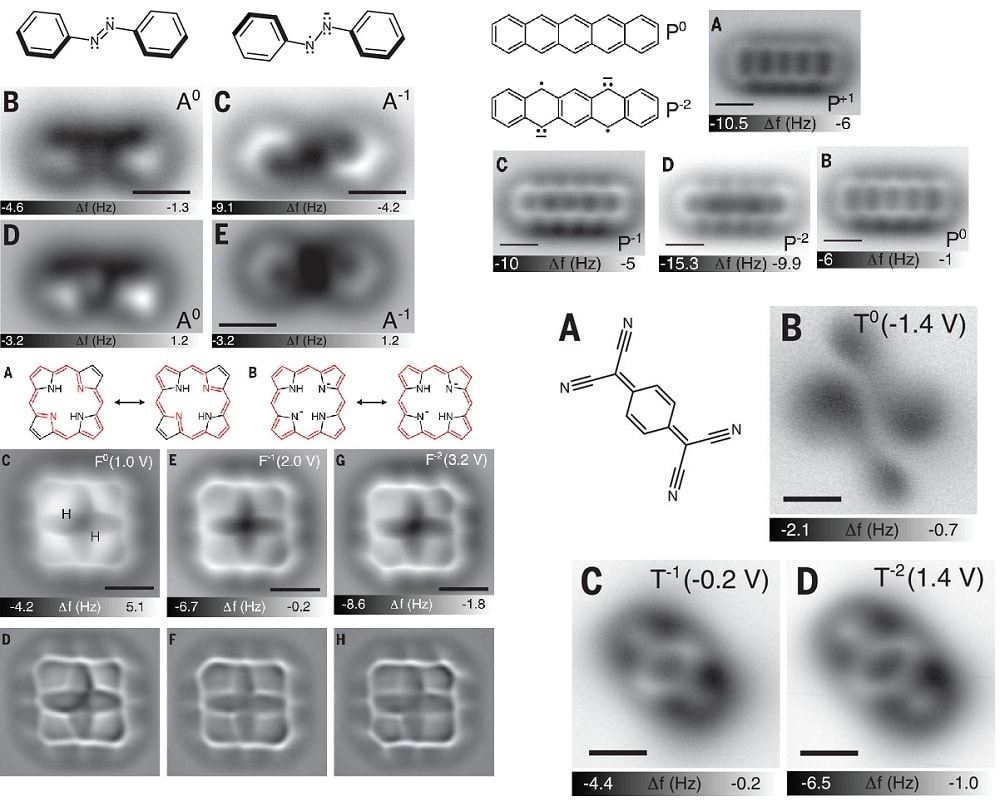
Ces résultats aideront à mieux comprendre le transfert d’énergie moléculaire. Plus précisément, examiner de si près les molécules de porphine pourrait nous aider à mieux comprendre certains processus biologiques fondamentaux, car la porphine est le composé de base des porphyrines, un groupe de composés organiques qui composent à la fois la chlorophylle et l’hémoglobine.
« Les transitions de charge de ces molécules sont essentielles à la vie. Grâce à notre nouvelle technique, nous pouvons mieux comprendre en quoi la charge modifie la structure et le fonctionnement des molécules, qui jouent un rôle essentiel à de nombreux égards, telles que la photoconversion et le transport d’énergie dans les organismes vivants » conclut Gross.


 L’électron est une particule élémentaire qui, avec les protons et les neutrons, constitue les atomes. C’est donc l’un des composants principaux de la matière baryonique. À ce titre, il revêt... [...]
L’électron est une particule élémentaire qui, avec les protons et les neutrons, constitue les atomes. C’est donc l’un des composants principaux de la matière baryonique. À ce titre, il revêt... [...]