Un tube digestif vieillissant produit des molécules spécifiques affaiblissant l’activité de l’axe intestin-cerveau et provoquant un déclin cognitif lié à l’âge, révèle une expérience chez les souris. Ces molécules sont produites par une souche bactérienne particulièrement répandue chez les animaux âgés, mettant en lumière l’implication du microbiote intestinal dans le processus de vieillissement.
Si le déclin cognitif lié à l’âge est habituellement associé au vieillissement et à la dégénérescence cérébrale, des études ont démontré des associations avec des processus se produisant ailleurs dans l’organisme. En particulier, le microbiote intestinal est apparu au cours des dernières décennies comme un important régulateur cognitif, notamment par le biais de l’axe intestin-cerveau.
Des recherches ont par exemple montré que le microbiote intestinal peut affecter l’apprentissage, la mémoire et le comportement. Sa dérégulation est associée à des pathologies neurodégénératives affectant généralement les personnes âgées telles que la maladie d’Alzheimer et la maladie de Parkinson.
Cependant, les mécanismes par lesquels le microbiote intestinal influence l’axe intestin-cerveau et peut moduler le déclin cognitif lié à l’âge demeurent largement incompris, la littérature scientifique présentant de nombreux résultats contradictoires. La manière dont les interventions ciblant le microbiote pourraient potentiellement permettre d’inverser ce déclin est donc encore incertaine.
Une étude codirigée par l’Université de Pennsylvanie et l’Université de Stanford décrit une voie microbiote-intestin-cerveau qui influencerait le rythme du déclin cognitif. « Dans nos nouveaux travaux publiés aujourd’hui dans Nature, nous avons découvert que le tube digestif vieillissant produit des molécules spécifiques qui atténuent l’activité d’une voie neuronale clé entre l’intestin et le cerveau, entraînant un déclin cognitif lié à l’âge chez les souris », expliquent les chercheurs dans un communiqué de l’Arc Institute, qui a également contribué aux travaux.
Une bactérie spécifique associée au déclin lié à l’âge
Pour décrypter le lien entre le microbiote intestinal et le déclin cognitif, l’équipe de la nouvelle étude a modifié le microbiote de jeunes souris soit en les faisant cohabiter avec des souris âgées, soit en les nourrissant avec leurs excréments. Les tests de mémoire ont été effectués en comparant par exemple le temps que les animaux mettent pour explorer de nouveaux endroits et celui qu’ils mettent à explorer ceux qu’ils connaissent déjà.
Les souris exposées au microbiote intestinal de souris âgées ont obtenu de moins bons résultats aux tests de mémoire que celles non exposées. Leur capacité semblait cependant s’être rétablie après l’administration d’antibiotiques, suggérant une implication significative du microbiote intestinal. Les souris âgées traitées avec des antibiotiques présentaient également moins de troubles de la mémoire.
Parmi les nombreuses espèces bactériennes intestinales dont l’abondance augmentait chez les souris âgées, les chercheurs se sont particulièrement concentrés sur les Parabacteroides goldsteinii, dont l’abondance est connue pour augmenter avec l’âge. L’administration de la bactérie seule à des souris dont le microbiote intestinal avait été éliminé entraînait un déficit de mémoire par rapport aux animaux témoins. En revanche, l’administration de plusieurs autres espèces bactériennes ne provoquait pas le même effet.
D’autre part, l’élimination du microbiote semblait associée à un déclin cognitif ralenti avec l’âge, par rapport aux souris dont le microbiote vieillissait normalement. « L’ensemble de ces résultats suggère qu’un composant ou un sous-produit du microbiote vieillissant contribue au processus de perte de mémoire », indiquent les chercheurs.
Les effets de la bactérie sur le déclin cognitif seraient attribués à des métabolites qu’elle produit : des acides gras à chaîne moyenne (AGCM). Les analyses de l’équipe ont montré que les taux d’AGCM augmentent avec l’âge proportionnellement à la prolifération de P. goldsteinii. Ces composés activent les cellules immunitaires myéloïdes intestinales, ce qui induit à son tour la production de molécules de signalisation inflammatoires. La IL-1β, l’une de ces molécules proinflammatoires, altère la fonction des neurones sensoriels vagaux.
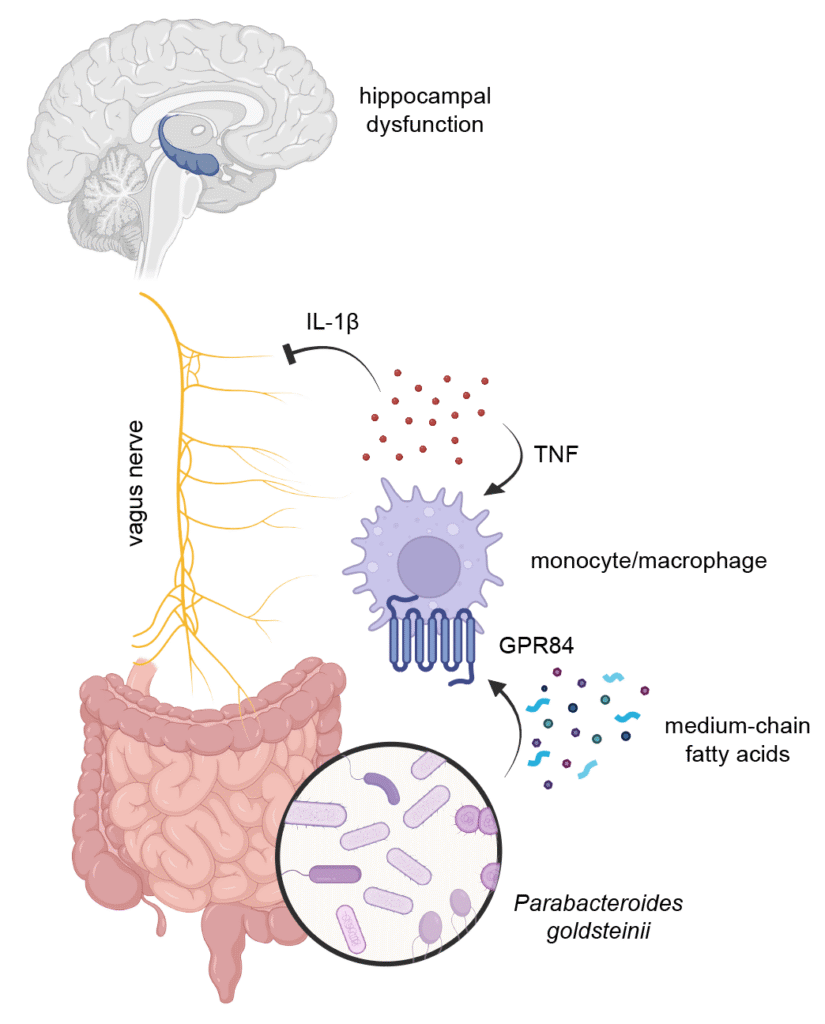
Une cascade inflammatoire impactant la mémoire
Pour étayer leurs observations, les chercheurs ont effectué une autre expérience où les souris ont été nourries avec des AGCM. Cela a provoqué une diminution de l’activité du nerf vague, ainsi qu’une activité réduite de l’hippocampe, la région du cerveau impliquée dans l’apprentissage et la mémoire.
« C’est un véritable tour de force », a indiqué à la revue Science, Haijiang Cai, neuroscientifique à l’Université d’Arizona, spécialiste de la communication intestin-cerveau et qui n’a pas participé à ces travaux. « Ils ont défini l’ensemble du processus, du vieillissement aux bactéries… jusqu’aux fonctions cognitives ; c’est vraiment impressionnant. »
À noter toutefois que la mesure dans laquelle ces résultats pourraient être transposés aux humains reste à déterminer. En outre, si des études antérieures ont identifié un lien entre le vieillissement en bonne santé et une abondance réduite de bactéries apparentées à Parabacteroides, de nombreux autres microorganismes et métabolites intestinaux pourraient aussi influencer l’axe intestin-cerveau.
Vidéo de présentation de l’étude :