Des chercheurs ont découvert que le cuivre, en tant que catalyseur, pouvait potentiellement transformer le dioxyde de carbone en produits chimiques et en carburants durables, sans produire aucun sous-produit inutile, créant ainsi une alternative écologique à la fabrication actuelle de produits chimiques.
Durant des décennies, les scientifiques ont recherché des moyens efficaces d’éliminer les émissions excessives de dioxyde de carbone dans l’air et de les recycler dans des produits tels que les carburants renouvelables. Cependant, convertir le dioxyde de carbone en produits chimiques utiles est une tâche fastidieuse, coûteuse et peu rentable. Et, de ce fait, non viable économiquement ou écologiquement.
Mais à présent, une découverte effectuée par des chercheurs du Lawrence Berkeley National Laboratory (Berkeley Lab) et du Joint Center for Artificial Photosynthesis (JCAP), démontre que le recyclage du dioxyde de carbone en produits chimiques et en combustibles peut être économique et efficace, le tout grâce à un catalyseur de cuivre unique.
Vous aimerez également : Écologie ; l’ONU souhaite que l’Afrique s’inspire du Maroc
Lorsque vous prenez un morceau de cuivre, il peut vous sembler lisse au toucher, mais au niveau microscopique, sa surface est bosselée : ces bosses sont ce que les scientifiques appellent des « sites actifs », a déclaré Joel Ager, chercheur au JCAP, qui a dirigé l’étude. Ager est également membre du personnel scientifique de la division Science des matériaux du Berkeley Lab, et professeur auxiliaire au département Science et génie des matériaux de l’Université de Berkeley.
Ces sites actifs sont le lieu où la « magie » de l’électrocatalyse se produit : les électrons de la surface du cuivre interagissent avec le dioxyde de carbone et l’eau, en une succession d’étapes qui les transforment en produits comme l’éthanol, l’éthylène (précurseur des sacs en plastique) ou le propanol (un alcool couramment utilisé dans l’industrie pharmaceutique).
Depuis les années 1980, lorsque le potentiel du cuivre pour convertir le carbone en divers produits utiles a été découvert, il a toujours été supposé que ses sites actifs n’étaient pas spécifiques à un seul et unique produit. En d’autres termes, vous pouvez utiliser le cuivre comme catalyseur pour la fabrication de l’éthanol, de l’éthylène, du propanol, ou encore un autre produit chimique à base de carbone. Cependant, vous devrez suivre de nombreuses étapes pour séparer les produits chimiques indésirables résiduels formés au cours des étapes intermédiaires d’une réaction chimique, avant d’arriver à votre objectif final : soit le produit chimique final.
« L’objectif de la chimie « verte », ou durable, consiste à obtenir le produit que vous souhaitez lors de la synthèse chimique », a déclaré Ager. « Vous ne voulez pas séparer les produits que vous ne voulez pas des produits désirés, car cela est coûteux et indésirable pour l’environnement. Et cette dépense, et ce gaspillage, réduisent la viabilité économique des combustibles solaires à base de carbone », a ajouté Ager.
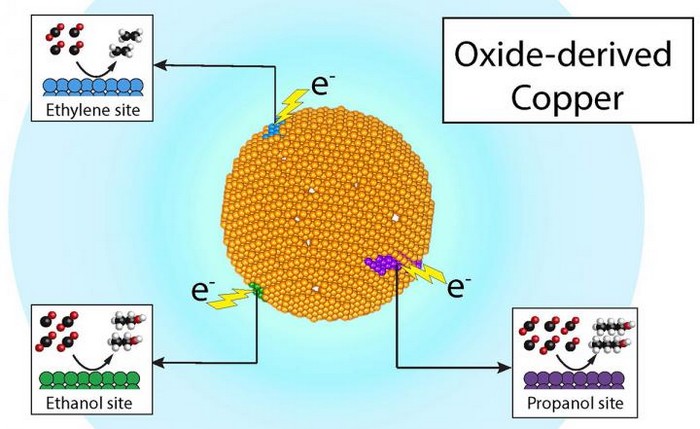
Donc, lorsqu’Ager et le co-auteur Yanwei Lum, qui était Ph.D. à l’Université de Berkeley au moment de l’étude, étudiaient les propriétés catalytiques du cuivre pour un projet de combustibles solaires, ils se sont demandés : « Et si, comme la photosynthèse dans la nature, nous pouvions utiliser des électrons de cellules solaires pour piloter des sites actifs spécifiques d’un catalyseur en cuivre, afin de créer un flux de produit pur d’un carburant ou d’un produit chimique à base de carbone ? », se souvient Ager.
Retracer l’origine d’un produit chimique grâce à son « passeport »
Des études antérieures avaient déjà permis de démontrer que le cuivre « oxydé », ou rouillé, est un excellent catalyseur pour la fabrication d’éthanol, d’éthylène et de propanol. Les chercheurs ont émis l’hypothèse que si les sites actifs du cuivre étaient en fait spécifiques à un produit, ils pourraient retracer l’origine des produits chimiques au moyen d’isotopes de carbone, « un peu comme un passeport avec des timbres nous indiquant les pays visités », a déclaré Ager.
« Lorsque nous avons pensé à l’expérience, nous nous sommes dit qu’il s’agissait d’une idée si peu évidente, que ce serait simplement fou d’essayer. Mais, nous ne pouvions pas oublier cette idée, nous pensions aussi que cela fonctionnerait, car nos recherches précédentes sur les isotopes nous avaient permis de découvrir de nouvelles voies de réaction », a ajouté Ager.
Ainsi, au cours des mois qui ont suivi, Lum et Ager ont mené une série d’expériences utilisant deux isotopes de carbone, le carbone 12 et le carbone 13, comme « tampons de passeport ».
Le dioxyde de carbone était marqué avec du carbone 12 et le monoxyde de carbone (un intermédiaire clé dans la formation de liaisons carbone-carbone), était marqué avec du carbone 13. Selon la méthodologie des chercheurs, ces derniers ont estimé que le rapport entre le carbone 13 et le carbone 12 contenu dans un produit déterminerait les sites d’origine du produit chimique.
Après avoir effectué des dizaines d’expériences et utilisé des techniques de pointe de spectrométrie de masse et de spectroscopie RMN (résonance magnétique nucléaire) au JCAP, les chercheurs ont découvert que trois des produits (soit toujours l’éthylène, l’éthanol et le propanol) présentaient des signatures d’isotopes différentes, démontrant qu’elles provenaient de différents sites sur le catalyseur ! « Cette découverte motive des travaux futurs visant à isoler et à identifier ces différents sites. Le regroupement de ces sites spécifiques en un seul catalyseur pourrait un jour aboutir à une génération très efficace et sélective de produits chimiques », a déclaré Lum.
Nous allons peut-être vers des jours plus verts concernant la fabrication de produits chimiques
La nouvelle méthodologie des chercheurs, décrite par Ager comme « une chimie simple avec une touche environnementale et économique », est le début de ce qu’ils espèrent être un nouveau départ pour la fabrication de produits chimiques verts, où une cellule solaire pourrait alimenter des électrons sur des sites actifs spécifiques au sein d’un catalyseur en cuivre, ce qui permettrait d’optimiser la production de carburants à l’éthanol, par exemple.
« Peut-être qu’un jour cette technologie pourrait rendre possible la création d’une raffinerie de pétrole, mais alimentée par le soleil, peut-être qu’elle permettra d’extraire le dioxyde de carbone de l’atmosphère et créer un flux de produits utiles », a-t-il déclaré.



 L’électron est une particule élémentaire qui, avec les protons et les neutrons, constitue les atomes. C’est donc l’un des composants principaux de la matière baryonique. À ce titre, il revêt... [...]
L’électron est une particule élémentaire qui, avec les protons et les neutrons, constitue les atomes. C’est donc l’un des composants principaux de la matière baryonique. À ce titre, il revêt... [...]