La compréhension de l’autisme a notablement évolué au cours de ces dernières années, avec l’apparition de meilleurs outils diagnostics et thérapeutiques. Cependant, les causes exactes à l’origine de ce trouble du développement sont encore mal connues, c’est notamment le cas de la part génétique complexe associée au développement de l’autisme. Récemment, une équipe de chercheurs a fourni une explication concernant l’apparition fréquente de crises épileptiques concomitantes à l’autisme.
Les troubles du spectre de l’autisme (TSA) constituent un trouble neurodéveloppemental extrêmement fréquent – touchant 1 enfant sur 68 – caractérisé par une large variété de symptômes, incluant d’importantes difficultés dans la communication et les interactions sociales. Un tiers des enfants avec des troubles autistiques présentent également des crises d’épilepsie. Les scientifiques savaient déjà que cette épilepsie était due à une mutation génétique retrouvée chez ces enfants, mais ne comprenaient pas le rôle exacte de cette mutation dans l’apparition de crises épileptiques.
Dans une étude publiée dans le journal Molecular Psychiatry, des neurobiologistes de l’université de Northwestern (Chicago, USA) montrent que la mutation en question altère la taille et la morphologie des épines dendritiques et des synapses, des éléments neuronaux impliqués dans la transmission des signaux cérébraux. L’altération génétique entraînerait ainsi une perte d’intégrité, partielle ou totale, des différents signaux transmis.
Chez les personnes atteintes de cette mutation génétique, les neurones inhibiteurs – des neurones chargés de minimiser ou bloquer les influx nerveux anarchiques ou de trop grande amplitude – sont sous-développés, perdant ainsi une grande partie de leur efficacité. L’impossibilité d’inhiber suffisamment les différents signaux erratiques produits conduit à l’apparition de fréquentes crises d’épilepsie.
La mutation génétique affecte une protéine baptisée « CNTNAP2 » (pour Contactin associated protein-like 2), et est associée à une seconde mutation appelée « CASK » (pour Calmodulin-dependent serine protein kinase), impliquée dans certaines déficiences intellectuelles. Grâce à cette découverte, les chercheurs ont pu mettre en lumière de nouvelles cibles pour le développement de traitements thérapeutiques. « Désormais, nous pouvons commencer à tester des traitements ciblant les crises épileptiques ainsi que les autres symptômes autistiques » explique Peter Penzes, auteur principal de l’étude. « Les personnes présentant la mutation souffrent également de retards du langage et de déficiences intellectuelles. Donc un médicament ciblant directement la mutation pourrait avoir de multiples bénéfices ».
Dans ce podcast (en anglais), Peter Penzes aborde les résultats de la découverte et ses implications thérapeutiques :
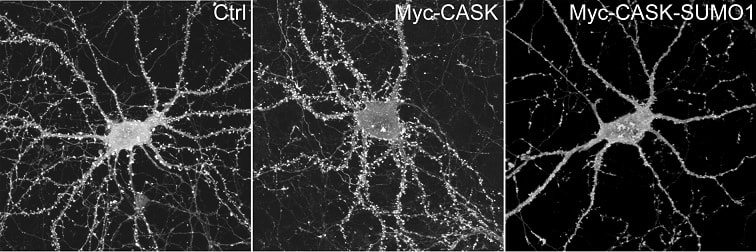
Le prochain objectif de l’équipe de Penzes sera de trouver des molécules activant CASK, car son activité permet de maintenir l’intégrité des dendrites et favorise le développement de l’arborescence dendritique. Lorsque CASK est bloquée, la croissance des dendrites est stoppée. De nombreuses recherches devront encore être menées afin de passer aux premiers essais cliniques humains, mais cette découverte ouvre d’ores et déjà la voie au développement de nouveaux traitements prometteurs.


