Pour la toute première fois, la fonction de la protéine SAP-97, fortement liée au développent de la schizophrénie, a été mise en évidence. L’équipe de recherche à l’origine de cette découverte a réussi à localiser son lieu d’action dans le cerveau. Il s’agirait d’une région de l’hippocampe appelée « gyrus denté ». C’est une avancée majeure dans la compréhension de la maladie, qui pourrait aboutir rapidement à l’amélioration des traitements actuels.
La schizophrénie est une maladie psychiatrique, très invalidante et relativement fréquente. Elle touche près de 20 millions de personnes dans le monde. Elle débute généralement chez l’adolescent ou le jeune adulte, entre 15 et 25 ans. La personne atteinte perd le contact avec la réalité et n’est pas consciente de son trouble. Elle peut présenter des idées délirantes, des hallucinations, l’absence d’émotions ou l’incapacité de planifier des actions et des déficits de mémoire.
Si des éléments importants concernant le rôle de la génétique et de l’environnement ont été rapportés, les mécanismes cellulaires et moléculaires perturbés dans le cerveau sont encore à élucider, malgré plusieurs décennies de recherche. Les régions spécifiques du cerveau affectées par ces perturbations ne sont toujours pas connues.
Des facteurs de risque génétiques, augmentant la susceptibilité de développer la maladie, ont été identifiés, ainsi que des mutations ponctuelles avec des effets probables sur la plasticité cérébrale, la dynamique des connexions cérébrales et de leur adaptation aux apprentissages et expériences de vie. Par exemple une micro-délétion sur le chromosome 22 dans la région q11, augmente le risque de développer une schizophrénie de 25%, selon Hideyuki Okano, professeur de physiologie à l’école de médecine de l’Université Keio.
Des synapses dysfonctionnelles et une mauvaise mémoire
Les chercheurs de l’Université de Californie du Sud (USC) se sont focalisés sur une protéine spécifique nommée SAP-97 (protéine associée à la synapse 97). Les études antérieures soutiennent un lien entre la perte de fonction de SAP-97 et la schizophrénie. Effectivement, le gène codant pour SAP-97, DLG1, a été récemment identifié comme une plaque tournante potentielle du dysfonctionnement synaptique lié à la schizophrénie. Des mutations de micro-délétion entraînant la perte de DLG1 augmentent d’ailleurs de 40 fois le risque de développer une schizophrénie. Reste à déterminer son rôle précis et son lieu d’action.
SAP-97 est une protéine guanylate kinase associée à la membrane (MAGUK). Cette famille de protéines contient les principaux constituants de la synapse glutamatergique, c’est-à-dire médiée par le glutamate. Elles forment, en d’autres termes, l’armature protéique des synapses. Dans le cerveau des vertébrés, le glutamate est le principal neurotransmetteur excitateur, transmettant les messages nerveux de la synapse au neurone suivant. SAP-97 régulariserait alors la signalisation glutamatergique entre les neurones du cerveau et influencerait la création et le stockage des souvenirs.
Logiquement, les scientifiques, depuis des années, cherchent à démontrer la présence et l’action de cette protéine dans les zones cérébrales habituellement impliquées dans la régulation de la communication entre les neurones. Tel n’étant pas le cas, ils ont tout simplement décidé de chercher dans une autre partie du cerveau, fortement liée à la schizophrénie, le gyrus denté.
Ce dernier fait partie de la formation hippocampique et joue un rôle clé notamment dans le traitement des informations spatiales et les processus mnésiques. Il contrôle la mémoire épisodique contextuelle, qui est le souvenir conscient des expériences de la vie. C’est dans cette partie du cerveau que nous nous souviendrons de ce qui s’est passé et du contexte (où et quand).
Ce type de mémoire est souvent déformé et altéré dans la schizophrénie, ce qui pourrait signifier que le gyrus denté serait altéré chez une personne atteinte de ce trouble. En étudiant des rats, chez lesquels SAP-97 avait été endommagé, l’équipe de recherche a mis en évidence des changements d’activité dans les neurones granulaires du gyrus denté.
Bruce Herring, auteur principal de l’étude, déclare dans un communiqué : « la fonction SAP-97 réduite peut très bien entraîner la plus forte augmentation du risque de schizophrénie chez l’homme à notre connaissance. Mais la fonction de SAP-97 est un mystère total depuis des décennies. Notre étude révèle où SAP-97 agit dans le cerveau et montre exactement ce que les mutations associées à la schizophrénie, dans cette protéine, impliquent pour les neurones ».
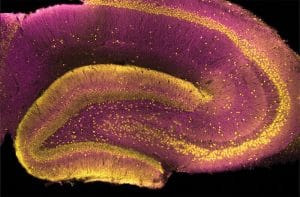
Les neurones du gyrus denté, avec une fonction SAP-97 réduite, ont montré des augmentations extrêmement importantes de la signalisation glutamatergique. Les récepteurs seraient surexcités. Ces pointes d’activité produisent de graves altérations de la mémoire épisodique contextuelle, symptôme classique de la schizophrénie.
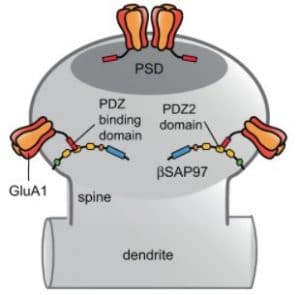
Les données démontrent que SAP-97 est distincte des autres protéines MAGUK dans sa fonction. Ces dernières diminuent l’activité synaptique si elles sont endommagées, ce qui n’est pas le cas ici. Il semble, selon les auteurs, que SAP-97 modifie la configuration du récepteur glutamate. Ceci serait induit par la perturbation de l’interaction de SAP-97 avec le domaine de liaison PDZ C-terminal de la protéine GluA1 de ces récepteurs (figure ci-dessous).
Espoirs thérapeutiques
L’équipe de B. Herring prévoit maintenant de rechercher l’activité de SAP-97 dans d’autres régions du cerveau. Ils veulent également déterminer si des mutations liées à la schizophrénie dans d’autres protéines produisent des augmentations similaires de la signalisation glutamatergique dans le gyrus denté.
Avec ces découvertes, identifier les personnes à risque de développer une schizophrénie pourrait être facilité, en sachant où et quoi chercher. Cela conduira à de nouvelles mesures de diagnostic, de prévention et de traitement.
Actuellement, le traitement le plus courant de la schizophrénie est la médication antipsychotique associée à la thérapie et au soutien social. Cependant, ces médicaments peuvent avoir de très nombreux effets secondaires, perturbant la vie quotidienne.
Ces travaux en cours contribueront de manière significative au développement de stratégies thérapeutiques plus efficaces, améliorant la vie de millions de personnes atteintes de schizophrénie dans le monde.