Des chercheurs ont identifié deux molécules dont l’interaction augmente considérablement la propagation de la protéine alpha-synucléine toxique au niveau des neurones, une caractéristique clé de la maladie de Parkinson. Le ciblage de l’une d’entre elles par un médicament anticancéreux approuvé par la FDA inhiberait cette interaction, conduisant ainsi à une réduction significative de la quantité de la protéine alpha-synucléine. Le médicament pourrait ainsi constituer une option prometteuse pour ralentir la progression de la maladie.
Affectant près de 8,5 millions de personnes dans le monde, Parkinson est la deuxième maladie neurodégénérative la plus courante, après Alzheimer. Elle se manifeste par des troubles progressifs du mouvement (tremblements, raideurs, problèmes d’équilibre, difficultés d’élocution, …) ainsi que des troubles de l’humeur et des fonctions cognitives. Ces symptômes sont dus à l’accumulation excessive de protéines alpha-synucléine mal repliées au niveau des neurones et des cellules gliales.
Alors que l’alpha-synucléine soluble est essentielle à la communication synaptique, celle mal repliée est une forme toxique se propageant progressivement depuis les systèmes nerveux entérique et périphérique vers le système nerveux central. Son accumulation induit une forme de mort programmée (un processus appelé « parthanatos ») des neurones dopaminergiques, ce qui entraîne les symptômes typiques de la maladie.
La propagation de l’alpha-synucléine pathologique est donc considérée comme un mécanisme essentiel à la pathogénicité de la maladie. Ce processus s’effectue par le biais de récepteurs de surface cellulaires médiant à la fois sa propagation entre les neurones et son absorption par ces derniers. Parmi ces récepteurs figure par exemple le gène d’activation des lymphocytes 3 (Lag3).
De précédentes études ont montré que sa suppression réduit significativement l’absorption de l’alpha-synucléine toxique par les neurones, sans pour autant la stopper. Cela suggère que d’autres récepteurs pourraient être partiellement impliqués dans la propagation et l’absorption de la protéine.
L’équipe de la nouvelle étude suggère qu’il pourrait s’agir de la protéine précurseur de la bêta-amyloïde de type 1 (Aplp1). En effet, il a notamment été montré que cette protéine se lie spécifiquement à l’alpha-synucléine pathologique et est associée à la neurodégénérescence. Cependant, son implication dans la propagation de l’alpha-synucléine était jusqu’ici inexplorée.
« Nos travaux ont précédemment démontré que Lag3 n’est pas la seule protéine de surface cellulaire qui aide les neurones à absorber l’alpha-synucléine. Nous nous sommes donc tournés vers Aplp1 dans nos expériences plus récentes », explique dans un communiqué la coauteure principale de la nouvelle étude, Valina Dawson, de l’Université Johns Hopkins (aux États-Unis). Des chercheurs de l’Université de technologie de Nagaoka (au Japon), de l’Université de Heidelberg (en Allemagne), de l’Université de Pittsburgh et de l’Académie chinoise des sciences, ont également participé à l’étude.
Une réduction de 90 % de l’absorption des protéines toxiques
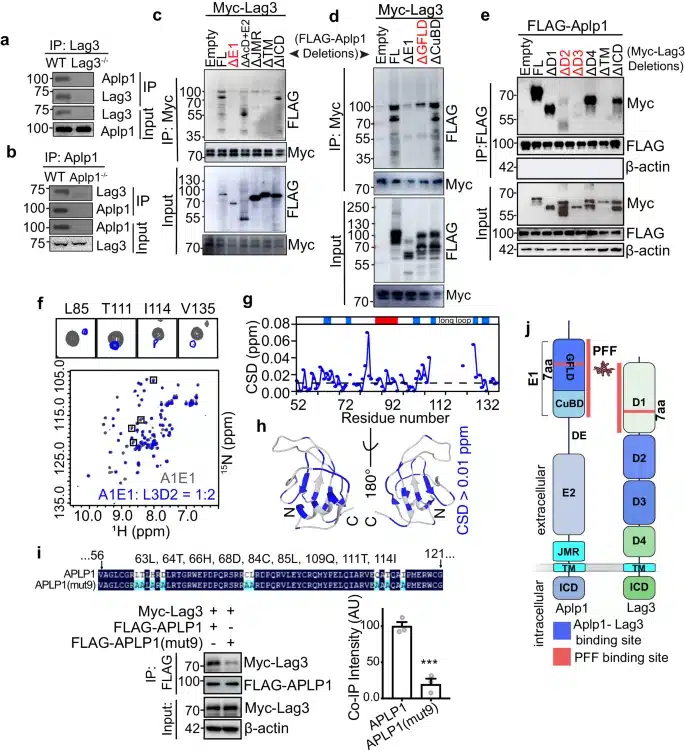
Pour étayer leur hypothèse, les chercheurs ont sélectionné des souris transgéniques dépourvues soit d’Aplp1, soit de Lag3, soit des deux. Ils ont constaté que la suppression d’Aplp1 réduisait significativement l’absorption de l’alpha-synucléine toxique et sa transmission de neurone à neurone. Les déficits comportementaux étaient également réduits chez les souris dépourvues du récepteur. Un effet similaire a été observé chez les souris dépourvues de Lag3.
Cependant, l’effet était encore plus important chez les souris dépourvues des deux récepteurs. L’absorption cellulaire de la protéine alpha-synucléine nocive a chuté de 90 %, tandis que la perte de neurones dopaminergiques et les déficits comportementaux étaient quasi inexistants. Cela suggère que l’interaction entre les deux protéines joue un rôle clé dans la progression de la maladie. La liaison d’Aplp1 avec Lag3 à la surface des neurones permettrait à ceux-ci d’absorber massivement l’alpha-synucléine toxique circulant dans l’espace intercellulaire, ce qui entraînerait un parthanatos.
Un médicament qui pourrait cibler toute une gamme de maladies neurodégénératives
Les chercheurs en ont déduit que cette interaction pourrait être une cible potentiellement prometteuse pour traiter la maladie. Le nivolumab/relatlimab, un anticorps anti-Lag3 approuvé en 2022 par la FDA pour le traitement du mélanome, pourrait inhiber cette interaction.
En injectant le médicament à des souris non génétiquement modifiées (c’est-à-dire pourvues des récepteurs Aplp1 et Lag3), le médicament a effectivement inhibé la propagation et l’absorption de l’alpha-synucléine mal repliée. Cet effet était en outre supérieur à celui de la suppression génétique de Lag3, en raison de l’association étroite entre les deux récepteurs.
Ces résultats suggèrent que le médicament pourrait à la fois être utilisé en tant que traitement contre Parkinson et pour d’autres maladies neurodégénératives impliquant le récepteur Aplp1, telles qu’Alzheimer. « Nos résultats suggèrent que cibler cette interaction avec des médicaments pourrait ralentir considérablement la progression de la maladie de Parkinson et d’autres maladies neurodégénératives », indique le coauteur de l’étude, Xiaobo Mao, également de l’Université Johns Hopkins.
D’autre part, étant donné qu’Alzheimer est également caractérisée par l’interaction de la protéine tau avec le récepteur Lag3, il serait logiquement possible de la traiter avec le même anticorps anti-Lag3. En prochaine étape, les chercheurs prévoient d’évaluer l’efficacité du nivolumab/relatlimab sur des modèles murins des deux pathologies. Les résultats de l’étude sont publiés dans la revue Nature Communications.