Développé par le laboratoire Gilead Sciences, le remdésivir est un analogue de l’adénosine, perturbant la chaîne de réplication virale. D’abord développé dans le cadre de la lutte contre le virus Ebola, dans laquelle il s’est montré très peu efficace, il a ensuite été testé en tant que thérapie contre le coronavirus SARS-CoV-2. Un premier essai, ayant donné lieu à une publication dans la revue The Lancet, a conclu à son inefficacité. Mais récemment, un second essai, supervisé par le NIAID, a montré que le remdésivir avait des effets positifs sur l’infection. Bien que les résultats soient prometteurs, ils n’ont pas encore fait l’objet de publication évaluée par les pairs, ils doivent donc être considérés avec précaution.
Une déclaration de l’Institut national américain des allergies et des maladies infectieuses (NIAID), qui a supervisé l’essai, affirme que les patients prenant le médicament, fabriqués par Gilead Sciences, ont montré un temps de récupération 31% plus rapide que ceux sous placebo. « Plus précisément, le délai médian de récupération était de 11 jours pour les patients traités par remdésivir contre 15 jours pour ceux qui ont reçu un placebo », indique le communiqué.
Les résultats de l’essai clinique du NIAID concernant le remdésivir
« Les données montrent que le remdésivir a un effet clair, significatif et positif en réduisant le délai de récupération. Bien qu’une amélioration de 31% ne semble pas être un knock-out à 100%, c’est une preuve de concept très importante, car ce qui a été prouvé, c’est qu’un médicament peut freiner ce virus », déclare Anthony Fauci, directeur du NIAID.
Les résultats suggèrent également que les personnes qui prenaient le médicament étaient moins susceptibles de décéder, bien que la différence soit assez faible. Le taux de mortalité était de 8.0% pour le groupe recevant du remdésivir contre 11.6% pour le groupe placebo. L’essai a commencé le 21 février et a impliqué 1063 personnes réparties sur 68 sites aux États-Unis, en Europe et en Asie.
Le premier patient à être inscrit était un Américain qui a été rapatrié après avoir été mis en quarantaine sur le bateau de croisière Diamond Princess et soigné à l’University of Nebraska Medical Center. Ni les patients ni leurs médecins ne savaient à quel groupe ils appartenaient, afin d’éliminer les biais méthodologiques. « Nous devons voir les résultats complets, mais s’il est confirmé, ce serait un résultat fantastique et une excellente nouvelle pour la lutte contre le COVID-19 », indique Peter Horby, un épidémiologiste de l’Université d’Oxford.
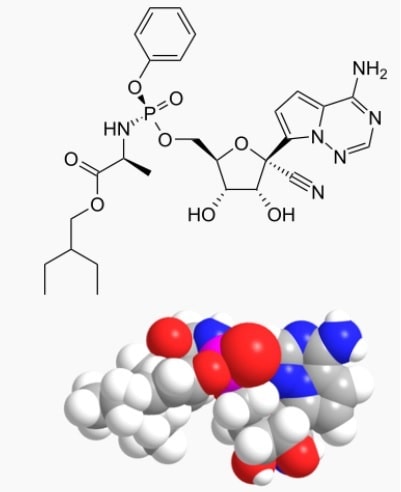
Le remdésivir, qui a précédemment échoué dans les essais contre le virus Ebola, appartient à une classe de médicaments qui agissent directement sur le virus. Il mime l’une des bases nucléotidiques de l’ARN et est absorbé dans le génome du virus, neutralisant son processus de réplication. Fauci a indiqué que puisque cette approche avait donné un certain succès, elle pourrait ouvrir la voie à de meilleurs médicaments adoptant le même modèle.
Les résultats de l’essai n’ont toutefois pas encore été évalués par les pairs, il n’y a donc pour le moment aucune publication scientifique officielle ; les scientifiques ne pouvant pour l’instant que s’appuyer sur les déclarations du NIAID. Cependant, les essais ont été menés en respectant scrupuleusement la méthodologie clinique — un essai randomisé en double aveugle — et, malgré l’absence de peer-review, s’avèrent tout de même prometteurs.
Contradictions avec les essais chinois et précautions
Alors que les résultats ont reçu des avis positifs de la part de la communauté scientifique, d’autres experts ont précisé que les avantages étaient relativement modestes. « Il s’agit de la première preuve que le remdésivir présente de réels avantages, mais ils ne sont certainement pas spectaculaires », déclare Stephen Evans, expert en statistiques médicales à la London School of Hygiene & Tropical Medicine.
Sur le même sujet : Coronavirus : les potentiels dangers de l’hydroxychloroquine soulevés par une étude américaine
« Ces données sont prometteuses, et étant donné que nous n’avons pas encore de traitements éprouvés pour le coronavirus, cela pourrait bien conduire à une approbation accélérée du remdésivir pour le traitement de COVID-19. Cependant, cela montre également que le remdésivir n’est pas une solution miracle dans ce contexte », déclare Babak Javid, virologiste à la Tsinghua University School of Medicine à Pékin.
Un résumé des résultats, publié sur le site de l’Organisation mondiale de la santé la semaine dernière, a montré que la molécule avait échoué dans un essai chinois plus restreint. La revue The Lancet a publié l’article revu par les pairs décrivant cet essai clinique. Dans cette étude portant sur 237 patients (158 traités et 79 sous placebo) à Wuhan, les médecins n’ont trouvé aucun effet positif de l’administration du médicament par rapport à un groupe témoin d’adultes, à l’exception des patients nécessitant des respirateurs.
Mais le test chinois a dû être interrompu tôt car il ne pouvait pas recruter suffisamment de personnes pour atteindre ses objectifs initiaux et a été considéré par certains experts comme trop petit pour en tirer des conclusions fiables. Toutefois, l’essai chinois respectait lui aussi rigoureusement la méthodologie clinique, et les seules critiques pouvant lui être adressées ne concernent que la taille de son échantillon. Il faudra donc attendre plus de résultats pour déterminer les véritables effets du remdésivir.