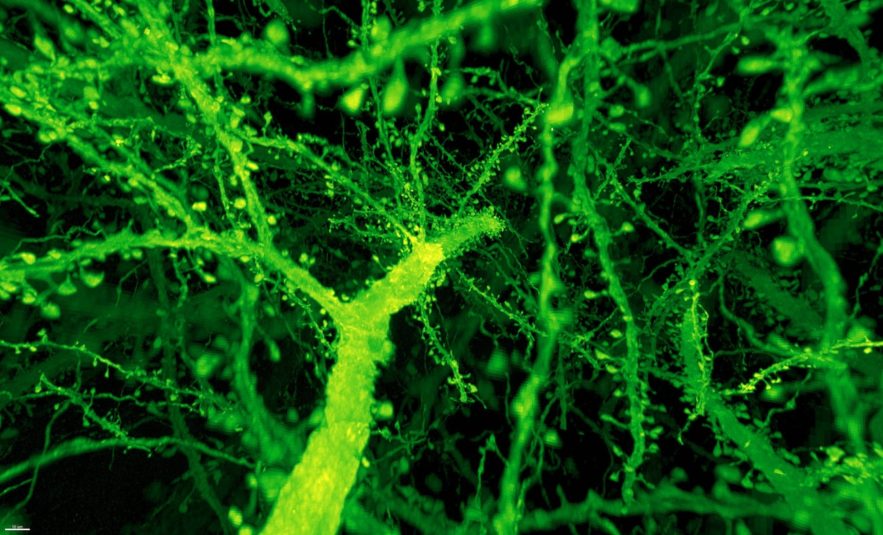
Des scientifiques ont amélioré une méthode de microscopie à fluorescence pour obtenir de meilleures images d’échantillons de tissus, et ainsi permettre d’observer avec une haute résolution les structures en 3D, sans altération de la qualité de la fluorescence.
La « microscopie par dilatation« , une technique apparue il y a quelques années, consiste à injecter un gel dans un tissu ou des cellules, qui va se polymériser et ainsi augmenter leur taille apparente au microscope, sans perturber leur structure, évitant ainsi un zoom trop important. Elle permet par exemple de mieux détailler les images du cerveau, en marquant les neurones pour obtenir un plan de leur trajet et de leurs connections.
Mais le gel injecté augmente considérablement le temps nécessaire pour capturer les images. Les inconvénients apparaissent lorsque l’on travaille avec de gros échantillons, où le faisceau envoyé par le microscope, qui capture des images de haut en bas, peut détruire des molécules de fluorescence attachées aux protéines que l’on souhaite observer, lorsque la capture est trop longue, causant l’apparition de zones sombres sur l’image.
Des chercheurs du Howard Hughes Medical Institute aux États-Unis ont trouvé un moyen de capturer les images plus rapidement, en combinant deux techniques : la méthode de la dilatation par le gel, et la microscopie à nappe de lumière, qui permet d’envoyer un réseau de faisceaux lumineux très minces sur l’échantillon à analyser. Cette stratégie évite la perte de fluorescence causée par la phototoxicité du faisceau, en réduisant au maximum le champ de rayonnement de ce dernier, permettant ainsi la diminution de l’intensité de la lumière.
Les chercheurs ont diffusé des images détaillés des épines dendritiques de souris, ainsi que celles d’un cerveau entier d’une mouche, capturées en seulement 62.5 heures, ce qui est sept fois plus rapide que les microscopes à haute résolution connus pour être les plus efficaces.
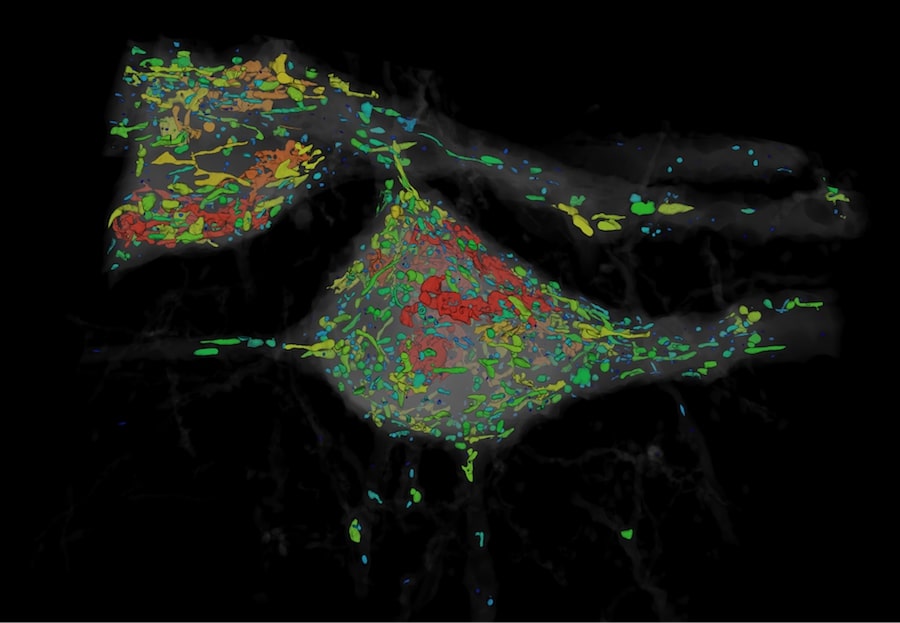
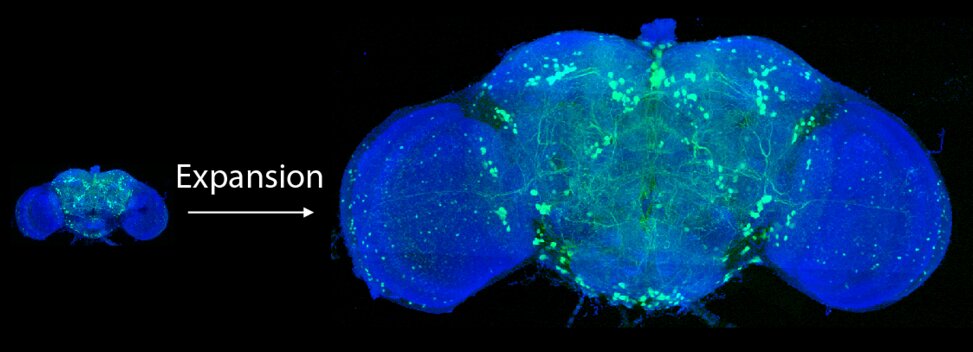
« Je nous vois au point d’imager au moins 10 cerveaux de mouche par jour », a déclaré Betzig, prix Nobel de chimie en 2014 pour ses travaux en microscopie, et qui a aidé le groupe pour la recherche. « Cette rapidité et cette résolution permettront aux scientifiques de se poser de nouvelles questions, notamment concernant les différences entre les cerveaux des hommes et des femmes, ou entre les circuits du cerveau des mouches du même type ».
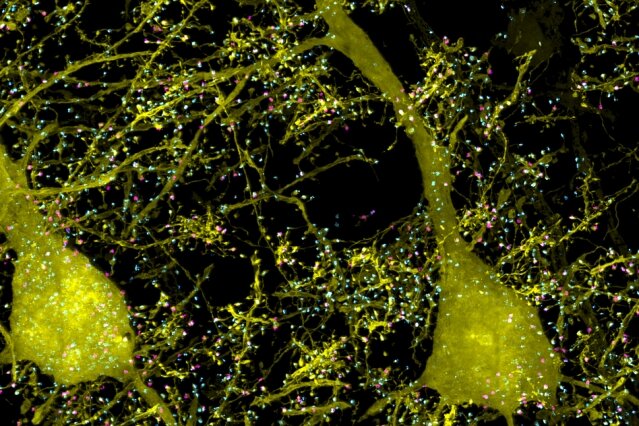
Les progrès réalisés dans les outils informatiques qui permettent d’associer plusieurs segments en 3D, ont permis aux chercheurs de capturer des images de larges sections du cerveau, pour pouvoir ensuite les zoomer à haute résolution. Ils espèrent à l’avenir créer une carte du cerveau détaillée au point de pouvoir le simuler sur ordinateur.
« Nous avons franchi un seuil en matière de performances d’imagerie », a déclaré Ed Boyden, chef du groupe.« C’est pourquoi nous sommes si enthousiastes. Nous ne balayons pas simplement de plus en plus de tissu cérébral, nous scrutons des cerveaux entiers ».
Une vidéo montrant les différentes captures 3D :