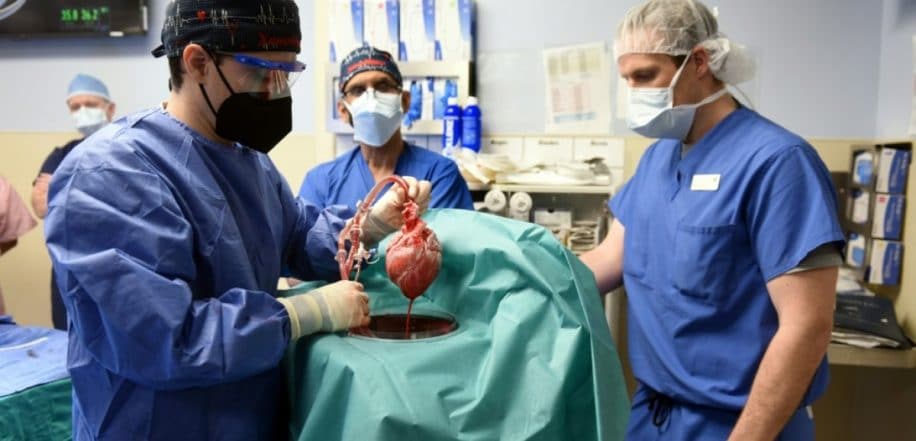
David Bennett, le premier patient au monde à avoir reçu une greffe de cœur de porc (génétiquement modifié), est décédé deux mois après son opération, a annoncé mercredi 9 mars l’hôpital où il était pris en charge. Les responsables de l’essai ont néanmoins souligné que l’expérience représentait une grande avancée pour la recherche. Retour sur cette prouesse médicale.
Actuellement, l’OMS estime à environ 90 000 le nombre de dons d’organes qui sont effectués chaque année dans le monde, parmi lesquels on dénombre 6000 transplantations cardiaques. Cette opération est proposée aux patients porteurs d’une insuffisance cardiaque grave et irréversible, pour laquelle l’espérance de vie est limitée. La transplantation cardiaque reste essentiellement limitée par la faible disponibilité des greffons. De fait, le nombre de transplantés stagne alors que les besoins augmentent.
C’est pourquoi l’opération, réalisée le 7 janvier, avait soulevé un grand enthousiasme, car de telles xénogreffes — d’un animal à un humain — pourraient potentiellement permettre de remédier à la pénurie de dons d’organes.
David Bennett, porteur d’espoir
David Bennett est arrivé au centre médical de l’Université du Maryland (UMMC) en tant que patient en octobre 2021. Il a été alité et placé sur un appareil de pontage cœur-poumon, appelé oxygénation par membrane extracorporelle (ECMO), pour rester en vie. Il a été jugé inéligible pour une transplantation cardiaque conventionnelle.
Avant de consentir à recevoir la greffe, D. Bennett a été pleinement informé des risques de la procédure et du fait qu’elle était expérimentale, avec des risques et des avantages inconnus. Le 31 décembre 2021, l’U.S. Food and Drug Administration a accordé une autorisation d’urgence pour l’opération, dans l’espoir de lui sauver la vie. Après la chirurgie, le cœur transplanté a très bien fonctionné pendant plusieurs semaines, sans aucun signe de rejet. Le patient a pu passer du temps avec sa famille et participer à une thérapie physique pour l’aider à reprendre des forces.
Bartley P. Griffith, MD, qui a chirurgicalement transplanté le cœur de porc chez le patient, déclare dans un communiqué : « Nous sommes dévastés par la perte de M. Bennett. Il s’est avéré être un patient courageux et noble qui s’est battu jusqu’au bout ». Le Dr Mohiuddin, professeur de chirurgie et directeur scientifique du programme de xénotransplantation cardiaque à la faculté de médecine de l’Université du Maryland (UMSOM), ajoute : « Nous avons acquis des connaissances inestimables en apprenant que le cœur de porc génétiquement modifié peut bien fonctionner dans le corps humain alors que le système immunitaire est correctement inhibé ».
Un porte-parole de l’hôpital a déclaré : « Aucune cause évidente n’a été identifiée au moment de sa mort », ajoutant que des médecins procédaient à un examen qui serait publié dans une revue scientifique. Le Dr Mohiuddin a cependant précisé que D. Bennett avait des « épisodes infectieux ». Compte tenu du fait qu’il était sous traitement immunosuppresseur, il a été difficile de contrôler ses infections. L’état de D. Bennett a commencé à se détériorer il y a plusieurs jours. Lorsqu’il est devenu évident qu’il ne s’en remettrait pas, il a reçu des soins palliatifs.
David Bennett, outre le fait de porter les espoirs de xénogreffes, a aussi mis en lumière les dilemmes éthiques qui peuvent surgir lors de transplantations. En effet, il avait été reconnu coupable d’avoir poignardé un homme à plusieurs reprises en 1988, laissant la victime paralysée et en fauteuil roulant. Elle décéda en 2005. Son cas se veut l’illustration, pour les éthiciens médicaux, que les antécédents criminels d’une personne ne devraient avoir aucune incidence sur son traitement futur.
Les xénotransplantations pour pallier la pénurie d’organes humains
Environ 110 000 Américains attendent actuellement une greffe d’organe, et plus de 6000 patients meurent chaque année avant d’en obtenir une, selon les chiffres officiels. Pour répondre à la demande, les médecins s’intéressent depuis longtemps à la xénotransplantation, ou don d’organes interespèces, avec des expériences remontant au XVIIe siècle. Notons que la xénotransplantation est une procédure impliquant la transplantation, chez un receveur humain, de cellules, tissus ou organes vivants provenant, soit d’une source animale non humaine, soit d’une source humaine, mais ayant subi un contact ex vivo avec du matériel biologique vivant d’animaux non humains.
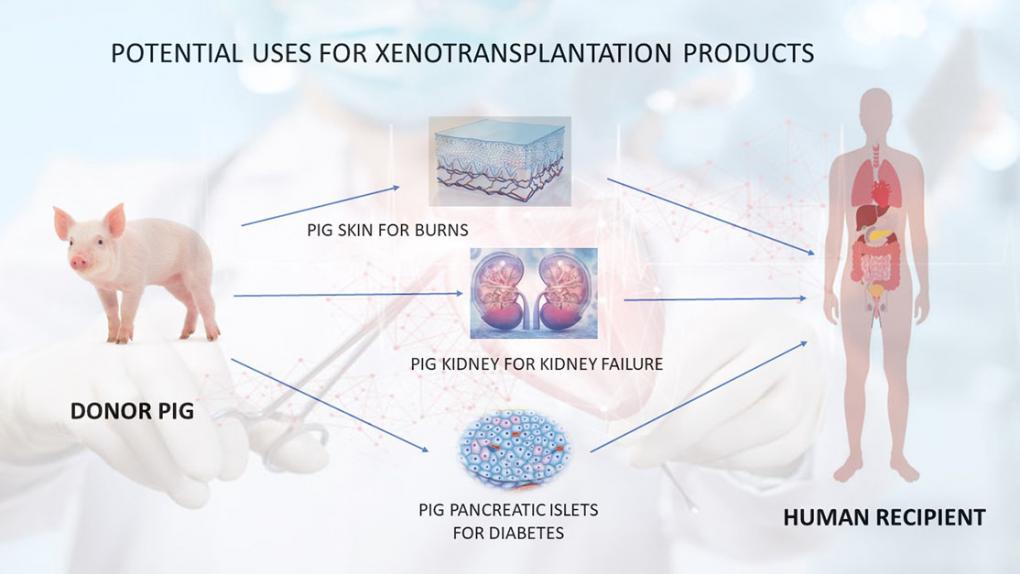
Les premières recherches concernaient le prélèvement d’organes sur des primates. Aujourd’hui, les valvules cardiaques de porcs sont largement utilisées chez l’Homme, par exemple.
Dans ce contexte, les porcs sont les donneurs idéaux en raison de leur taille, de leur croissance rapide et de leurs grandes portées. Par ailleurs, l’emploi d’organes porcins est mieux accepté, car ils sont déjà utilisés pour l’alimentation, avait expliqué en octobre Robert Montgomery, directeur de l’Institut de transplantation de l’Université de New York. Le cœur utilisé pour D. Bennett provenait de Revivicor en Virginie, une filiale d’United Therapeutics. Cette société de biotechnologie a également fourni les animaux utilisés dans trois récentes greffes de rein de porc chez l’homme. Mais ces procédures ont été effectuées sur des receveurs en état de mort cérébrale, dans le cadre d’expériences de preuve de concept. La chirurgie de Bennett a été la première à réellement aider un patient qui a continué à vivre après la procédure.
Ainsi, le coeur greffé a subi 10 modifications génétiques afin de le rendre acceptable pour un humain. Certaines des modifications sont conçues pour empêcher l’organe de se développer après la greffe, d’autres pour le rendre plus tolérable pour le système immunitaire humain, notamment en éliminant un gène produisant un sucre particulier. Ce dernier aurait autrement déclenché une forte réponse immunitaire et conduit au rejet de l’organe. Enfin, six gènes humains responsables de l’acceptation immunitaire ont été insérés dans le génome. L’équipe du centre médical de l’Université du Maryland a également utilisé un nouveau médicament fabriqué par Kiniksa Pharmaceuticals dans le but d’empêcher l’organe d’être rejeté par le corps du patient.
Et ce fut le cas : après la chirurgie, le cœur transplanté a très bien fonctionné pendant plusieurs semaines sans aucun signe de rejet, a précisé l’hôpital. L’expérience peut dès lors être considérée comme un succès, selon les chercheurs. Mohiuddin conclut : « Nous restons optimistes et prévoyons de poursuivre nos travaux dans de futurs essais cliniques ».