Des chercheurs ont développé un dispositif permettant d’isoler le flux sanguin alimentant le cerveau afin de le maintenir en vie indépendamment du reste du corps. Testé sur des modèles porcins anesthésiés, le dispositif a permis de maintenir presque toutes les fonctions de l’organe durant cinq heures. Cette prouesse technique ouvre la voie à de nouvelles façons d’étudier le fonctionnement cérébral sans l’influence d’autres fonctions organiques. Elle pourrait aussi aider à la conception de machines cœur-poumon plus efficaces.
Le cerveau contrôle l’ensemble de l’organisme en régissant un large éventail de processus, des plus vitaux tels que la fréquence cardiaque, la respiration, le cycle du sommeil, aux plus subtils. Inversement, ces processus peuvent à leur tour influencer le fonctionnement cérébral. La manipulation du flux sanguin cérébral permettrait, en isolant l’organe, d’étudier en profondeur les effets de différents dysfonctionnements physiologiques sur le cerveau, tels que l’ischémie et les accidents vasculaires cérébraux par exemple. Elle permettrait également d’analyser de manière plus précise le mode d’action des molécules thérapeutiques.
Un accès vasculaire spécifiquement cérébral permettrait notamment de caractériser différentes propriétés indépendamment des influences somatiques, autrement inévitables. En effet, le métabolisme ou la distribution multi-organes de substances bioactives peuvent entraver la précision des analyses cinétiques spécifiquement associées au cerveau. La fluctuation du débit et de la pression sanguine (en cas d’hypertension artérielle par exemple) peuvent par exemple provoquer des effets non négligeables sur le fonctionnement cérébral.
Afin de contourner ces limitations, des scientifiques tentent depuis plusieurs décennies de concevoir des dispositifs permettant d’isoler le cerveau du reste du corps tout en maintenant ses fonctions. L’approche la plus utilisée implique la déconnexion de la vascularisation naturelle, suivie de l’apport artificiel du soutien et du contrôle circulatoire. Cependant, cette méthode comporte des limites pouvant entraver l’étude détaillée du cerveau.
Le nouveau dispositif, décrit dans la revue Scientific Reports, consiste en un système mécanique assisté par ordinateur de régulation de la perfusion et de la composition sanguine. En d’autres termes, le cerveau est isolé du corps puis alimenté en débit sanguin contrôlé. Selon les auteurs de la nouvelle étude, il n’existait jusqu’à présent aucun dispositif permettant de véritablement isoler le cerveau et de le garder fonctionnel.
L’isolement du cerveau permet de manipuler les entrées afin d’étudier de quelle manière elles y provoquent des modifications. Dans une précédente étude, l’équipe de recherche a utilisé le dispositif pour analyser les effets cérébraux de l’hypoglycémie. Il est important de noter que bien que l’on puisse induire une hypoglycémie in vivo (en réduisant l’apport calorique ou en administrant de l’insuline), le reste de l’organisme peut partiellement compenser en modifiant le métabolisme, qui à son tour modifie le cerveau. En revanche, le nouveau système proposé ici permet de contrôler la glycémie directement par le biais du sang pompé vers le cerveau.
Un flux sanguin pulsatile comparable à celui du cœur
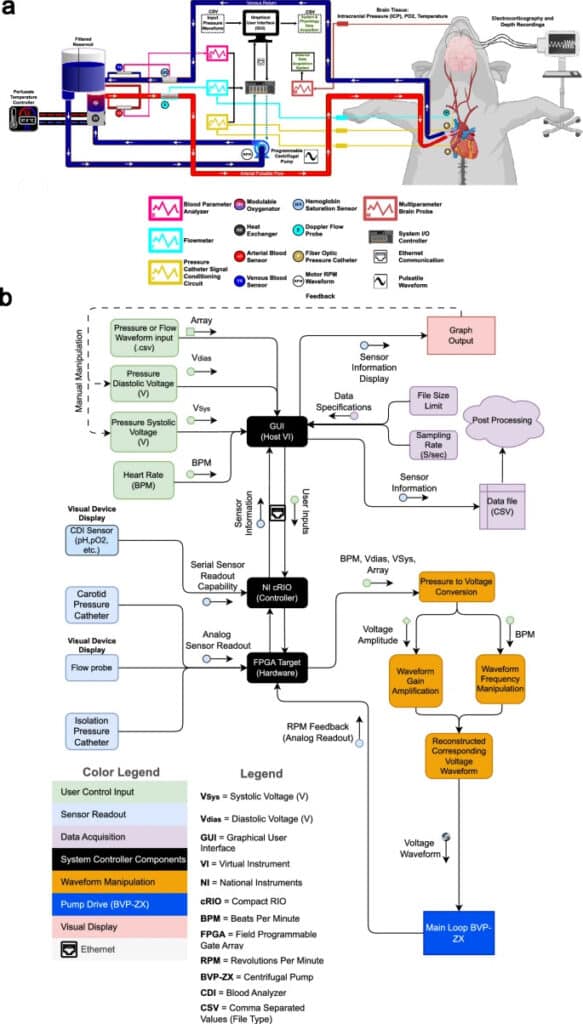
Le dispositif est adapté à la circulation naturelle artérielle et veineuse des porcs (sur lesquels ont été menées les expérimentations). L’apport sanguin au cerveau est assuré par un système de pompe contrôlant différentes variables physiologiques, notamment la pression artérielle, le volume sanguin ainsi que sa température, son niveau d’oxygène et les nutriments qu’il contient. À noter que les machines cœur-poumon conventionnelles reproduisent certaines des fonctions de ces organes, en délivrant un flux continu de sang oxygéné dans l’ensemble de l’organisme. En revanche, le nouvel appareil — baptisé système de Contrôle Circulatoire Pulsatile Extracorporel (EPCC) — utilise un flux pulsatile comparable à celui du cœur. Cela permettrait de prévenir les effets secondaires provoqués par les dispositifs standards (tels que l’hémorragie et l’AVC).
Afin de permettre des analyses neurophysiologiques correspondant aux conditions naturelles, le dispositif a été paramétré de sorte à conserver l’activité neuronale d’ordre supérieur, telle que rapportée par l’électrocorticographie continue (ECoG) et les enregistrements intracérébraux de potentiel de champ (enregistrements en profondeur par électrodes).


L’EcoG est une mesure englobant un grand ensemble d’activités cellulaires, de connectivités hautement organisées en signaux oscillatoires, ainsi que d’autres signaux périodiques qui changent sur des intervalles de temps bien définis. De précédentes expériences ont montré que même si un cerveau animal post-mortem soumis à une perfusion mécanique maintient un large éventail d’activités neuronales locales et individuelles, l’ECoG n’est pas maintenue. Cela indique qu’elle représente une mesure particulièrement fiable de l’intégrité des fonctions neuronales.
D’autre part, des enquêtes ont révélé que les deux mesures (ECoG et enregistrements de potentiel de champ profond intracérébral) sont sujettes à quelques secondes ou minutes de fluctuation de perfusion. Afin d’évaluer la conservation de l’activité cérébrale sous EPCC, les enregistrements ont été effectués avant et pendant la perfusion et sous interférence minimale avec l’anesthésie.
Après analyse, les chercheurs ont constaté que les mesures du fonctionnement cérébral des animaux ne présentaient que des changements mineurs, voire nuls, sur une période 5 heures. L’activité cérébrale restait inchangée ou peu perturbée par rapport à celle normale, ainsi que le taux d’oxygénation, la pression interne, la température et la structure microscopique. « Cette nouvelle méthode permet des recherches axées sur le cerveau indépendamment du corps, ce qui nous permet de répondre aux questions physiologiques d’une manière qui n’a jamais été réalisée », conclut l’un des concepteurs, Juan M. Pascual, de l’UT Southwestern Medical Center (États-Unis).


