Un nouveau traitement sous forme de gouttes nasales pourrait réparer les dommages résultant d’un accident vasculaire cérébral (AVC), en boostant le système naturel de réparation neuronale. Administrées une semaine après un AVC, les gouttes pourraient potentiellement éviter les séquelles à long terme pour les patients ne pouvant bénéficier de soins immédiats.
À la suite d’un AVC, un processus naturel connu sous le nom de « gliose réactive » s’enclenche dès les premières heures qui s’ensuivent, afin de réparer les dommages neuronaux liés à l’ischémie (ou déficit d’apport en oxygène). Il s’agit d’une réponse dynamique majoritairement orchestrée par les astrocytes et les cellules de la microglie, visant à limiter la perte de tissu et à en restaurer l’homéostasie. Cette réponse engendre la différenciation de cellules souches neurales en nouveaux neurones afin de remplacer ceux perdus, ainsi qu’un « recâblage » des connexions neuronales restantes.
Cependant, la réaction astrocytaire — dont les modifications peuvent considérablement changer avec le temps — a également un impact sur la plasticité neuronale et la récupération fonctionnelle. En effet, les astrocytes régulent à la hausse l’expression de la protéine acide fibrillaire gliale (GFAP) quelques heures après l’ischémie et commencent à s’hypertrophier après quelques jours. Ce processus engendre un tissu cicatriciel glial qui manque de malléabilité, au niveau de la région endommagée. Il y a également une suractivation des microglies dès 30 minutes après l’ischémie, persistant durant les semaines suivantes. Ainsi, ce schéma de suractivation croissante suggère un effet protecteur au stade précoce post-AVC, mais qui devient délétère aux stades ultérieurs.
De ce fait, malgré les avancées en matière de prise en charge d’urgence, l’AVC ischémique reste une cause majeure d’invalidité à long terme, dont les symptômes vont des troubles de la parole à la paralysie motrice partielle ou totale. Une recherche antérieure suggère que la modulation de la gliose réactive pourrait constituer une approche prometteuse pour potentiellement inverser ces séquelles. Une nouvelle étude, dirigée par l’Université suédoise de Göteborg, fait suite à cette découverte en analysant les effets d’un peptide (C3a) intervenant spécifiquement au cours de ce processus avec le bon « timing ».
Plus de « course contre la montre »
Selon l’étude, publiée dans la revue Journal of Clinical Investigation, le traitement de l’AVC ne se cantonne désormais plus aux interventions d’urgence, dans les premières heures suivant l’apparition des symptômes. En effet, il est traditionnellement accepté que les premières minutes d’intervention influencent considérablement l’efficacité des traitements post-AVC et diminuent les risques de séquelles à long terme.
Milos Pekny, professeur au Département de neurosciences cliniques à l’Université de Göteborg et coauteur principal de l’article, explique que de manière contre intuitive, « il existe un grand potentiel d’amélioration substantielle, même à un stade ultérieur. Comme la molécule est administrée sous forme de gouttes nasales, le traitement peut être pris à domicile ».
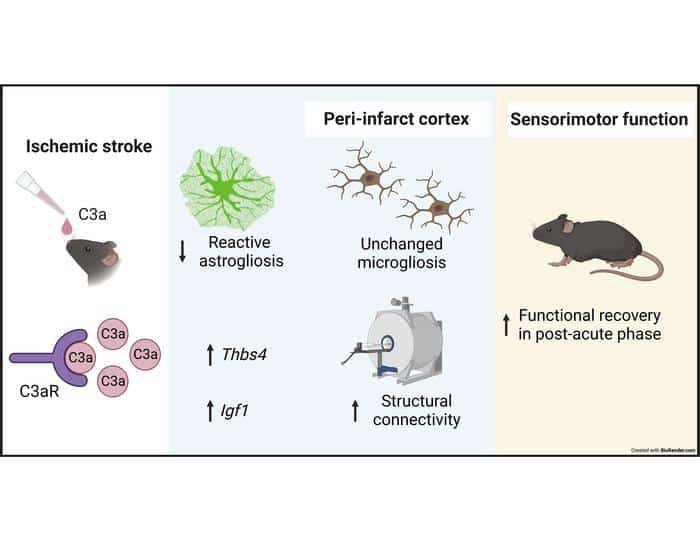
Lors de tests in vitro, les chercheurs ont découvert que le peptide C3a augmente l’expression du facteur de croissance nerveuse au niveau de la microglie et des astrocytes, améliore leur survie et réduit l’activation du GFAP à la suite d’un stress ischémique. Le peptide régule également la prolifération, la migration et la différenciation des cellules progénitrices neurales. L’activation du récepteur C3aR stimule ainsi la neurogenèse et la plasticité neuronale, dans le cortex péri-infarctus post-AVC.
Les tests in vivo sur des souris ont montré que l’instillation de gouttes nasales contenant du C3a a permis une meilleure récupération des fonctions motrices après un AVC préalablement induit. Les données d’imagerie par résonance magnétique (IRM) ont révélé une augmentation notable de connexions neuronales nouvellement établies. Ces effets ont perduré sur le long terme après l’arrêt du traitement et ont été parallèlement confirmés par des tests similaires menés par l’Université de Cologne (en Allemagne).
Cependant, il est important de noter que les gouttes doivent impérativement être instillées exactement une semaine après l’AVC. En effet, à un moment précis durant le processus de gliose réactive, la suractivation de C3aR peut contribuer à la neuropathologie en augmentant le taux de cellules inflammatoires, tel que susmentionné. Cet effet délétère de C3a est couramment observé dans la neurodégénérescence de type Alzheimer, dans la perte synaptique induite par un virus ainsi que dans la détérioration de la barrière hémato-encéphalique liée au vieillissement. En administrant trop tôt le traitement à base de C3a, la quantité de cellules inflammatoires pourrait donc être exacerbée.
Néanmoins, le traitement après sept jours élimine la nécessité d’une « course contre la montre » et améliore les chances de récupération des patients ne pouvant bénéficier de soins d’urgence. Les gouttes peuvent également être administrées en complément chez les patients présentant des séquelles après une thrombolyse (élimination chimique du caillot sanguin à l’origine de l’AVC) ou une thrombectomie (élimination mécanique du caillot sanguine).


