Un nouveau type de batterie lithium-soufre a été développé par une équipe de chercheurs de l’université du Michigan. Ils ont pour cela exploité les propriétés des nanofibres d’aramide pour améliorer considérablement les performances des batteries lithium-soufre standards.
La batterie ainsi conçue approche, selon les scientifiques, les limites théoriques des capacités d’une batterie. Sa durée de vie serait aussi augmentée, pour atteindre plus de 3500 cycles de charge théoriquement. En situation réelle cependant, cela serait sans doute moins admettent-ils, expliquant qu’on s’approcherait alors plutôt des 1000 cycles. Pour rappel, le nombre maximum de « cycles » pour une batterie représente le nombre de fois où elle peut être chargée et déchargée complètement avant qu’elle défaille ou perde en capacité de stockage.
Elle serait aussi résistante à la chaleur, jusqu’à 80 °C, ce qui en fait une candidate idéale pour des développements dans le domaine des véhicules électriques, par exemple. Dans un communiqué, l’université du Michigan affirme qu’elle serait surtout en mesure de quintupler l’autonomie des voitures électriques. Leur nouveau système de batterie semble ainsi résoudre plusieurs problèmes récurrents dans les batteries lithium-soufre existantes.
Comme le rappellent les scientifiques dans leur article, publié dans la revue Nature communications « la capacité spécifique théorique élevée de 1675 mAh g-1, le respect de l’environnement et l’abondance terrestre d’éléments formant des batteries lithium-soufre en font une plate-forme attrayante pour le stockage d’énergie dans une variété de domaines technologiques allant des véhicules électriques à la robotique, en passant par les réseaux électriques et l’ingénierie aérospatiale ». Cependant, ce type de batterie est aussi confronté à plusieurs problèmes clés qui entravent grandement leurs capacités.
Une membrane protectrice qui filtre les molécules
Premièrement, les « dendrites ». Dans une batterie, les dendrites sont de petites excroissances qui se forment par déposition de lithium, lors des cycles de déchargement et de rechargement. Elles peuvent causer des surchauffes, ou même des courts-circuits lorsqu’elles se développent assez pour relier l’anode et la cathode (les bornes « + » et « – » d’un circuit).
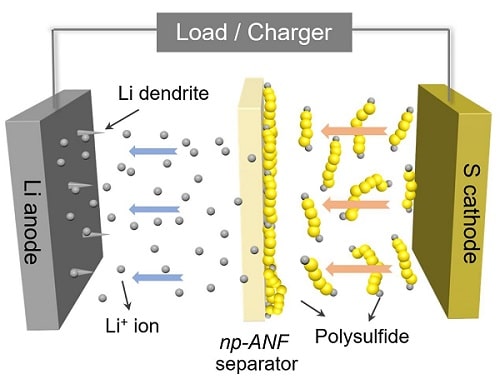
Précédemment, l’équipe de recherche avait déjà réussi à surmonter ce problème en utilisant une membrane séparatrice en nanofibres d’aramide. En effet, la solidité de ces fibres est en mesure d’empêcher la formation des dendrites. Les scientifiques précisent que les « pores » laissés par ce matériau sont de 1 nanomètre, alors que les dendrites sont de 300 nanomètres : une différence qui bloque aussi efficacement leur développement. Cette membrane présente une structure proche du cartilage, dont son utilisation s’inspire.
Autre problème : la diffusion de polysulfures de lithium de la cathode à l’anode réduit drastiquement ses capacités. En effet, le principe de fonctionnement d’une batterie lithium-ions est l’échange d’ions. Il faut donc que les ions lithium puissent transiter librement de la cathode vers l’anode et inversement. Seulement, ils ne sont pas les seuls à se promener dans la batterie. De petites molécules de lithium et de soufre, appelées polysulfures de lithium, se forment également et s’écoulent vers le lithium. Elles s’y fixent et réduisent ainsi sa capacité.
Pour contrer cela, les scientifiques s’appuient, une fois de plus, sur leur fameuse membrane en nanofibres d’aramides. Tout d’abord, les pores de 1 micromètre proposent des « voies de passage » très étroites, et réduisent la capacité des polysulfures à s’y glisser. Mais cela n’est pas tout. Les scientifiques chargent aussi la membrane en exploitant les propriétés des molécules de polysulfure. Celles-ci, chargées négativement, ont tendance à se lier à la membrane. Elles forment donc une « couche » supplémentaire qui repousse les autres molécules de même type alors que les ions-lithium, chargés positivement, peuvent passer sans problème.
Recycler des gilets pare-balles
Cette membrane, disposée en couches successives, est assez fine. Un autre avantage selon les scientifiques, puisque cela laisse plus d’espace pour les autres parties de la batterie, permettant donc d’augmenter sa capacité. Enfin, les nanofibres d’aramide sont selon eux plutôt faciles à fabriquer, voire à recycler à partir d’objets en kevlar, comme les gilets pare-balles.
« Atteindre des niveaux records pour plusieurs paramètres et pour plusieurs propriétés de matériaux est ce qui est nécessaire maintenant pour les batteries de voitures », a déclaré Nicholas Kotov, qui a dirigé la recherche. « C’est un peu similaire à la gymnastique pour les Jeux olympiques – vous devez être ‘parfait’ sur tous les points ».


