Parce qu’ils contribuent à de nombreuses réactions biochimiques, certains métaux sont indispensables au bon fonctionnement de l’organisme. Le fer et le cuivre sont ainsi connus pour jouer un rôle essentiel dans le cerveau ; sous forme d’ions, ils participent notamment à la production de neurotransmetteurs et de neuropeptides. Mais des chercheurs ont mis pour la première fois en évidence la formation de véritables dépôts de cuivre et de fer métalliques dans le cerveau de personnes atteintes de la maladie d’Alzheimer, ce qui soulève de nouvelles questions concernant leur rôle dans l’étiologie de cette maladie.
Le fer est l’oligoélément le plus important du corps humain (entre 2,5 et 4 g pour un adulte) ; c’est l’un des constituants de l’hémoglobine. Mais, tout comme le cuivre, il entre également dans la composition de certaines enzymes et protéines sur lesquelles reposent des processus clés du système nerveux. Une accumulation de ces métaux dans le cerveau pourraient toutefois s’avérer hautement toxique.
En effet, de précédents travaux de recherche ont mis en évidence le fait que le fer labile (débarrassé de ses chaînes protéiques) était associé à des troubles neurodégénératifs, tels que la maladie d’Alzheimer. Il en est de même pour le cuivre : en cas de dysmétabolisme, il peut favoriser un stress oxydatif générant des troubles du système nerveux.
Des métaux à différents états d’oxydoréduction
Plusieurs thérapies reposent aujourd’hui sur l’élimination de ces plaques amyloïdes, mais aucun traitement ne s’est révélé efficace à ce jour pour endiguer la maladie d’Alzheimer. Pour rappel, les plaques amyloïdes sont des agrégats de bêta-amyloïde qui se forment autour des neurones lors des maladies neurodégénératives ; elles nuisent au bon fonctionnement des neurones et des neurotransmetteurs. Par conséquent, les spécialistes s’interrogent sur la responsabilité réelle de ces dépôts de bêta-amyloïde dans l’apparition et l’évolution de la maladie.
Plusieurs autres pistes ont ainsi été explorées pour rechercher les causes de cette dégénérescence ; de récents travaux ont par exemple révélé que l’aluminium contribue à la pathogenèse de la maladie. Parmi les autres causes à l’étude : l’accumulation de fer minéralisé sous forme de magnétite — un oxyde de fer composé à la fois de Fe(III) et de Fe(II), source potentielle de toxicité cellulaire.
Afin de comprendre le rôle des métaux dans l’apparition de la démence, une équipe de l’Université de Keele au Royaume-Uni a entrepris de rechercher des traces de fer et de cuivre au sein des plaques amyloïdes prélevées sur les lobes frontaux et temporaux de deux patients décédés de la maladie d’Alzheimer. Les échantillons ont été analysés par microscopie à rayons X à transmission à balayage synchrotron, afin de déterminer la distribution spatiale et l’état chimique de chaque métal.
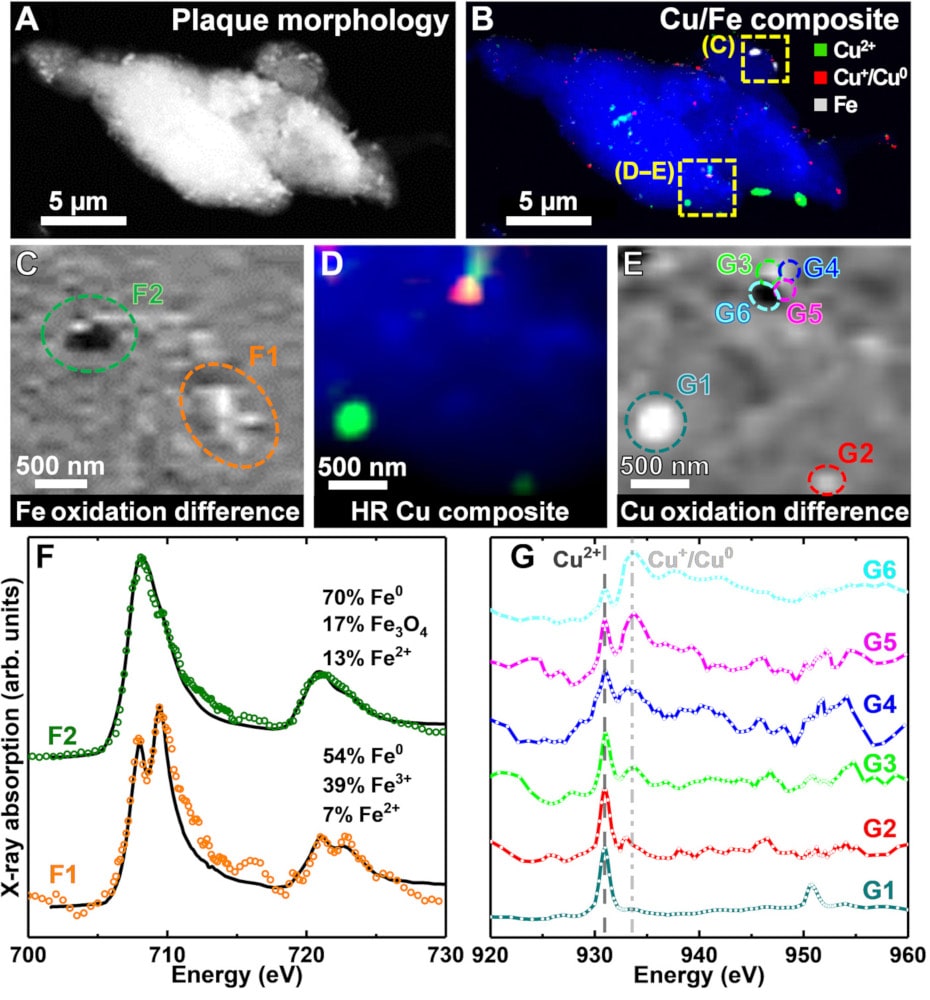
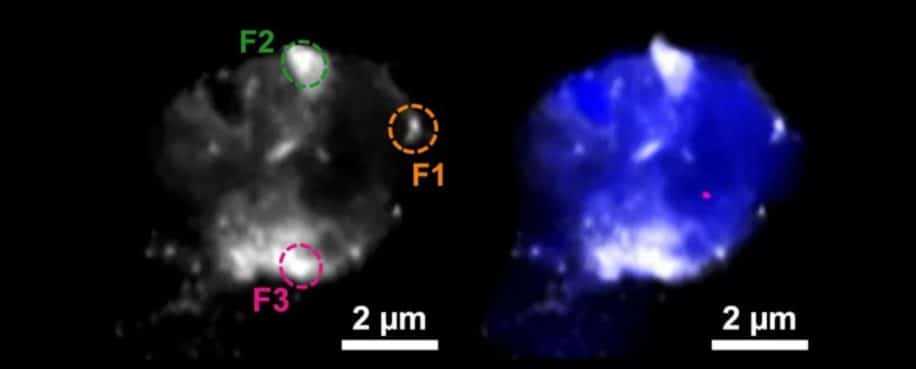
C’est ainsi que les chercheurs ont pu détecter plusieurs accumulations de fer et de cuivre à l’échelle nanométrique, y compris dans leur état élémentaire (Cu0 et Fe0), qui s’avère encore plus réactif que les oxydes dont il est issu ; les deux métaux se trouvaient dans différents états de réduction au sein d’une même plaque amyloïde. La présence de ces métaux sous plusieurs états ionisés aux côtés de leur forme métallique suggère qu’ils pourraient jouer un rôle dans l’inflammation, voire la mort des cellules neuronales.
Vers un diagnostic plus précoce de la maladie
Ce n’est pas la première fois que des scientifiques rapportent la présence de dépôts de fer dans les tissus cérébraux humains : une étude publiée en 1992 faisait déjà état du phénomène ; des traces de magnétite minérale magnétique (Fe3O4) avaient été détectées dans divers tissus du cerveau humain. Des agrégats de fer ont également déjà été identifiés chez certaines bactéries et quelques espèces animales.
En revanche, les chercheurs précisent qu’il s’agit de la première découverte de Cu0 dans les tissus humains. En d’autres termes, cela signifie que les réactions de réduction et d’oxydation du cuivre peuvent elles aussi se produire au sein de ces structures cérébrales. « L’identification inattendue de Cu0 et Fe0 dans les plaques amyloïdes de la maladie d’Alzheimer suggère que des éléments métalliques biogéniques, observés auparavant uniquement dans les micro-organismes, les virus et les plantes, peuvent également se produire chez l’homme », écrivent les auteurs de l’étude. Ces nanoparticules de métal sont très réactives et sont donc susceptibles d’endommager les cellules neuronales.
L’équipe souligne que d’autres analyses seront nécessaires, afin de vérifier si les métaux apparaissent dans les cerveaux d’autres patients atteints de la maladie et si le phénomène se produit également dans le cerveau de personnes atteintes d’autres troubles cérébraux dégénératifs. Cette découverte ne mènera pas nécessairement à de nouvelles voies de traitement. Mais elle pourrait en revanche aider à mettre en œuvre un diagnostic plus précoce de la maladie d’Alzheimer ou encore, à distinguer les différents sous-types de la maladie afin d’améliorer la prise en charge des patients.