Une étude suggère que l’acide oxalique, une molécule présente dans de nombreux aliments, favorise l’accumulation de gadolinium — un métal toxique utilisé dans les produits de contraste pour IRM — dans les tissus. Cela pourrait expliquer pourquoi certaines personnes réagissent fortement aux produits de contraste, tandis que d’autres ne réagissent pas. L’accumulation du métal est associée à de graves affections au niveau des reins et d’autres organes.
Les agents de contraste à base de gadolinium sont parfois injectés avant les examens d’imagerie par résonance magnétique (IRM) afin d’améliorer la visibilité des organes internes et la netteté des images. Le gadolinium cationique améliore la qualité des images grâce à ses caractéristiques paramagnétiques uniques. Il possède également un noyau métallique paramagnétique et un ligand chélateur qui atténue sa toxicité pour l’organisme. Ce ligand lui permet notamment d’être facilement excrété par l’organisme via l’urine.
Si la plupart des patients ne présentent pas d’effets secondaires aux produits de contraste, d’autres manifestent de fortes réactions. Des études ont montré que l’accumulation de produits de contraste à base de gadolinium est associée à des affections graves, telles que des lésions rénales aiguës, une encéphalopathie au gadolinium et une fibrose systémique néphrogénique. Cette dernière entraîne un épaississement et un durcissement de la peau, des tissus pulmonaires et cardiaques, ainsi que des contractures articulaires douloureuses.
Selon Brent Wagner, professeur au Département de médecine interne de la Faculté de médecine de l’Université du Nouveau-Mexique, « des personnes ont succombé après une seule dose de produit de contraste à base de gadolinium ». En 2006, des néphrologues ont confirmé l’implication directe du gadolinium dans la fibrose systémique néphrogénique.
Cependant, des recherches ont également montré que des particules de gadolinium ont été détectées au niveau des reins et du cerveau chez des personnes asymptomatiques. Le métal a aussi été retrouvé dans leur sang et leur urine plusieurs années après l’exposition. Les chercheurs se sont alors demandés pourquoi certaines personnes réagissent à l’accumulation de la molécule tandis que d’autres ne réagissent pas, et comment le métal se dissocie de ses ligands chélateurs pour persister dans les tissus.
Wagner et ses collègues ont mis en évidence un facteur spécifique qui pourrait expliquer la raison pour laquelle l’accumulation de ces particules provoque des effets différents selon les individus. « Près de la moitié des patients n’avaient été exposés qu’une seule fois, ce qui signifie qu’un élément amplifie le signal de la maladie », explique l’expert. « Cette formation de nanoparticules pourrait expliquer plusieurs choses. Elle pourrait expliquer l’intensité de certains cas. Lorsqu’une cellule tente de gérer cette nanoparticule métallique étrangère qu’elle contient, elle envoie des signaux qui indiquent à l’organisme d’y réagir. »
Une infiltration facilitée au niveau des tissus et des organes
L’équipe de Wagner s’est concentrée sur l’acide oxalique, car il se lie aux ions métalliques et est présent dans l’organisme à des concentrations variées selon le régime alimentaire et d’autres facteurs. Il s’agit d’un composé que l’on retrouve dans de nombreux aliments d’origine végétale, tels que les noix, les baies, les épinards, la rhubarbe ou le chocolat. Son interaction avec les ions métalliques provoque une réaction liant l’oxalate avec le calcium, ce qui favorise la formation de calculs rénaux. L’acide oxalique s’accumule également dans l’organisme après la consommation d’aliments ou de compléments alimentaires riches en vitamine C.
« Un dépôt de gadolinium a été observé avec toutes les marques d’agents de contraste d’imagerie par résonance magnétique », indiquent les chercheurs dans leur étude, publiée dans la revue Magnetic Resonance Imaging. Or, « hormis les métaux endogènes et les conditions acides, peu d’attention a été accordée au rôle du milieu biologique dans la dégradation des agents de contraste d’imagerie par résonance magnétique en nanoparticules. »
Au cours de leurs expériences, les chercheurs ont constaté que l’acide oxalique provoquait la précipitation de petites quantités de gadolinium et la formation de nanoparticules métalliques. L’acide oxalique entraînait la dissociation du métal des autres molécules constituant l’agent de contraste. Sous forme de nanoparticules, le métal s’infiltre ensuite plus facilement dans les tissus et les organes.
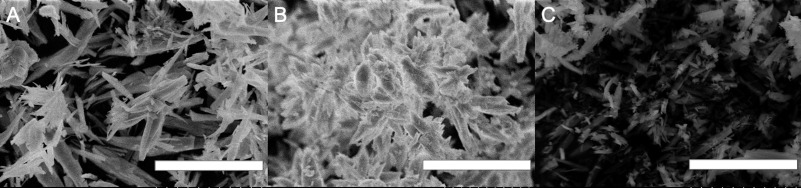
Certaines personnes formeraient des nanoparticules et d’autres non en raison de différences entre leurs milieux métaboliques. « Cela pourrait être dû à un état oxalique élevé ou à un état où les molécules sont plus susceptibles de se lier au gadolinium, entraînant la formation de nanoparticules », suggère Wagner. Cela pourrait expliquer pourquoi certaines personnes présentent des symptômes graves, même après une seule injection de produit de contraste à base de gadolinium.
D’après l’équipe, aucun autre agent thérapeutique ou pharmaceutique n’a, à ce jour, été associé à la formation spontanée de telles nanoparticules in vivo. Toutefois, davantage de recherches sont nécessaires afin de déterminer les implications exactes de cette interaction chimique pour la santé. Néanmoins, ces résultats suggèrent une nouvelle stratégie de prévention quant aux risques associés à l’IRM. « Je ne prendrais pas de vitamine C si je devais passer une IRM avec produit de contraste en raison de la réactivité du métal (à cette dernière) », affirme Wagner.
La prochaine étape de la recherche consistera à identifier les personnes les plus exposées à ces produits pour en étudier les effets sur leur organisme. L’équipe prévoit de les interroger sur leurs antécédents médicaux et leur prise de compléments alimentaires et de prélever des échantillons susceptibles de mettre en évidence l’accumulation de gadolinium.