Marcher sur un lac gelé ou sur une plaque de verglas résulte souvent en une glissade pouvant avoir de fâcheuses conséquences. C’est donc un fait connu de tous : la glace nous fait glisser. Cependant, la cause de ce phénomène de glissade n’est pas aussi certaine qu’elle apparaît de prime abord. Plusieurs théories ont tenté de répondre à cette question, et ce n’est que récemment que des physiciens ont pu apporter une explication précise au phénomène.
Parce que la glace est moins dense que l’eau liquide, son point de fusion est abaissé sous des pressions élevées. Une théorie de longue date suggère que c’est ce qui rend la glace glissante : lorsque vous marchez dessus, la pression de votre masse fait fondre la couche supérieure en eau.
« Je pense que tout le monde convient que cela ne peut pas être le cas. Les pressions devraient être si extrêmes que vous ne pouvez même pas y parvenir en y mettant un éléphant », déclare Mischa Bonn, directeur du département de spectroscopie moléculaire de l’Institut Max Planck pour la recherche sur les polymères en Allemagne.
Une autre théorie dit que la chaleur créée par la friction lorsque vous vous déplacez sur la glace produit la couche d’eau. Cependant, la glace n’est pas seulement glissante lorsque vous vous déplacez, comme le découvre rapidement quiconque essaie de se tenir debout sur des patins à glace pour la première fois. Même si la pression ou la friction faisaient fondre la glace, une couche d’eau pourrait-elle expliquer cet aspect glissant ? Daniel Bonn, physicien à l’Université d’Amsterdam, ne le pense pas.
Des molécules d’eau en vrac faisant office de « roulements à billes »
« La théorie de la couche d’eau n’a pas beaucoup de sens. Si vous renversez de l’eau sur le sol de votre cuisine, il devient glissant mais pas très glissant non plus… Une simple couche d’eau ne suffit pas ». Mischa et Daniel Bonn ont publié un article dans la revue The Journal of Chemical Physics décrivant la surface de la glace. Plutôt qu’une couche d’eau liquide à la surface de la glace, ils ont découvert qu’il y avait des molécules d’eau en vrac.
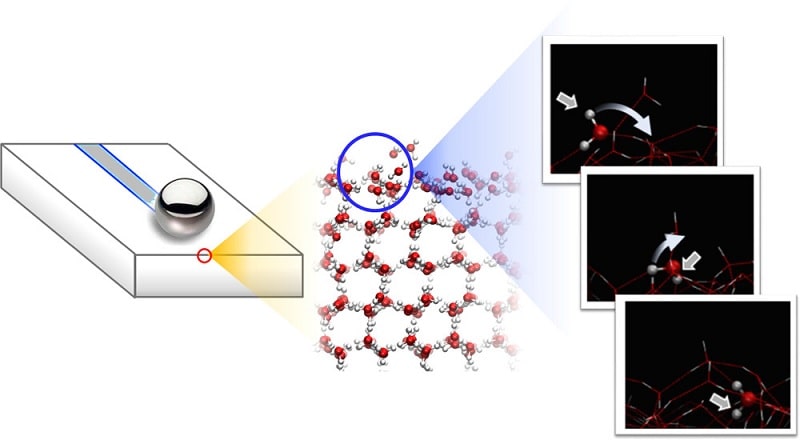
Les chercheurs comparent cela à une piste de danse « remplie de billes ou de roulements à billes ». Glisser sur la surface de la glace, c’est simplement « rouler » sur ces billes moléculaires. La glace a une structure cristalline très régulière, où chaque molécule d’eau du cristal est attachée à trois autres. Les molécules en surface, cependant, ne peuvent être attachées qu’à deux autres. Le fait d’être si faiblement liées au cristal permet à ces molécules de surface de tomber, de se fixer et de se détacher à divers sites du cristal à mesure qu’elles se déplacent.
Sur le même sujet : D’où vient la sensation de « cerveau gelé » après avoir mangé une glace ?
Même si le glissement sur la glace est essentiellement causé par le roulement sur ces molécules d’eau, cette couche de molécules n’est pas la même qu’une couche d’eau liquide. Ces molécules et la glisse existent à des températures bien inférieures au point de congélation de l’eau. En fait, la façon dont ces molécules se déplacent si librement et se diffusent sur la surface les fait ressembler davantage à un gaz.
Mais si la glace est glissante à cause de molécules de surface lâches, seule la glace est-elle glissante ? Pas vraiment, explique Martin Truffer, professeur de physique à l’Université d’Alaska. Ce n’est pas tant la nature de la glace qui est unique, mais plutôt notre relation avec elle. « Ce qui est inhabituel à propos de la glace, c’est que nous la rencontrons généralement si près du point de fusion. C’est vraiment le seul matériau où nous avons la phase gazeuse, la phase liquide et la phase solide dans la plage climatique normale dans laquelle nous vivons ».

